
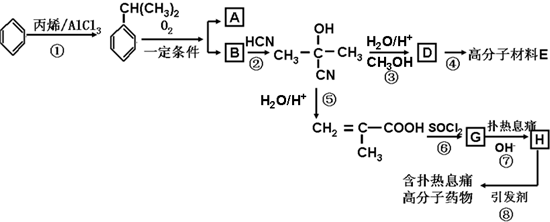
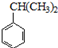
 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色;反应②为加成反应
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色;反应②为加成反应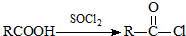
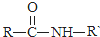
| NaOH溶液 |
 属于芳香烃的同分异构体的同系物制备
属于芳香烃的同分异构体的同系物制备 的合成路线,
的合成路线,| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
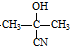 ,则B为丙酮,1mol
,则B为丙酮,1mol  可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是苯酚,
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是苯酚, 发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=
发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=| 60% |
| 12 |
| 8% |
| 1 |
| 32% |
| 16 |
| 2×5+2-8 |
| 2 |
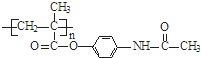
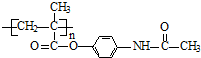 ,则H为
,则H为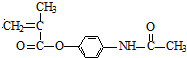 ,据此进行解答.
,据此进行解答. ,则B为丙酮,1mol
,则B为丙酮,1mol  可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是苯酚,
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,说明A中含有酚羟基,根据碳原子守恒知A是苯酚, 发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=
发生反应生成D,D蒸气密度是相同状态下甲烷密度的6.25倍,则D的相对分子质量是100,D中各元素的质量分数分别为碳60%,氢8%,氧32%,则碳、氢、氧原子个数比=| 60% |
| 12 |
| 8% |
| 1 |
| 32% |
| 16 |
| 2×5+2-8 |
| 2 |
 ,则H为
,则H为 ,
, ,
, ;
;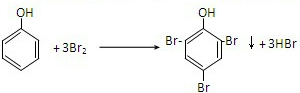 ,
, ;
;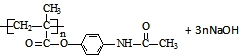 →
→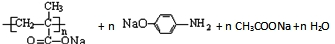 ,
, →
→ ;
; 的属于芳香烃的同分异构体的同系物为甲苯,用甲苯制备
的属于芳香烃的同分异构体的同系物为甲苯,用甲苯制备 的合成路线为:
的合成路线为: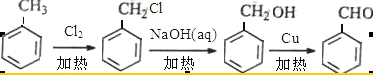 ,
, .
.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
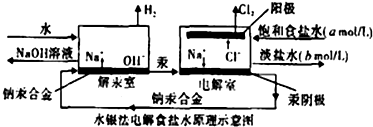 水银法电解食盐水是氯碱工业发展进程中的重要里程碑,以制得碱液纯度高、质量好而著称,其生产原理示意图如图.下列说法正确的是( )
水银法电解食盐水是氯碱工业发展进程中的重要里程碑,以制得碱液纯度高、质量好而著称,其生产原理示意图如图.下列说法正确的是( )| A、钠汞合金中钠的化合价为+1价 |
| B、电解室中产生氯气的电极为阳极,产生氢气的电极为阴极 |
| C、当阳极产生3.36 m3(标准状况)Cl2时,解汞室中生成NaOH的质量为24kg |
| D、目前氯碱生产采用离子膜法取代了水银法,其主要原因是汞有毒性,对环境有污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
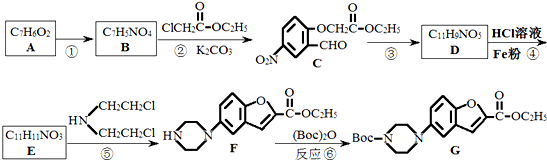
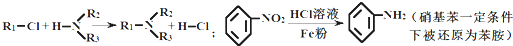
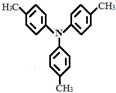 ,请设计合成路线(无机试剂及溶剂任选).
,请设计合成路线(无机试剂及溶剂任选).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
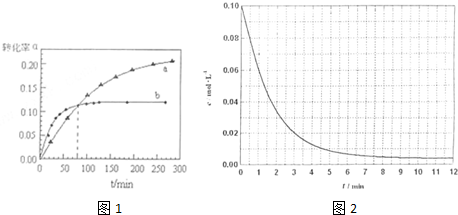
| △n(40℃) |
| △n(60℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
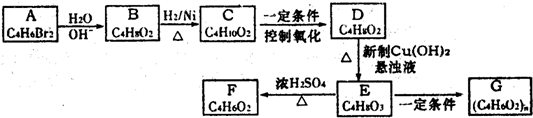
查看答案和解析>>
科目:高中化学 来源: 题型:
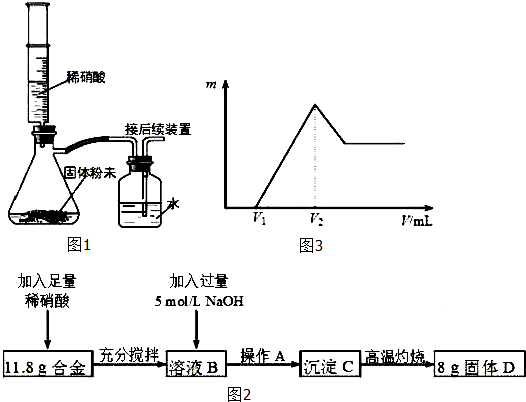
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用福尔马林浸泡海鲜防止鱼虾变质 |
| B、用小苏打做发酵粉制面包 |
| C、二氧化硫可广泛用于食品的增白 |
| D、向乳制品中添加三聚氰胺以提高含氮量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com