
【题目】甲烷、乙烯、乙醇都是重要的有机化合物。请回答下列问题:
(1)甲烷与氯气的第一步取代反应的化学方程式为_______。
(2)把乙烯通入到溴的四氯化碳溶液中,充分振荡、静置,观察到溴的四氯化碳溶液褪色,写出该过程中发生反应的化学方程式_______。
(3)下列几组物质中,互为同分异构体的是____;互为同系物的是____;同素异形体的是_____。
A.甲烷与新戊烷 B.氧气和臭氧 C.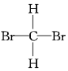 和
和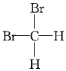
D.35Cl和37Cl E.CH3CH2OH和CH3OCH3
【答案】CH4+Cl2![]() CH3Cl+HCl CH2=CH2+Br2
CH3Cl+HCl CH2=CH2+Br2![]() CH2BrCH2Br E A B
CH2BrCH2Br E A B
【解析】
(1)烷烃发生取代反应是逐步进行的,据此书写反应方程式。
(2)乙烯与溴单质发生加成反应产生1,2-二溴乙烷;
(3)同分异构体是分子式相同、结构不同的化合物;同系物是结构相似,在分子组成上相差一个或若干个CH2原子团的化合物;同素异形体是由同种元素组成的不同性质的单质。
(1)甲烷与Cl2在光照条件下发取代反应,首先发生反应,产生一氯甲烷和HCl,反应方程式为CH4+Cl2![]() CH3Cl+HCl,反应产生的CH3Cl会进一步发生取代反应,产生CH2Cl2、CHCl3、CCl4;
CH3Cl+HCl,反应产生的CH3Cl会进一步发生取代反应,产生CH2Cl2、CHCl3、CCl4;
(2)乙烯分子中含有碳碳双键,通入溴的四氯化碳溶液中,与溴发生加成反应,产生1,2-二溴乙烷,反应方程式为CH2=CH2+Br2![]() CH2BrCH2Br;
CH2BrCH2Br;
(3)A.甲烷与新戊烷都是烷烃,属于同系物;
B.氧气与臭氧是同一元素的不同性质的单质,互为同素异形体;
C.由于甲烷是正四面体结构,任何两个化学键都相邻,因此这两个结构表示的是同一物质;
D. 35Cl和37Cl是表示的是Cl元素的两种不同原子,互为同位素;
E.CH3CH2OH和CH3OCH3分子式相同,结构不同,互为同分异构体;
故互为同分异构体的是E;互为同系物的是A;同素异形体的是B。


科目:高中化学 来源: 题型:
【题目】如图为元素周期表短周期的一部分,下列关于X、Y、Z、M的说法中正确的是( )
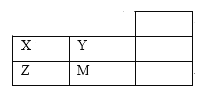
A. ZX2形成的晶体为分子晶体
B. Y的最高正价等于其最外层电子数
C. 原子半径:M>Z>Y
D. 非金属性:Z>X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3—、SO42—、CO32—,已知:
①五种盐均溶于水,水溶液均为无色;
②D的焰色反应呈黄色;
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性;
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀;
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失;
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀;
已知:向Ag+溶液中滴加氨水,先产生沉淀,继续滴加氨水,沉淀溶解。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是_____;所含阴离子相同的两种盐的化学式是________。
(2)D的化学式为____________,D溶液显碱性的原因是(用离子方程式表示)_____________。
(3)A和C的溶液反应的离子方程式是_______________;E和氨水反应的离子方程式是_______________。
(4)若要检验B中所含的阳离子,正确的实验方法是:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Mg2+、Cu2+、Ba2+、C1—、SO42—、CO32-。将该混合物溶于水后得无色澄清溶液,现分别取3份100mL该溶液进行如下实验:
实验序号 | 实验内容 | 实验结果 |
a | 加AgNO3溶液 | 有白色沉淀生成 |
b | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
c | 加足量BaC12溶液,将所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
试回答下列问题:
(1)该混合物中一定不存在的离子是______________________。
(2)试写出实验b发生反应的离子方程式_______________________。
(3)溶液中一定存在的阴离子及其物质的量浓度(可不填满):
阴离子符号 | 物质的量浓度(mol·L—1) |
___________ | ___________ |
___________ | ___________ |
(4)判断混合物中是否存在K+,如果不存在,请说明理由,如果存在,请求出C(K+)的取值范围?______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过如下流程制备氧化亚铜:
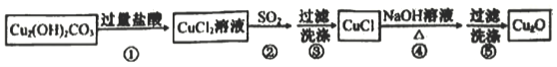
已知CuCl难溶于水和稀硫酸:Cu2O+2H+==Cu2++Cu+H2O
下列说法不正确的是
A. 步骤②SO2可用Na2SO3替换
B. 步骤③中为防止CuCl被氧化,可用SO2水溶液洗涤
C. 步骤④发生反应的离子方程式为2CuCl+2OH-=Cu2O+2Cl-+H2O
D. 如果Cu2O试样中混有CuCl和CuO杂质,用足量稀硫酸与Cu2O试样充分反应,根据反应前、后固体质量可计算试样纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两个装置的烧杯中分别盛有足量的CuCl2溶液。
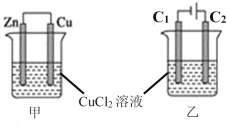
(1)甲装置中,Zn电极发生______反应(填“氧化”或“还原”),溶液中Cl-向_____极(填“Zn”或“Cu”)移动,Zn电极反应式为_______,若反应过程中有0.1mol电子发生转移,则Cu极质量增加__________。
(2)乙装置中,石墨电极C1是_______极,现象是______,C2极电极反应式为_______,若反应过程中阴极析出12.8g的Cu,则阳极产生的气体在标准状况下的体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定条件下一定能大量共存的是
A. 使甲基橙呈黄色的溶液中:![]()
B. 使![]() 试纸显蓝色的溶液中:
试纸显蓝色的溶液中:![]()
C. 由水电离出的![]() mol
mol ![]() L-1的溶液中:
L-1的溶液中:![]()
D. 与铝反应生成![]() 的溶液中:
的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是
A. (CN)2+H2===2HCN
B. MnO2+4HCN![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 将(CN)2通入水中:(CN)2+H2O ===HCN+ HCNO
D. 在NaI和KCN混合液中通入少量Cl2:Cl2+2KCN===2KCl+(CN)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com