
����Ŀ�������ϰ�һ���������з����˴����δ����������������˲��õ��л����������̥���ԭ��--������![]() ���ɲ�����ʯ��̥��������ϵijɷ���Ҫ�Ǽس�ʯ
���ɲ�����ʯ��̥��������ϵijɷ���Ҫ�Ǽس�ʯ![]() ����
����![]() ����һ���ճɵ��Կ��γɾ�������ɡ�
����һ���ճɵ��Կ��γɾ�������ɡ�
![]() ������������
������������![]() ______�����______
______�����______![]() ���������������������������β�Ʒ��
���������������������������β�Ʒ��
![]() �����ϰ�һ��������ֱ�������У����øߴ���
�����ϰ�һ��������ֱ�������У����øߴ���![]() ����Ĺ��ˡ���ͼ���ú��ߵ�ʯӢɰ
����Ĺ��ˡ���ͼ���ú��ߵ�ʯӢɰ![]() ���Ȼ��ơ�������������
���Ȼ��ơ�������������![]() �Ʊ���������ֲ�Ʒ�Ĺ������̡�
�Ʊ���������ֲ�Ʒ�Ĺ������̡�
��ϴ��ʯӢɰ��Ŀ����______��
�������������У�Ҫ��ϴ����ʯӢɰ��ĥ�ɷ�ĩ��Ŀ����______��
![]() ��ҵ�ϳ��ö���������̼�ڸ����·�����Ӧ����ֹ裬�ֹ��к���SiC����������Si��SiC�����ʵ���֮��Ϊ1��
��ҵ�ϳ��ö���������̼�ڸ����·�����Ӧ����ֹ裬�ֹ��к���SiC����������Si��SiC�����ʵ���֮��Ϊ1��![]() д���仯ѧ����ʽ______��
д���仯ѧ����ʽ______��

���𰸡�4 ���� ��ȥ������NaCl���� ����Ӵ�������ӿ췴Ӧ���ʣ��������Ч�� 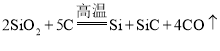
��������
![]() ���ݻ��ϼ۴�����Ϊ����㣻�����β�Ʒ���Ժ�������Ϊԭ�Ͼ������Ƴɵ���Ҫ������ˮ�ࡢ�������մɣ�
���ݻ��ϼ۴�����Ϊ����㣻�����β�Ʒ���Ժ�������Ϊԭ�Ͼ������Ƴɵ���Ҫ������ˮ�ࡢ�������մɣ�
![]() ϴ��ʯӢɰ��Ŀ����Ϊ�˳�ȥ���������ʣ�
ϴ��ʯӢɰ��Ŀ����Ϊ�˳�ȥ���������ʣ�![]() ��ϴ����ʯӢɰ��ĥ�ɷ�ĩ������Ӵ�������ӿ췴Ӧ���ʣ��������Ч�ʣ�
��ϴ����ʯӢɰ��ĥ�ɷ�ĩ������Ӵ�������ӿ췴Ӧ���ʣ��������Ч�ʣ�
![]() ������Ŀ��Ϣ��������غ㣬������д��ѧ��Ӧ����ʽ��
������Ŀ��Ϣ��������غ㣬������д��ѧ��Ӧ����ʽ��
��1��������![]() �У���Ϊ
�У���Ϊ![]() �ۣ���Ϊ
�ۣ���Ϊ![]() �ۣ���Ϊ
�ۣ���Ϊ![]() �ۣ����ݴ�����Ϊ�㣬��֪���������Ӹ���Ϊ4����������������
�ۣ����ݴ�����Ϊ�㣬��֪���������Ӹ���Ϊ4����������������![]() ��ˮ�ࡢ�������մɶ��Ǵ�ͳ���ǽ������ϣ���Ҫ�ǹ����β�Ʒ���Ʊ�ԭ�϶���Ҫ�õ�����Ԫ�ص����ʣ���������ڹ����β�Ʒ��
��ˮ�ࡢ�������մɶ��Ǵ�ͳ���ǽ������ϣ���Ҫ�ǹ����β�Ʒ���Ʊ�ԭ�϶���Ҫ�õ�����Ԫ�ص����ʣ���������ڹ����β�Ʒ��
�ʴ�Ϊ��4�����ڣ�
![]() ϴ��ʯӢɰ��Ŀ����Ϊ�˳�ȥ������NaCl���ʣ�
ϴ��ʯӢɰ��Ŀ����Ϊ�˳�ȥ������NaCl���ʣ�
�ʴ�Ϊ����ȥ������NaCl���ʣ�
![]() �����������У�Ҫ��ϴ����ʯӢɰ��ĥ�ɷ�ĩ��Ŀ��������Ӵ�������ӿ췴Ӧ���ʣ��������Ч�ʣ�
�����������У�Ҫ��ϴ����ʯӢɰ��ĥ�ɷ�ĩ��Ŀ��������Ӵ�������ӿ췴Ӧ���ʣ��������Ч�ʣ�
�ʴ�Ϊ������Ӵ�������ӿ췴Ӧ���ʣ��������Ч�ʣ�
![]() ����ֹ�ʱ�ķ�ӦΪ
����ֹ�ʱ�ķ�ӦΪ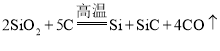 ����������ֹ��к���SiC������Si��SiC�����ʵ���֮��Ϊ1��1��
����������ֹ��к���SiC������Si��SiC�����ʵ���֮��Ϊ1��1��
�ʴ�Ϊ��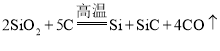 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�������һ��2L���ܱ�������������4 molA��2molB�������·�Ӧ��
3A(g)+2B(g)![]() 4C(s)+D(g)����Ӧ2 min��ﵽƽ�����������1.6 mol C������˵����ȷ����( )
4C(s)+D(g)����Ӧ2 min��ﵽƽ�����������1.6 mol C������˵����ȷ����( )
A. ǰ2min��D��ƽ����Ӧ����Ϊ0.2mol/(L��min)
B. ��ʱ��B��ƽ��ת������40��
C. ����B��ƽ�������ƶ���B��ƽ��ת��������
D. �������ϵ��ѹǿ��ƽ�ⲻ�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ�����pH=1��������Һ���й�������
�ٸ���Һ1mLϡ����100mL��pH=3
�������Һ�м���������pH=13������������Һǡ����ȫ�к�
�۸���Һ������������c(H+)��ˮ�������c(H+)֮��ֵΪ1��10��12
�������Һ�м�����������Ũ�ȵİ�ˮ��������ҺpH=7
������ȷ����
A. �٢� B. �٢� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25��ʱ,���ᡢ̼���������ĵ���ƽ�ⳣ�����±���ʾ:
�� | ����ƽ�ⳣ�� |
���� |
|
̼�� |
|
������ |
|
�������ᷢ������ķ���ʽΪ____________________________________________��
��̼���������ĵ�һ������̶ȴ��ڵڶ�������̶ȵ�ԭ��:_____________________��
������ͬ������,�ԱȽ�![]() ��
��![]() ��
��![]() ������ǿ��:_______> ______>_______��
������ǿ��:_______> ______>_______��
�ܽ�pH=4��![]() ��Һϡ��100������Һ��pH��Χ��______________________,ͼ�е������������_______________________��
��Һϡ��100������Һ��pH��Χ��______________________,ͼ�е������������_______________________��
a.��Һ��pH b.����ĵ���ƽ�ⳣ�� c.��Һ�ĵ������� d.����ĵ���̶�
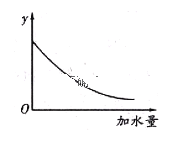
��������ij�ʼŨ��Ϊ0.01 mol/L��ƽ��ʱ������Ũ����________________________��д����ϸ���ⲽ�裩
��д��������������̼���Ʒ�Ӧ�����ӷ���ʽ_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ���ݻ��̶����ܱ��������п��淴Ӧ A2(g) + B2(g)![]() 2AB(g)���ﵽƽ��ı�־��
2AB(g)���ﵽƽ��ı�־��
A.�������������ѹǿ����ʱ��ı仯���仯
B.��λʱ��������n mol A2ͬʱ����2 n mol AB����
C.������������ܶȲ���ʱ��ı仯���仯
D.��λʱ������n mol B2����ͬʱ����n mol AB�ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��Ҫ����ѡ�����αװͿ�ϵ����ϵȡ����ܿ�ʯ
��Ҫ����ѡ�����αװͿ�ϵ����ϵȡ����ܿ�ʯ![]() ��
��![]() ��CoO������
��CoO������![]() ��
��![]() ��
��![]() ��
��![]() ����
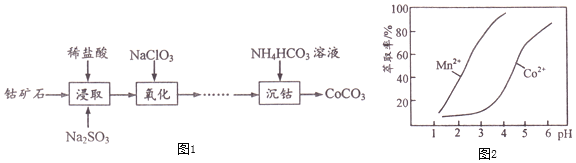
����![]() ��������ͼ1��
��������ͼ1��
�±��г��˼������������������������pH![]() ��������ȫ����ָ��Һ������Ũ�ȵ���
��������ȫ����ָ��Һ������Ũ�ȵ���![]()
|
|
|
|
| |
��ʼ������pH |
|
|
|
|
|
������ȫ��pH |
|
|
|
|
|
![]() д������ȡ������
д������ȡ������![]() ������Ӧ�����ӷ���ʽ______��
������Ӧ�����ӷ���ʽ______��
![]() ����ȡ�������
����ȡ�������![]() �⣬�ܿ�ʯ�л��ܱ�
�⣬�ܿ�ʯ�л��ܱ�![]() ��ԭ��������______��
��ԭ��������______��
![]() ��
��![]() ��Ŀ��������
��Ŀ��������![]() ��
��![]() �������������ɵIJ��������______��
�������������ɵIJ��������______��
![]() ��������������
��������������![]() ��Һ����
��Һ����![]() ��Һ��Ҫ
��Һ��Ҫ![]() �����½��У����˵ļ��ȷ�ʽΪ______���¶ȿ�����
�����½��У����˵ļ��ȷ�ʽΪ______���¶ȿ�����![]() ��ԭ��Ϊ______��
��ԭ��Ϊ______��
![]() ��֪������ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2��ʾ���벹���������������������Һ�Ʊ�
��֪������ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2��ʾ���벹���������������������Һ�Ʊ�![]() ��ʵ�鷽�������������������Һ�м���______������
��ʵ�鷽�������������������Һ�м���______������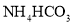 ��Һ���ܵ�
��Һ���ܵ�![]() ʵ������ʹ���Լ���
ʵ������ʹ���Լ���![]() ��Һ��������ȡ��������
��Һ��������ȡ��������![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ����������⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵���������
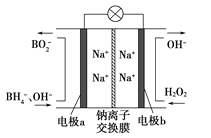
A. ��طŵ�ʱNa+��a��������b����
B. �缫b����MnO2��MnO2�����缫�������д�����
C. �õ�صĸ�����ӦΪ��BH4��+8OH�D�D8e��=BO2��+6H2O
D. ÿ����3molH2O2��ת�Ƶĵ���Ϊ3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����6mol��L-1����������100mL1mol��L-1���ᣬ��ʵ�������У�
A��100mL��Ͳ B��������ƽ C�������� D��50mL����ƿ E��20mL��Ͳ F����ͷ�ι� G��50mL�ձ� H��100mL����ƿ
��1��ʵ��ʱӦѡ���������Ⱥ�˳���ǣ������ţ�__��
��2��������ƿ��ʹ�÷����У����в�������ȷ���ǣ���д��ţ�__��
A��ʹ������ƿǰ������Ƿ�©ˮB������ƿ������ˮϴ�������ô�����Һ��ϴ
C��������Һʱ����������ǹ��壬�ѳƺõ�������ֽ��С�ĵ�������ƿ�У�������������ˮ���ӽ�����2cm��3cm�����õιܵμ�����ˮ������
D��������Һʱ�����������Һ�壬����Ͳ��ȡ������ֱ�ӵ�������ƿ�У�������������ˮ���ӽ�����ƿ�̶ȱ���1cm��2cm�����õιܵμ�����ˮ���̶���
E���Ǻ�ƿ������ʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��ת��ҡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�10mL0.40molL-1H2O2��Һ�������ֽ⡣��ͬʱ�̲������O2�����(������Ϊ��״��)���±���
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
������������ȷ����(��Һ����仯���Բ���)�� ��
A.0~6min��ƽ����Ӧ���ʣ�v(H2O2)��3.3��10-2mol��L-1��min-1
B.6~10min��ƽ����Ӧ���ʣ�v(H2O2)<3.3��10-2mol��L-1��min-1
C.��Ӧ��6minʱ��c(H2O2)=0.30mol��L-1
D.��Ӧ��6minʱ��H2O2�ֽ���50%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com