
【题目】现有下列物质:①He;②![]() ;③
;③![]() ;④CaO;⑤
;④CaO;⑤![]() ;⑥
;⑥![]() ;⑦
;⑦![]() ;⑧
;⑧![]() ;⑨KOH; 请用序号填空:
;⑨KOH; 请用序号填空:
(1)只含离子键的物质是______________;
(2)既含离子键又含共价键的物质是____;
(3)只含极性键的物质是______________;
(4)属于共价化合物的是______________;
(5)既含离子键又含非极性键的物质是______ ;
(6)不存在化学键的物质是__________ 。
【答案】④⑧ ⑤⑥⑨ ⑦ ③⑦ ⑥ ①
【解析】
一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,同种原子形成的是非极性共价键,不同种原子形成的是极性共价键,含离子键的一定为离子化合物,据此分析解答。
①He为单原子分子,不含化学键,为单质;
②N2含N≡N共价键,为单质;
③H2O2中含极性共价键和非极性共价键,为共价化合物;
④CaO只含离子键,为离子化合物;
⑤NH4Cl中含离子键和N-H极性共价键,为离子化合物;
⑥Na2O2中含离子键和O-O非极性共价键,为离子化合物;
⑦![]() 属于原子晶体,只含有极性共价键,属于共价化合物;
属于原子晶体,只含有极性共价键,属于共价化合物;
⑧MgCl2中只含离子键,为离子化合物;
⑨KOH含离子键和O-H极性共价键,为离子化合物;
(1)只含离子键的是④⑧,故答案为:④⑧;
(2)既含离子键又含共价键的物质是⑤⑥⑨,故答案为:⑤⑥⑨;
(3)只含极性键的物质是⑦,故答案为:⑦;
(4)属于共价化合物的是③⑦,故答案为:③⑦;
(5)既有离子键又有非极性键的是⑥,故答案为:⑥;
(6)不存在化学键的物质是①,故答案为:①。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】主要用于高分子胶囊和印刷油墨的粘合剂的甲基两烯酸缩水油酯GMA(即:![]() )的合成路线如下(部分反应所需试剂和条件已略去):
)的合成路线如下(部分反应所需试剂和条件已略去):

已知:
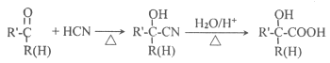
请按要求回答下列问题:
(1)GMA的分子式______________________;B中的官能团名称:______________________;甘油的系统命名:______________________。
(2)验证D中所含官能团各类的实验设计中,所需试剂有______________________。
(3)写出下列反应的化学方程式:反应⑤:____________________。反应⑧:______________________。
(4)M是H的同分异构体。M有多种同分异构体,写出满足下述所有条件的M的所有可能的结构:____________________________。
①能发生银镜反应 ②能使溴的四氯化碳溶液褪色 ③能在一定条件下水解
(5)已知: { 2 }![]()
![]()
![]() 。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯
。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯![]() Br
Br![]() ________________________。
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 可用溴的四氯化碳溶液区别![]() 和
和![]()
B. 甲苯分子中所有原子在同一平面上
C. 苯、乙酸、乙醇均能发生取代反应
D. 分子式为C3H6Cl2的同分异构体共有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】产自我国西北某盐湖的“块碱”是一种Na2CO3和NaCl的混合物。可通过以下方法对块碱样品的组成和含量进行分析测定。
Ⅰ.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加_________________溶液,能观察到有_______________________产生,说明块碱中含有NaCl。
Ⅱ.定量测定Na2CO3的含量:
准确称量w g样品置于如下装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:

(2)测定装置中,导管a的作用是___________________________________________。
(3)为提高测定的准确度,溶液b最宜选用___________________________________。
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)若根据所取样品的质量估计反应时产生的气体体积最多在30mL左右,则产生气体前对量气装置读数时,装置内的装液量和液面调节最为合理的是_______________________(填虚线框中对应这的字母编号)。
(5)用你以上所选出的最为合理的读数为起点,若终点读数为17.60mL,则反应所产生的气体的测定体积为_____________mL。若实验温度下的气体摩尔体积为VmL.mol-1,由此可得出样品中Na2CO3的含量表达式为: __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mo1 NH3时反应放出___________kJ 的热量。
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是________(填序号)。

(3)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。

①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() =1×10-12的溶液:Na+、K+、ClO-、CO32-
=1×10-12的溶液:Na+、K+、ClO-、CO32-
B. 滴入酚酞变红色的溶液:K+、Ca2+、HCO3-、CO32-
C. 能溶解Al(OH)3的溶液:K+、NH4+、NO3—、CH3COO—
D. 0.1mol/LFe(NO3)2溶液:H+、Cu2+、SO42—、Cl—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要在“校园科艺节活动”中使用氢气球表演节目。经过测量,每个氢气球的体积约为1.12L(已折成标准状况)。
已知兴趣小组采用Al和氢氧化钠溶液反应制取氢气。
(1)若实验需要1L 2.5 mol·L-1的NaOH溶液,则要用称取NaOH固体______g。配制溶液过程中所需仪器除天平、钥匙、烧杯、玻璃棒外,还需要__________、____________(填仪器名称)。
(2)若要制取60个氢气球,至少需要Al的质量为_____g,转移的电子数为________。
(3)该化学兴趣小组为了营造气氛,做了惊艳全场的铝热反应(如下图),写出该反应的化学方程式____________________________。兴趣小组同学取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因可能是______。

(4)若要除去上述所得“铁块”中含有的氧化铝,可选择____(填试剂名称),所发生反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
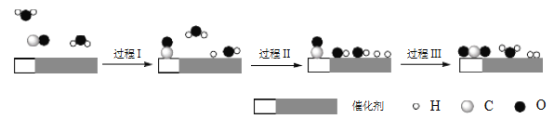
下列说法正确的是
A. 过程Ⅰ、过程Ⅲ均为放热过程
B. 过程Ⅲ生成了具有极性共价键的H2、CO2
C. 使用催化剂降低了水煤气变换反应的ΔH
D. 图示过程中的H2O均参与了反应过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温条件下,用0.100 mol·L-1的NaOH溶液分别滴定HA和HB两种酸溶液,两种酸溶液的体积均为20.00 mL,浓度均为0.100 mol·L-1,滴定曲线如图所示。下列叙述正确的是( )

A. HA可以是醋酸,HB可以是HCl
B. 浓度相等时,B-的水解程度大于HB的电离程度
C. V(NaOH)=20.00 mL时,c(Na+)=c(A-)>c(B-)
D. pH=7时,滴定HB溶液消耗的V(NaOH)>20.00 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com