
【题目】主要用于高分子胶囊和印刷油墨的粘合剂的甲基两烯酸缩水油酯GMA(即:![]() )的合成路线如下(部分反应所需试剂和条件已略去):
)的合成路线如下(部分反应所需试剂和条件已略去):

已知:
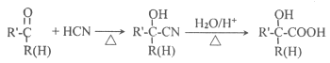
请按要求回答下列问题:
(1)GMA的分子式______________________;B中的官能团名称:______________________;甘油的系统命名:______________________。
(2)验证D中所含官能团各类的实验设计中,所需试剂有______________________。
(3)写出下列反应的化学方程式:反应⑤:____________________。反应⑧:______________________。
(4)M是H的同分异构体。M有多种同分异构体,写出满足下述所有条件的M的所有可能的结构:____________________________。
①能发生银镜反应 ②能使溴的四氯化碳溶液褪色 ③能在一定条件下水解
(5)已知: { 2 }![]()
![]()
![]() 。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯
。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯![]() Br
Br![]() ________________________。
________________________。
【答案】C7H10O3 氯原子、羟基 1,2,3-丙三醇 NaOH溶液、HNO3溶液、AgNO3溶液 2CH3CH(OH)CH3+O2![]() 2
2![]() +2H2O
+2H2O ![]() +
+![]()
![]()
![]() +H2O
+H2O ![]()
![]()
 CH2=CH-CH3
CH2=CH-CH3![]()
![]()
![]()
![]()
![]()
![]()
【解析】
甘油与HCl在催化剂存在时发生取代反应产生B:CH2(OH)CH(OH)CH2Cl,B在NaOH的乙醇溶液中,加热发生反应产生C:![]() ;丙烯与HCl发生加成反应产生D是2-氯丙烷,结构简式为:CH3CHClCH3,D与NaOH的水溶液在加热时发生取代反应,产生E是2-丙醇:CH3CH(OH)CH3,E与O2在Cu催化下,加热发生氧化反应产生F是丙酮,结构简式是
;丙烯与HCl发生加成反应产生D是2-氯丙烷,结构简式为:CH3CHClCH3,D与NaOH的水溶液在加热时发生取代反应,产生E是2-丙醇:CH3CH(OH)CH3,E与O2在Cu催化下,加热发生氧化反应产生F是丙酮,结构简式是![]() ;F在i.NaCN存在时,加热发生反应产生
;F在i.NaCN存在时,加热发生反应产生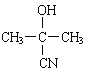 ,该物质在ii.H2O、H+作用下反应产生G:
,该物质在ii.H2O、H+作用下反应产生G: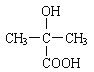 ;G与浓硫酸混合加热发生消去反应产生F:
;G与浓硫酸混合加热发生消去反应产生F:![]() ,F与C在浓硫酸作用下发生酯化反应产生
,F与C在浓硫酸作用下发生酯化反应产生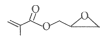 ,据此分析解答。
,据此分析解答。
(1)根据物质的结构简式可知化合物GMA的分子式为C7H10O3;化合物B结构简式为![]() ,根据物质结构可知,B中的官能团名称羟基、氯原子;甘油的系统命名为1,2,3-丙三醇;
,根据物质结构可知,B中的官能团名称羟基、氯原子;甘油的系统命名为1,2,3-丙三醇;
(2)化合物D是2-氯丙烷,官能团为Cl原子,检验Cl原子的方法是取2-氯丙烷少量,向其中加入NaOH的水溶液,加热足够长时间,然后将反应后的溶液用硝酸酸化,再向反应后的溶液中加入AgNO3溶液,若看到有白色沉淀产生,就证明其中含有Cl原子,可见检验D中含有的Cl原子。使用的试剂有:NaOH溶液、HNO3溶液、AgNO3溶液;
(3) 反应⑤是2-丙醇被氧气催化氧化产生丙酮,该反应的化学方程式:2CH3CH(OH)CH3+O2![]() 2
2![]() +2H2O。反应⑧是
+2H2O。反应⑧是![]() 与
与![]() 发生酯化反应,反应的方程式为:
发生酯化反应,反应的方程式为:![]() +
+![]()
![]()
![]() +H2O;
+H2O;
(4)H是2-甲基丙烯酸,结构简式为![]() ,M是H的同分异构体。M的同分异构体,满足条件:①能发生银镜反应 ②能使溴的四氯化碳溶液褪色 ③能在一定条件下水解,说明含有碳碳双键,含有醛基、含有酯基,应该为甲酸形成的酯,分子结构中含不饱和的碳碳双键,则M的所有可能的结构:
,M是H的同分异构体。M的同分异构体,满足条件:①能发生银镜反应 ②能使溴的四氯化碳溶液褪色 ③能在一定条件下水解,说明含有碳碳双键,含有醛基、含有酯基,应该为甲酸形成的酯,分子结构中含不饱和的碳碳双键,则M的所有可能的结构:![]()
![]()
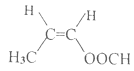
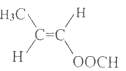 ;
;
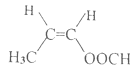
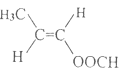
(5)丙烯CH2=CH-CH3与Br2在加热时发生取代反应产生CH2=CH-CH2Br,该物质与与O2在Ag催化下,加热发生反应产生![]() ,
,![]() 在NaOH的水溶液中加热,发生取代反应产生
在NaOH的水溶液中加热,发生取代反应产生![]() ,所以合成路线为: CH2=CH-CH3
,所以合成路线为: CH2=CH-CH3![]()
![]()
![]()
![]()
![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】某学习小组利用反应4HCl(浓)+MnO2![]() MnCl2+2H2O+Cl2↑。制取纯净、干燥的氯气,装置如图所示:
MnCl2+2H2O+Cl2↑。制取纯净、干燥的氯气,装置如图所示:

请回答下列问题:
(1)a装置的名称________
(2)收集氯气的方法有________
(3)烧瓶中发生反应的离子方程式为___________
(4)装置B中饱和食盐水的作用是_______,装置E的作用是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1molL﹣1 的 NaOH 溶液中,溶液的 pH=_____。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____, 由水电离出的 c(OH﹣)=_____molL﹣1。
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____(填“强酸”或“弱酸”),理由是_____。

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________(填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电子式的表述正确的是( )
A.HClO的电子式为
B.SCl2的电子式为
C.用电子式表示HCl的形成过程为
![]()
D.已知SCN-每个原子都达到8电子结构,则其电子式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.在任何条件下,1mol任何气体的体积都是22.4L
B.同温同压下,相同体积的两种气体物质,其物质的量一定相等
C.在相同温度下,气体分子间的平均距离几乎相等
D.测得1mol某气体的体积为22.4L,则测定条件一定是标准状况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是应用广泛的化工原料和前景乐观的无色液体燃料。请按要求回答下列问题。
(1)已知25℃、101 kpa时一些物质的燃烧热如下表:
物质 | CH3OH(l) | CO(g) | H2(g) |
燃烧热/(kJ/mol) | 726.8 | 283.0 | 285.8 |
写出由CO和H2反应生成CH3OH(l)的热化学方程式: _________________________。
(2)一定温度下,在容积为2L的恒容密闭容器中进行反应:CO(g)+2H2(g)=CH3OH(g),其相关数据如图所示。

①从反应开始至5min时,用CH3OH表示的反应平均速度为____________。
②图中反应达平衡时,K=_______(mol/L)-2;CO的平衡转化率为________________。
(3)人们利用甲醇制得能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,该装置工作时,a极反应式为____________________。

若用该电池及惰性电极电解2L饱和和食盐水产生224mL(标准误差2)Cl2时(假设全部句逸出并收集,忽略溶液体积的变化),常温下所得溶液的pH为________。
(4)甲醇在一定条件下可转化为甲酸。常温下,向0.1mol/L HCOOH溶液中滴加0.1mol/LNaOH溶液至pH=7[已知,K(HCOOH)=1.8×10-4]。此时混合游学中两溶质的物质的量之比n(HCOOH):n(HCOONa)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关![]() 和
和![]() 混合溶液的叙述正确的是( )
混合溶液的叙述正确的是( )
A. 向该溶液中加入浓盐酸,每产生![]() ,转移电子约为
,转移电子约为![]() 个
个
B. 该溶液中,![]() 可以大量共存
可以大量共存
C. 滴入少量![]() 溶液,反应的离子方程式为:
溶液,反应的离子方程式为:![]()
D. 为验证![]() 的水解,用
的水解,用![]() 试纸测该溶液的
试纸测该溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酰亚胺是重要的特种工程材料,广泛应用在航空、纳米、激光等领域。某聚酰亚胺的合成路线如下(部分反应条件略去):

已知:
①有机物A的质谱与核磁共振氢谱图如下:

②
③
回答下列问题:
(1)A的名称是__________________;C中含氧官能团的名称是________________。
(2)反应②的反应类型是____________________。
(3)反应①的化学方程式是__________________________。
(4) F的结构筒式是_____________________。
(5)同时满足下列条件的G的同分异构体共有___________种(不含立体结构);写出其中一种的结构简
式:________________。
①能发生银镜反应 ②能发生水解反应,其水解产物之一能与FeC13溶液发生显色反应
③1 mol该物质最多能与8 mol NaOH反应
(6) 参照上述合成路线,以间二甲苯和甲醇为原料(无机试剂任选)设计制备 的合成路线:_______________________。
的合成路线:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①He;②![]() ;③
;③![]() ;④CaO;⑤
;④CaO;⑤![]() ;⑥
;⑥![]() ;⑦
;⑦![]() ;⑧
;⑧![]() ;⑨KOH; 请用序号填空:
;⑨KOH; 请用序号填空:
(1)只含离子键的物质是______________;
(2)既含离子键又含共价键的物质是____;
(3)只含极性键的物质是______________;
(4)属于共价化合物的是______________;
(5)既含离子键又含非极性键的物质是______ ;
(6)不存在化学键的物质是__________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com