
【题目】聚酰亚胺是重要的特种工程材料,广泛应用在航空、纳米、激光等领域。某聚酰亚胺的合成路线如下(部分反应条件略去):

已知:
①有机物A的质谱与核磁共振氢谱图如下:

②
③
回答下列问题:
(1)A的名称是__________________;C中含氧官能团的名称是________________。
(2)反应②的反应类型是____________________。
(3)反应①的化学方程式是__________________________。
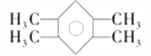
(4) F的结构筒式是_____________________。
(5)同时满足下列条件的G的同分异构体共有___________种(不含立体结构);写出其中一种的结构简
式:________________。
①能发生银镜反应 ②能发生水解反应,其水解产物之一能与FeC13溶液发生显色反应
③1 mol该物质最多能与8 mol NaOH反应
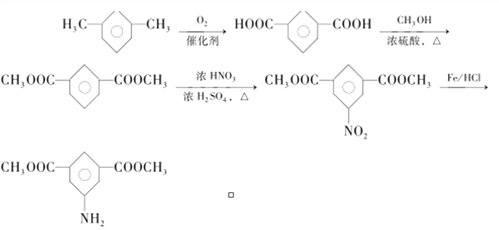
(6) 参照上述合成路线,以间二甲苯和甲醇为原料(无机试剂任选)设计制备 的合成路线:_______________________。
的合成路线:_______________________。
【答案】 乙醇 羧基 取代反应 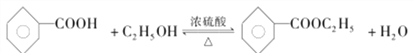
 3
3 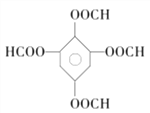
【解析】根据已知:①有机物A的质谱与核磁共振氢谱图可知,A的相对分子质量为46,核磁共振氢谱有3组峰,峰面积之比为1:2:3,则A为乙醇;根据流程可知,E在铁和氯化氢作用下发生还原反应生成 ,则E为
,则E为![]() ;E是D发生硝化反应而得,则D为
;E是D发生硝化反应而得,则D为![]() ;D是由A与C在浓硫酸作用下发生酯化反应而得,则C为
;D是由A与C在浓硫酸作用下发生酯化反应而得,则C为![]() ;C是由分子式为C7H8的烃B氧化而得,则B为甲苯;结合已知③
;C是由分子式为C7H8的烃B氧化而得,则B为甲苯;结合已知③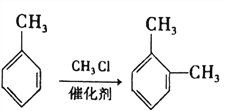 以及G的分子式,可知对二甲苯与二分子一氯甲烷反应生成F,F为
以及G的分子式,可知对二甲苯与二分子一氯甲烷反应生成F,F为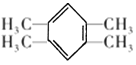 ;根据已知②
;根据已知②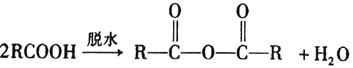 可知,F氧化生成G为
可知,F氧化生成G为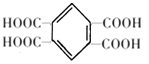 ;G脱水生成H,H为
;G脱水生成H,H为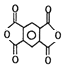 。
。
(1)A的名称是乙醇;C为![]() ,含氧官能团的名称是羧基;(2)反应②是D在浓硫酸和浓硝酸作用下发生硝化反应(或取代反应)生成E;(3)反应①是A与C在浓硫酸作用下发生酯化反应生成D,其化学方程式是
,含氧官能团的名称是羧基;(2)反应②是D在浓硫酸和浓硝酸作用下发生硝化反应(或取代反应)生成E;(3)反应①是A与C在浓硫酸作用下发生酯化反应生成D,其化学方程式是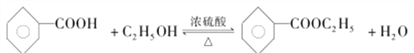 ;(4)F的结构筒式是
;(4)F的结构筒式是 ;(5)
;(5)  的同分异构体满足条件:①能发生银镜反应,说明含有醛基;②能发生水解反应,其水解产物之一能与FeC13溶液发生显色反应,说明含有甲酸酯的结构,且水解后生成物中有酚羟基结构;③1mol该物质最多能与8mol NaOH反应,则符合条件的同分异构体可以是:
的同分异构体满足条件:①能发生银镜反应,说明含有醛基;②能发生水解反应,其水解产物之一能与FeC13溶液发生显色反应,说明含有甲酸酯的结构,且水解后生成物中有酚羟基结构;③1mol该物质最多能与8mol NaOH反应,则符合条件的同分异构体可以是: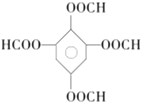 、
、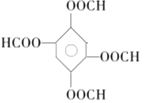 、
、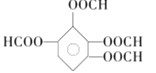 共3种;(6)间二甲苯氧化生成间苯二甲酸,间苯二甲酸与甲醇发生酯化反应生成间苯二甲酸二甲酯,间苯二甲酸甲酯发生硝化反应生成
共3种;(6)间二甲苯氧化生成间苯二甲酸,间苯二甲酸与甲醇发生酯化反应生成间苯二甲酸二甲酯,间苯二甲酸甲酯发生硝化反应生成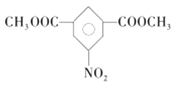 ,
, 还原得到
还原得到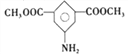 ,其合成路线为:
,其合成路线为: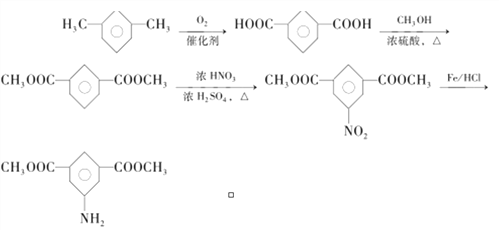 。
。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学用 NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
实验序号 | I | II | III |
盐酸体积(mL) | 100.0 | 100.0 | 100.0 |
样品质量/g | 9.2 | 15.7 | 27.6 |
CO2体积/L (标准状况) | 2.24 | 3.36 | 3.36 |
(1)该盐酸的物质的量浓度为______mol·Lˉ1
(2)使盐酸恰好完全反应,所需要的样品质量为______g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主要用于高分子胶囊和印刷油墨的粘合剂的甲基两烯酸缩水油酯GMA(即:![]() )的合成路线如下(部分反应所需试剂和条件已略去):
)的合成路线如下(部分反应所需试剂和条件已略去):

已知:
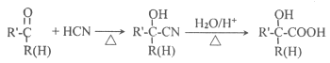
请按要求回答下列问题:
(1)GMA的分子式______________________;B中的官能团名称:______________________;甘油的系统命名:______________________。
(2)验证D中所含官能团各类的实验设计中,所需试剂有______________________。
(3)写出下列反应的化学方程式:反应⑤:____________________。反应⑧:______________________。
(4)M是H的同分异构体。M有多种同分异构体,写出满足下述所有条件的M的所有可能的结构:____________________________。
①能发生银镜反应 ②能使溴的四氯化碳溶液褪色 ③能在一定条件下水解
(5)已知: { 2 }![]()
![]()
![]() 。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯
。参照上述合成路线并结合此信息,以丙烯为原料,完善下列合成有机物C的路线流程图:丙烯![]() Br
Br![]() ________________________。
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将![]() 溶液分别滴加到浓度均为
溶液分别滴加到浓度均为![]() 的
的![]() 溶液中,所得的沉淀溶解平衡曲线如图所示(
溶液中,所得的沉淀溶解平衡曲线如图所示(![]() 用
用![]() 表示,不考虑
表示,不考虑![]() 的水解)。下列叙述正确的是( )。
的水解)。下列叙述正确的是( )。

A. ![]() 的数量级为
的数量级为![]()
B. ![]() 点对应的
点对应的![]() 溶液为不饱和溶液
溶液为不饱和溶液
C. 所用![]() 溶液的浓度为
溶液的浓度为![]()
D. ![]() 平衡常数为
平衡常数为![]() ,反应趋于完全
,反应趋于完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2熔点为-59.5℃,沸点为11.0℃,温度过高可能引起爆炸,易溶于水,易与碱液反应。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某同学设计了如图装置来制取、收集ClO2并测定其质量。

实验I:制取并收集ClO2,装置如图所示。
(1)装置A除酒精灯外,还必须添加__________装置,目的是____________。装置B应该添加_____________(填“冰水浴”、“沸水浴”或“60℃的热水浴”)装置。
(2)装置A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式_____________。
实验II:测定ClO2的质量,装置如图所示。过程如下:

①在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加![]() 硫酸溶液;
硫酸溶液;
②按照如图组装好仪器:在玻璃液封管中加入水,浸没导管口;
③将生成的ClO2气体由导管通入锥形瓶的溶液中,充分吸收后,把玻璃液封管中的水封液倒入锥形瓶中,再向锥形瓶中加入几滴淀粉溶液;
④用cmol/L Na2S2O3标准液滴定锥形瓶中的液体,共用去VmL Na2S2O3溶液(已知:I2+2S2O32-=2I-+S4O62-)。
(3)装置中玻璃液封管的作用是______________。
(4)滴定终点的现象是___________________。
(5)测得通入ClO2的质量m (ClO2)=_______![]() (用整理过的含
(用整理过的含![]() 的代数式表示)。
的代数式表示)。
(6)判断下列操作对m (ClO2)测定结果的影响(填“偏高”、“偏低”或“无影响”)。
①若在配制Na2S2O3标准溶液时,烧杯中的溶液有少量溅出,则测定结果________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下有机物:
① ![]() ②
② ![]() ③
③ ![]() ④ CH2=CH2 ⑤CH3—CH2Br
④ CH2=CH2 ⑤CH3—CH2Br
(1)能与![]() 溶液反应的有(填序号作答,以下同);______________________________
溶液反应的有(填序号作答,以下同);______________________________
(2)能与银氨溶液反应的有______________________________
(3)既能发生消去反应,又能发生酯化反应的有______________________________
(4)能发生氧化反应的有(除燃烧以外)______________________________
(5)能发生加成反应的是______________________________
(6)即能发生水解反应,又能发生消去反应的是____________
(7)乙烯生成聚乙烯反应方程式___________________________反应类型__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 可用溴的四氯化碳溶液区别![]() 和
和![]()
B. 甲苯分子中所有原子在同一平面上
C. 苯、乙酸、乙醇均能发生取代反应
D. 分子式为C3H6Cl2的同分异构体共有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】产自我国西北某盐湖的“块碱”是一种Na2CO3和NaCl的混合物。可通过以下方法对块碱样品的组成和含量进行分析测定。
Ⅰ.定性测定NaCl的存在:
(1)取样品少许溶于水,加入足量稀硝酸充分反应后再滴加_________________溶液,能观察到有_______________________产生,说明块碱中含有NaCl。
Ⅱ.定量测定Na2CO3的含量:
准确称量w g样品置于如下装置中,向其中加入足量稀硫酸,通过测定生成气体的体积来求算Na2CO3的含量。请回答下列相关问题:

(2)测定装置中,导管a的作用是___________________________________________。
(3)为提高测定的准确度,溶液b最宜选用___________________________________。
①饱和食盐水 ②饱和NaHCO3溶液 ③澄清石灰水 ④酸性KMnO4溶液
(4)若根据所取样品的质量估计反应时产生的气体体积最多在30mL左右,则产生气体前对量气装置读数时,装置内的装液量和液面调节最为合理的是_______________________(填虚线框中对应这的字母编号)。
(5)用你以上所选出的最为合理的读数为起点,若终点读数为17.60mL,则反应所产生的气体的测定体积为_____________mL。若实验温度下的气体摩尔体积为VmL.mol-1,由此可得出样品中Na2CO3的含量表达式为: __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
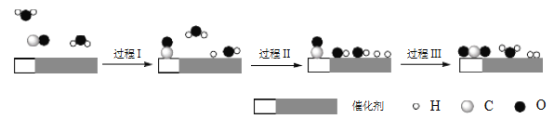
下列说法正确的是
A. 过程Ⅰ、过程Ⅲ均为放热过程
B. 过程Ⅲ生成了具有极性共价键的H2、CO2
C. 使用催化剂降低了水煤气变换反应的ΔH
D. 图示过程中的H2O均参与了反应过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com