
���� ��1����������ǿ�������ȫ����������Ӻ���������ӣ�
��2��̼������Ϊǿ����ʣ���ȫ���룬ע��̼���������Ϊ�������ʽ�����Ӳ��ܲ�
��3������������ȫ����������Ӻ����������ӣ�
��4�������������������������ط�Ӧ����������غ�ˮ��
��5������������θ���е�HCl��Ӧ�����Ȼ�����ˮ��
��6���Ȼ����������������Һ�����Ȼ��ơ�������ˮ��
��� �⣺��1����������ǿ�������ȫ����������Ӻ���������ӣ����������ӷ���ʽΪ��AgNO3=Ag++NO3-��
�ʴ�Ϊ��AgNO3=Ag++NO3-��
��2��̼������Ϊǿ����ʣ���ȫ���룬���뷽��ʽ��NaHCO3�TNa++HCO3-��
�ʴ�Ϊ��NaHCO3�TNa++HCO3-��
��3������������ȫ����������Ӻ����������ӣ����������ĵ��뷽��ʽ��Ba��OH��2=Ba2++2OH-��
�ʴ�Ϊ��Ba��OH��2=Ba2++2OH-��
��4�������������������������ط�Ӧ����������غ�ˮ���䷴Ӧ�Ļ�ѧ����ʽΪSO2+2KOH=K2SO3+H2O��
�ʴ�Ϊ��SO2+2KOH=K2SO3+H2O��
��5������������θ���е�HCl��Ӧ�����Ȼ�����ˮ����Ӧ�Ļ�ѧ����ʽΪAl��OH��3+3HCl�TAlCl3+3H2O��
�ʴ�Ϊ��Al��OH��3+3HCl�TAlCl3+3H2O��
��6���Ȼ����������������Һ�����Ȼ��ơ�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��NH4Cl+NaOH$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O+NaCl��
�ʴ�Ϊ��NH4Cl+NaOH$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O+NaCl��
���� ���⿼���˵���ʵ��뷽��ʽ����д�ͻ�ѧ����ʽ����д����ȷ�����ǿ�������뷽ʽ���Լ��йط�Ӧԭ���ǽ���ؼ���ע���������ʽ�����Ӳ��ܲ�ǿ�����ʽ�����ӱ������Ŀ�ѶȲ���


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 6 | 4 | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��H+����c��OH-����c��CH3COO-����c��Na+�� | B�� | c��H+����c��OH-����c��Na+����c��CH3COO-�� | ||
| C�� | c��H+����c��CH3COO-����c��OH-����c��Na+�� | D�� | c��OH-����c��CH3COO-����c��H+����c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Լ���SO32-������HNO3�ữ��BaCl2��Һ | |
| B�� | ����FeCl2��Һʱͨ��������HNO3�ữ����С��ˮ��̶� | |
| C�� | ����ij��Һ���Ƿ�Cl-����HNO3�ữ��AgNO3��Һ | |
| D�� | �����������е���������������������Һ�ܽ⣬Ȼ����������ữ�ĸ��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �÷�Ӧ����ȡ����Ӧ | |
| B�� | FeCl3��Һ���������������������������� | |
| C�� | �����������ķ���ʽΪC10H12O4 | |
| D�� | ����������������NaOH��Һ��ˮ��õ������ƺ������ص����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͬ��Ŀ��ԭ�� | B�� | ��ռ22.4 L | ||
| C�� | ������ͬ��Ŀ�ķ��� | D�� | ������ͬ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m=aVd | B�� | a%=��cM/1 0d��% | C�� | c=1 000mVM | D�� | c=1 000daM |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��ȼ����110.5 kJ/mol | |
| B�� | �ٵķ�Ӧ��Ϊ221 kJ/mol | |
| C�� | ϡ������ϡNaOH��Һ��Ӧ����1mol H2Oʱ��Ӧ�ķ�Ӧ��Ϊ-57.3 kJ/mol | |
| D�� | ϡ������ϡNaOH��Һ��Ӧ����1mol H2Oʱ��Ӧ�ķ�Ӧ��Ϊ-57.3 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4Br�ĵ���ʽ��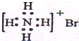 | |
| B�� | S2-�Ľṹʾ��ͼ��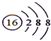 | |
| C�� | ����ķ���ʽ��CH3COOH | |
| D�� | ԭ�Ӻ�����18�����ӵ���ԭ�ӣ�37Cl |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com