
【题目】向2L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:mA(g)+nB(g)pC(g)+qD(g)
已知:A为有色气体;平均反应速率vC= ![]() vA;反应2min时,A的浓度减少了原来的
vA;反应2min时,A的浓度减少了原来的 ![]() ,B的物质的量减少了
,B的物质的量减少了 ![]() mol,有a mol D生成.
mol,有a mol D生成.
回答下列问题:
(1)反应2min内,vA= , vB= .
(2)化学方程式中,m= , n= , p= , q= .
(3)反应平衡时,D为2a mol,则B的平衡转化率为 .
(4)下列选项能说明该反应已经达到平衡状态的有
A.容器内的压强不再变化
B.体系的密度不变
C.容器内气体的质量不变
D.A,B,C,D的速率比恰好为其化学计量数之比
E.混合气体的颜色不再改变
F.混合气体的平均相对分子质量不再改变
G.vB(正)=vC(逆) .
【答案】
(1)![]() mol/(L?min);
mol/(L?min);![]() mol/(L?min)
mol/(L?min)
(2)2;3;1;6
(3)![]()
(4)AEF
【解析】解:(1)反应2min 时,A的浓度减少了 ![]() ,则△c(A)=
,则△c(A)= ![]() ×
× ![]() =
= ![]() amol/L,则v(A)=
amol/L,则v(A)= ![]() =
= ![]() (Lmin);B的物质的量减少了
(Lmin);B的物质的量减少了 ![]() mol,则△c(B)=
mol,则△c(B)= ![]() =
= ![]() mol/L,v(B)=
mol/L,v(B)= ![]() =
= ![]() mol/(Lmin);所以答案是:
mol/(Lmin);所以答案是: ![]() mol/(Lmin);
mol/(Lmin); ![]() mol/(Lmin);(2)根据(1),△c(A)=
mol/(Lmin);(2)根据(1),△c(A)= ![]() amol/L,△c(B)=
amol/L,△c(B)= ![]() mol/L,由题vC=
mol/L,由题vC= ![]() vA;则△c(C)=
vA;则△c(C)= ![]() △c(A)=
△c(A)= ![]()
mol/L,△c(C)= ![]() =
= ![]() mol/L,则m:n:p:q=
mol/L,则m:n:p:q= ![]() a:
a: ![]() a:
a: ![]()
![]() a=2:3:1:6;
a=2:3:1:6;
所以答案是:m=2,n=3,p=1,q=6;(3)反应达到平衡时,D为2amol,由方程式2A(g)+3B(g)=C(g)+6D(g)可知消耗的B为2amol× ![]() =amol,故B的转化率为
=amol,故B的转化率为 ![]() ;
;
所以答案是: ![]() ;(4)A.反应是一个前后系数和变化的反应,当容器内的压强保持不变,证明达到了平衡,故正确,
;(4)A.反应是一个前后系数和变化的反应,当容器内的压强保持不变,证明达到了平衡,故正确,
B.容器内的密度= ![]() ,质量守恒,V不变化,密度始终不变,所以当密度不变,不一定平衡,故错误;
,质量守恒,V不变化,密度始终不变,所以当密度不变,不一定平衡,故错误;
C.容器内气体的质量始终不变,不一定平衡,故错误;
D.A,B,C,D的速率比始终为其化学计量数之比,不一定平衡,故错误;
E.A为有色气体,混合气体的颜色不再改变,证明达到了平衡,故正确;
F.混合气体的平均相对分子质量不再改变,混合气体的平均相对分子质量M= ![]() ,质量守恒,n变化,所以当M不变,证明达到了平衡,故正确;
,质量守恒,n变化,所以当M不变,证明达到了平衡,故正确;
G.化学反应速率之比等于系数之比,vB(正)=vC(逆)不能说明正逆反应速率相等,故错误;
所以答案是:AEF.
【考点精析】关于本题考查的化学平衡的计算,需要了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能得出正确答案.


科目:高中化学 来源: 题型:
【题目】
(1)写出图中序号①~③仪器的名称:①__;②__;③__。
在仪器①~④中,使用前必须检查是否漏水的有__(填仪器序号)。
(2)下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上(密度1.84 g·cm-3,质量分数98%)的部分内容,现用该浓硫酸配制480 mL 1 mol·L﹣1的稀硫酸。可供选用的仪器有:

①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有__、__(写仪器名称)。
b.经计算,配制480 mL 1 mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积约为__mL(保留一位小数点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质分类或归类正确的是( )
①混合物:石炭酸、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚苯乙稀、HD ③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2 ⑤同素异形体:C60、C70、金刚石、石墨
A.①③④
B.③⑤
C.②③④
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,当X,Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( ) 
A.氯碱工业中,X,Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.若Z是稀硫酸,X为铜,Y为铁,则铁不溶解,该方法为外加电流的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种短周期元素,其元素特征信息如下:A的单质是密度最小的物质;B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;C的原子最外层电子数是其内层电子数的三倍;D与B同周期,该周期中D的简单离子半径最小;B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分;F元素最高正价与最低负价的代数和为4.
(1)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式 .
(2)D、E、F的简单离子半径由大到小的顺序是(直接用化学式表示) .
(3)向Fe和D单质组成的混合物中,加入足量F的最高价氧化物对应水化物的稀溶液,固体全部溶解.向所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体,经称量发现该固体的质量和原混合物的质量恰好相等.则原混合物中D单质的质量分数为 .
(4)一定量的石灰乳中通入一定量的E单质,两者恰好完全反应,生成物中有三种含E元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.t2时反应的化学方程式为 . 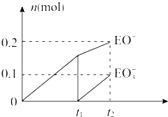
(5)A、B形成的化合物BA在有机合成中用途很广泛.它可以夺取很多化合物中的质子而生成相应的钠的化合物.写出它与乙醇反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液是否饱和的判断正确的是( )
A.溶质未达到溶解平衡的溶液一定是不饱和溶液
B.无固体溶质残留的溶液一定是不饱和溶液
C.加热蒸发一定溶剂后恢复至原温度无溶质析出,原溶液一定是不饱和溶液
D.冷却后无溶质析出,原溶液一定是不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种常见单质,其对应元素的原子质子数依次增大,甲、乙、丙、丁为常见化合物.它们之间有如下转化关系:
回答下列问题:
(1)A的化学式为;乙的化学式为 .
(2)D与甲反应的化学方程式为 .
(3)B与NaOH溶液反应的离子方程式为 , 该反应的氧化剂为 .
(4)B生成D的反应称为反应,实验室中,进行这个反应的操作为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.某芳香烃的分子式为C10H14 , 它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种
B.按系统命名法,有机物 ![]() 的命名为2,2,4,4,5﹣五甲基﹣3,3﹣二乙基己烷
的命名为2,2,4,4,5﹣五甲基﹣3,3﹣二乙基己烷
C.甲烷、甲醛、尿素都不存在同分异构体
D.某有机物含有C,H,O,N四种元素,其球棍模型为 ![]() ,该有机物的结构简式为
,该有机物的结构简式为 ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com