
����Ŀ������˵������ȷ���ǣ� ��
A.ij�������ķ���ʽΪC10H14 �� ������ʹ��ˮ��ɫ������ʹ����KMnO4��Һ��ɫ���ҷ��ӽṹ��ֻ��һ���������������������3��
B.��ϵͳ���������л��� ![]() ������Ϊ2��2��4��4��5�������3��3�����һ�����
������Ϊ2��2��4��4��5�������3��3�����һ�����
C.���顢��ȩ�����ض�������ͬ���칹��
D.ij�л��ﺬ��C��H��O��N����Ԫ�أ������ģ��Ϊ ![]() �����л���Ľṹ��ʽΪ
�����л���Ľṹ��ʽΪ ![]()
���𰸡�C
���������⣺A�������ķ���ʽC10H14����CnH��2n��6����ͨʽ��������ʹ��ˮ��ɫ������ʹKMnO4������Һ��ɫ�����Ժ��б�������������֪���÷��Ӻ��ж������������ֻ�ж϶��������ͬ���칹�弴�ɣ����������̼��ͬ���칹���У� 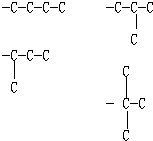 ����ͬϵ�����뱽��������Cԭ���ϱ��뺬��Hԭ�ӣ��ſɱ����Ը������������ʹ���Ը��������Һ��ɫ�����
����ͬϵ�����뱽��������Cԭ���ϱ��뺬��Hԭ�ӣ��ſɱ����Ը������������ʹ���Ը��������Һ��ɫ����� ![]() ���뱽��������Cԭ���ϲ���Hԭ�ӣ�����ʹ���Ը��������Һ��ɫ����˷���������������3�֣���A��ȷ�� B�����л����̼��Ϊ6��̼ԭ�ӣ��Ǽ��飬��Ŵ����ң�����Ϊ2��2��4��4��5�������3��3�����һ����飬��B��ȷ��
���뱽��������Cԭ���ϲ���Hԭ�ӣ�����ʹ���Ը��������Һ��ɫ����˷���������������3�֣���A��ȷ�� B�����л����̼��Ϊ6��̼ԭ�ӣ��Ǽ��飬��Ŵ����ң�����Ϊ2��2��4��4��5�������3��3�����һ����飬��B��ȷ��
C�����ش���ͬ���칹�� ![]() ����C����
����C����
D������ԭ�ӳɼ���ʽ֪�����γ�4�����ۼ���ԭ����Cԭ�ӡ����γ�1�����ۼ���ԭ����Hԭ�ӡ����γ�3�����ۼ�����Nԭ�ӡ����γ�2�����ۼ�����Oԭ�ӣ����Ը��л���ṹ��ʽΪ ![]() ����D��ȷ��
����D��ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ�������ͨ��a mol����A��b mol����B����һ�������·�����Ӧ��mA��g��+nB��g��pC��g��+qD��g��
��֪��AΪ��ɫ���壻ƽ����Ӧ����vC= ![]() vA����Ӧ2minʱ��A��Ũ�ȼ�����ԭ����
vA����Ӧ2minʱ��A��Ũ�ȼ�����ԭ���� ![]() ��B�����ʵ���������
��B�����ʵ��������� ![]() mol����a mol D���ɣ�
mol����a mol D���ɣ�
�ش��������⣺
��1����Ӧ2min�ڣ�vA= �� vB= ��
��2����ѧ����ʽ�У�m= �� n= �� p= �� q= ��
��3����Ӧƽ��ʱ��DΪ2a mol����B��ƽ��ת����Ϊ ��
��4������ѡ����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
A.�����ڵ�ѹǿ���ٱ仯
B.��ϵ���ܶȲ���
C.�������������������
D.A��B��C��D�����ʱ�ǡ��Ϊ�仯ѧ������֮��
E.����������ɫ���ٸı�
F.��������ƽ����Է����������ٸı�
G.vB������=vC���棩 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����ʯ�������ȵ�������( )
A. �Թ� B. ������ C. ���� D. Բ����ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ�ӽṹģ�͵��ݱ�ͼ��ͼ�� 
���У���1��Ϊ������ʵ����ʽԭ��ģ�ͣ���2��Ϊ¬ɪ��������תʽԭ��ģ�ͣ���3��Ϊ��ķ�����Ѹ����ʽԭ��ģ�ͣ���4��Ϊ����������ѧԭ��ģ�ͣ���5��Ϊ�������ʽԭ��ģ�ͣ����з�����ʷ�ݱ�˳���һ�������ǣ� ��
A.��1����3����2����5����4��
B.��1����2����3����4����5��
C.��1����5����3����2����4��
D.��1����3����5����4����2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ��Ȼ�����һ�����;�ˮ��������������Ũ�ȣ���AlT��ʾ���������ࣺ��ҪΪAl3+�ĵ�����̬����Ũ�ȣ���Ala��ʾ������ҪΪ[AlO4Al12��OH��24��H2O��12]7+���еȾۺ���̬����Ũ�ȣ���Alb��ʾ����Al��OH��3������̬����Ũ�ȣ���A1c��ʾ����
��1��һ�������£���1.0mol/LAlCl3��Һ�м���0.6mol/L��NaOH��Һ�����Ƶ�Alb����ԼΪ86%�ľۺ��Ȼ�����Һ��д������[AlO4Al12��OH��24��H2O��12]7+�����ӷ���ʽ�� ��
��2����Ĥ�����MD��Ũ���������ۺ��Ȼ�����Һ����Ũ����ʵ������в�ͬŨ�Ⱦۺ��Ȼ���������̬�ֲ����ٷ����������
AlT/��molL��1�� | Ala/% | Alb/% | A1c/% |
0.208 | 1.4 | 86.6 | 12.0 |
0.489 | 2.3 | 86.2 | 11.5 |
0.884 | 2.3 | 88.1 | 9.6 |
1.613 | 3.1 | 87.0 | 9.9 |
2.520 | 4.5 | 88.2 | 7.3 |
����һ���¶��£�AlTԽ��pH���Խ����ԽС�����䡱����
���罫AlT=2.520molL��1�ľۺ��Ȼ�����Һ��ˮϡ�ͣ���ϡ��������Ҫ������Ӧ�����ӷ���ʽ�� ��
��Ĥ������Һ�¶ȶ����ۺ���̬�ٷ�����������Ũ�ȵ�Ӱ����ͼ1����T��80��ʱ��AlT�����½���ԭ���� �� 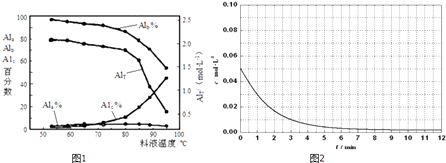
��3�����̼�Ȼ�ԭһ��������ʵ�����������Ʊ�����������ط�Ӧ���Ȼ�ѧ����ʽ���£���Al2O3��s��+AlCl3��g��+3C��s��=3AlCl��g��+3CO��g����H1=a kJmol��1
��3AlCl��g��=2Al��l��+AlCl3��g����H2=b kJmol��1
��ӦAl2O3��s��+3C��s��=2Al��l��+3CO��g����H=kJmol��1���ú�a��b�Ĵ���ʽ��ʾ������Ӧ�ٳ�ѹ����1900��ĸ����²��ܽ��У�˵����H0���������=����������
��4�������е���Ԫ�ؿ���ͨ������Ԫ��ת����Al3+ �� Ȼ����ˮ��Һ�������Լ���NH4��3C19H11O3��COO��3����Ʒ��Ϊ���������ã��ⶨ������������Һ�У�Al3+���������Լ���Ӧ������õ���ɫ�����ʣ����Ÿ÷�Ӧ�Ľ��У���Һ����ɫ���ϱ仯��������Һ��ɫ�뷴Ӧ��������Ũ�ȵĹ�ϵ������ɫ������������ȷ���û�ѧ��Ӧ�����ʣ����ڱ�ɫ������������ ��
A.pH��
B.Ԫ�ط�����
C.�ֹ��ȼ�
D.ԭ�����չ�����
��5����֪Al3++4X2[�� ![]() X2��1.5+]��X��ʾ��ɫ����
X2��1.5+]��X��ʾ��ɫ���� ![]() X21.5+��ʾ��ɫ���ʣ�ͨ����ɫ�����õ�25��ʱAl3+Ũ����ʱ��ı仯��ϵ��ͼ2��ʾ������ͬһͼ�л��
X21.5+��ʾ��ɫ���ʣ�ͨ����ɫ�����õ�25��ʱAl3+Ũ����ʱ��ı仯��ϵ��ͼ2��ʾ������ͬһͼ�л�� ![]() X21.5+Ũ����ʱ��ı仯���� ��
X21.5+Ũ����ʱ��ı仯���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ba��AlO2��2������ˮ����ͼ��ʾ������Al2��SO4��3��Һ����μ���Ba��OH��2��Һʱ�����ɳ��������ʵ���y�����Ba��OH��2�����ʵ���x�Ĺ�ϵ�������й�����������ǣ� �� 
A.a��bʱ���������ʵ�����Al��OH��3��BaSO4��
B.b��cʱ��Һ�����ӵ����ʵ�����AlO2����Ba2+��
C.a��dʱ���������ʵ�����Al��OH��3һ��С��BaSO4
D.d��eʱ��Һ�����ӵ����ʵ�����Ba2+���ܵ���AlO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ѧ��������A��B��C��D��X��Y����������ͼת����ϵ���������ʺ�������ȥ��
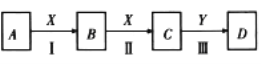
��1����AΪNaOH��Һ��XΪCO2��D�dz�������Y��Ϊ________������ţ���
A��SO3 B��Ba(OH)2 C��H2SO4 D��CaO
��2����AΪ������FeS2����D��H2SO4����Ӧ��Ļ�ѧ����ʽΪ_________________________��
��3����AΪ����ˮ�ʼ��Ե����壬��A��D��Ӧ���ɵ�һ�ֻ��ʵĻ�ѧʽΪ_____________����Ӧ��Ļ�ѧ����ʽΪ__________________��D��Ũ��Һ��̿��Ӧ�Ļ�ѧ����ʽ__________________________��
��4����A��X��Ϊ���ʣ���Ӧ��������ǰ�ɫ�������ڿ�����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ����ӦII�����ӷ���ʽΪ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ܱ������з������·�Ӧ��X��g��+3Y��g��2Z��g������H��0����ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵij�ʼ������������˵������ȷ���ǣ� �� 
A.t5ʱ������ѹǿ
B.t3ʱ�������¶�
C.t2ʱ�����˴���
D.t4��t5ʱ����ת����һ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com