
【题目】如图所示,已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,B和D都是日常生活食品中常见的有机物,F是一种高聚物,生活中用于制造食物保鲜膜。
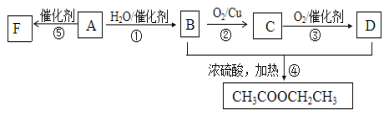
(1)请写出A的分子式:_____________。
(2)请写出下列反应的类型:④_____________,⑤_____________。
(3)请写出下列反应的化学方程式:
①_____________;⑤_____________;
(4)某实验小组用下列装置模拟上述反应②的转化过程。
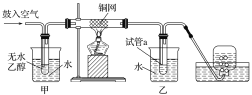
实验过程中铜网出现黑色和红色交替的现象。
①红色变成黑色的反应是2Cu+O2![]() 2CuO;
2CuO;
②黑色变为红色的化学方程式为____________________________________________。甲和乙两个水浴作用不相同,甲的作用是________(填“加热”或“冷却”);反应进行一段时间后,试管a中能收集到多种物质,它们是______(任写两种即可)
【答案】C2H4 取代反应或酯化反应 加聚反应 CH2=CH2+H2O![]() CH3CH2OH nCH2=CH2
CH3CH2OH nCH2=CH2![]() CH3CH2OH+CuO
CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 加热 乙醇、乙醛或水任写两个
CH3CHO+Cu+H2O 加热 乙醇、乙醛或水任写两个
【解析】
已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,推知A为乙烯;乙烯与水加成生成B,则B为乙醇;乙醇发生催化氧化反应生成C,则C为乙醛;乙醛氧化生成D,D是日常生活食品中常见的有机物,则D为乙酸;F是一种高聚物,生活中用于制造食物保鲜膜,由乙烯加聚生成,则F为聚乙烯。
(1)综上分析,A为乙烯,其分子式为C2H4。
(2)乙酸与乙醇发生酯化反应生成乙酸乙酯,则④的反应类型为取代反应或酯化反应;乙烯通过加聚反应生成聚乙烯,⑤的反应类型为加聚反应。
(3)①为乙烯与水发生加成反应生成乙醇,方程式为CH2=CH2+H2O![]() CH3CH2OH;⑤为乙烯发生加聚反应生成聚乙烯,方程式为nCH2=CH2
CH3CH2OH;⑤为乙烯发生加聚反应生成聚乙烯,方程式为nCH2=CH2![]() 。
。
(4)铜网加热生成黑色的氧化铜,通入乙醇后,乙醇与氧化铜反应生成乙醛、铜和水,反应方程式为CH3CH2OH+CuO![]() CH3CHO+Cu+H2O;甲水浴的作用是加热无水乙醇使乙醇挥发进入玻璃管中;反应一段时间后,试管a中可以收集到剩余的乙醇以及反应生成的乙醛和水。
CH3CHO+Cu+H2O;甲水浴的作用是加热无水乙醇使乙醇挥发进入玻璃管中;反应一段时间后,试管a中可以收集到剩余的乙醇以及反应生成的乙醛和水。


科目:高中化学 来源: 题型:
【题目】NA 是阿伏加德罗常数的值,下列说法正确的是
A. 1mol葡萄糖分子含有的羟基数目为6NA
B. 5.8gC4H10中含有共价键总数为1.3NA
C. 5.8g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.04NA
D. 4.6g乙醇完全氧化成乙醛,转移电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩,如图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是
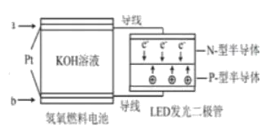
A.通入O2的电极发生反应:O2+4e-=2O2-
B.a处通入氧气,b处通氢气
C.电池放电后,OH-的物质的量浓度减小
D.电路中的电子从负极经外电路到正极,再经过KOH溶液回到负极,形成闭合回路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+等)为原料制备氧化锌的流程如下:
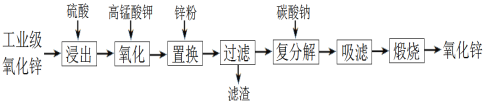
其中“氧化”加入KMnO4是为了除去浸出液中的Fe2+和Mn2+。下列有关说法错误的是
A. 浸出时通过粉碎氧化锌提高了浸出率
B. “氧化”生成的固体是MnO2和Fe(OH)3
C. “置换”加入锌粉是为了除去溶液中的Cu2+、Ni2+等
D. “煅烧”操作用到的仪器:玻璃棒、蒸发皿、泥三角
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为某有机物与各种试剂的反应现象,则这种有机物可能是( )
试剂 | 钠 | 溴水 |
|
现象 | 放出气体 | 褪色 | 放出气体 |
A.CH2=CH-CH2-OHB.![]()
C.CH2=CH-COOHD.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是( )
A. 0.1 mol·L-1 NaHCO3溶液:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)-c(CO32-)
B. 0.1 mol·L-1 NaHC2O4溶液呈酸性:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
C. 20 mL 0.10 mol·L-1 CH3COONa溶液与10 mL 0.10 mol·L-1 HCl溶液混合得到的酸性溶液:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
D. 向0.1mol·L-1 NH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:________________。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
________CuSO4+_____PH3+_____H2O=_____Cu3P↓+_____H3PO4+_____H2SO4
(3)工业制备PH3的流程如图所示。

①次磷酸属于________元酸。
②白磷和烧碱溶液反应的化学方程式为:____________________________________。
③若起始时有1 mol P4参加反应,则整个工业流程中共生成________mol PH3。(不考虑产物的损失)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变化如图。
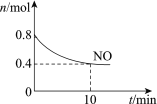
(1)将NO、CO转化为2种无毒气体的化学方程式是______。
(2)反应开始至10 min,v(NO)=______mol/(Lmin)。
(3)下列说法正确的是______。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com