
【题目】乙醚是有机合成中常用的溶剂.某实验小组在实验室利用乙醇脱水制备乙醚, 装置示意图( 夹持和加热装置已略去)、有关数据和实验步骤;

物质 | 相对分子质量 | 密度(g/mL) | 沸点(℃) | 在水中的溶解性 |
乙醇 | 46 | 0.816 | 78 | 互溶 |
乙醚 | 74 | 0.713 | 34.6 | 不容 |
已知:①相同条件下,乙醚在饱和食盐水中比在水中更难溶。
②氯化钙可与乙醇形成络合物 CaCl26C2H5OH.
请回答下列问题:
(1)由乙醇制备乙醚的总反应为2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O . 此反应分两步进行,第一步反应的化学方程式 : CH3CH2OH +H2SO4
CH3CH2OCH2CH3 + H2O . 此反应分两步进行,第一步反应的化学方程式 : CH3CH2OH +H2SO4 ![]() CH3CH2OSO2OH + H2O ,则第二步反应的化学方程式为 _____________________________。
CH3CH2OSO2OH + H2O ,则第二步反应的化学方程式为 _____________________________。
(2)仪器 D 中盛有冰水混合物 ,其作用为_____________________________。
(3)操作1 的名称为 ________,操作2 的名称为 ___________。
(4)若省略步骤 II会导致的后果是_________________________________。
(5)若实验过程中加入18mL 乙醇,最终得到 8.7g 乙醚.则乙醚的产率为_____ (计算结果精确到0.1%).
【答案】![]() 使乙醚冷凝为液体以便收集 分液 过滤 用饱和氯化钙溶液洗涤乙醚粗品时,析出氢氧化钙沉淀 73.6%
使乙醚冷凝为液体以便收集 分液 过滤 用饱和氯化钙溶液洗涤乙醚粗品时,析出氢氧化钙沉淀 73.6%
【解析】
乙醇在浓硫酸作用下,![]() 制得乙醚,反应过程中,防止滴入的乙醇受热被蒸发,提高产物的产率,减少杂质,仪器B的末端应浸入反应液中,馏出液中的乙醚混有乙醇,加入NaOH溶解乙醇,乙醚不溶,分液,向有机层加入饱和食盐水,进一步提纯乙醚,再加入饱和氯化钙溶液乙醇形成络合物CaCl26C2H5OH,向粗产品加入无水氯化钙吸水,过滤,蒸馏得到产品,
制得乙醚,反应过程中,防止滴入的乙醇受热被蒸发,提高产物的产率,减少杂质,仪器B的末端应浸入反应液中,馏出液中的乙醚混有乙醇,加入NaOH溶解乙醇,乙醚不溶,分液,向有机层加入饱和食盐水,进一步提纯乙醚,再加入饱和氯化钙溶液乙醇形成络合物CaCl26C2H5OH,向粗产品加入无水氯化钙吸水,过滤,蒸馏得到产品,
(1)由总反应-第一步反应可得;
(2)冰水混合物冷凝乙醚;
(3)根据分离混合物的状态分析;
(4)若省略步骤Ⅱ,步骤I中少量的NaOH与氯化钙生成沉淀;
(5)由乙醇计算理论生成的乙醚的质量,再计算产率可得。
(1)已知总反应:①![]() ,第一步反应的化学方程式为②
,第一步反应的化学方程式为②![]() ,由①-②可得第二步反应的为:
,由①-②可得第二步反应的为:![]() ,
,
故答案为:![]() ;
;
(2)仪器D中盛有冰水混合物使乙醚冷凝为液体以便收集;
故答案为:使乙醚冷凝为液体以便收集;
(3)通过操作1将溶液与乙醚分离,乙醚与溶液不溶,故为分液;操作2分离吸水后的氯化钙水合物固体与乙醚,故为过滤;
故答案我为:分液;过滤;
(4)若省略步骤Ⅱ,乙醚粗品混有少量步骤I的NaOH,用饱和氯化钙溶液洗涤乙醚粗品时,析出氢氧化钙沉淀;
故答案为:用饱和氯化钙溶液洗涤乙醚粗品时,析出氢氧化钙沉淀;
(7)若实验过程中共加入18mL乙醇,则m(乙醇)=![]() ,设理论生成的乙醚质量为m,根据:
,设理论生成的乙醚质量为m,根据:
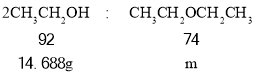
解得![]() ,则乙醚的产率为
,则乙醚的产率为![]() ;
;
故答案为:73.6%。


科目:高中化学 来源: 题型:
【题目】下图是半导体光电化学电池光解水制氢的反应原理示意图。在光照下,电子由价带跃迁到导带后,然后流向对电极。下列说法正确的是

A.半导体电极的电极反应式4OH -4e-=2H2O+O2↑
B.电解一段时间后,溶液的pH减少
C.电解质溶液中的阴离子移向半导体电极
D.整个过程中实现了太阳能—化学能—电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述错误的是( )
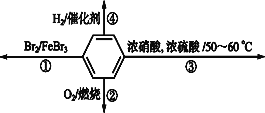
A.反应①为取代反应,有机产物与水混合浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种芳香化合物
D.反应④中1 mol苯最多与3 mol H2在催化剂作用下发生加成反应,说明苯具有类似烯烃的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用现代科技从苦艾精油中分离出多种化合物,其中四种的结构如下:

下列说法不正确的是( )
A.②③分子中所有碳原子不可能处于同一平面内
B.②④互为同分异构体
C.④的一氯代物有6种
D.①②③均能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.在CH3COOH分子中的所有碳原子和氧原子都在同一平面
B.在 中单体为
中单体为![]() 和NC-CHO
和NC-CHO
C.1mol 与NaOH溶液完全反应,消耗NaOH5mol
与NaOH溶液完全反应,消耗NaOH5mol
D.![]() 与Br21︰1加成可有4种加成产物
与Br21︰1加成可有4种加成产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A. 次氯酸的电离方程式:HClO===H++ClO-
B. 铝溶于烧碱溶液的离子方程式:Al+2OH-==AlO2-+H2↑
C. 电解精炼铜的阴极反应式:Cu-2e-==Cu2+
D. 已知中和热为57.3 kJ·mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH(aq)==Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇。一定条件下密闭容器中发生反应,测得数据曲线如下图所示(反应混合物均呈气态)。下列说法错误的是
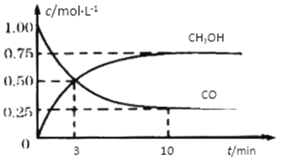
A.反应的化学方程式:CO+2H2![]() CH3OH
CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,(CO) = 0.075 mol/L·min
D.增大压强,平衡正向移动,K不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
(1)物质的量浓度均为0.1molL﹣1的四种溶液:pH由小到大排列的顺序是_______(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_____(填字母)_______
A. c(H+) B.![]() C. c(H+)c(OH﹣) D.
C. c(H+)c(OH﹣) D. ![]() E.
E. ![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________________
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(5)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____________________________________
(6)标准状况下,将1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: c(OH﹣)=2c(H2CO3)+_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】痛灭定钠是一种吡咯乙酸类的非甾体抗炎药,其合成路线如下:
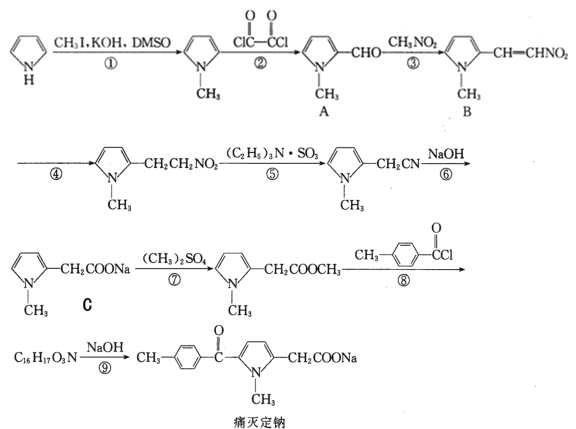
回答下列问题:
(1)化合物 C 中含氧官能团的名称是_____。
(2)化学反应①和④的反应类型分别为_____和_____。
(3)下列关于痛灭定钠的说法正确的是_____。
a.1mol 痛灭定钠与氢气加成最多消耗 7molH2 b.核磁共振氢谱分析能够显示 6 个峰 c.不能够发生还原反应 d.与溴充分加成后官能团种类数不变 e.共直线的碳原子最多有 4 个
(4)反应⑨的化学方程式为_____。
(5)芳香族化合物 X 的相对分子质量比 A 大 14,遇 FeCl3 溶液显紫色的结构共有_____种(不考虑立体异构),核磁共振氢谱分析显示有 5 个峰的 X 的结构简式有_____。
(6) 根据该试题提供的相关信息,写出由化合物![]() 及必要的试剂制备有机化合物
及必要的试剂制备有机化合物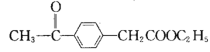 的合成路线图。________________
的合成路线图。________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com