
【题目】运用现代科技从苦艾精油中分离出多种化合物,其中四种的结构如下:

下列说法不正确的是( )
A.②③分子中所有碳原子不可能处于同一平面内
B.②④互为同分异构体
C.④的一氯代物有6种
D.①②③均能使酸性高锰酸钾溶液褪色
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
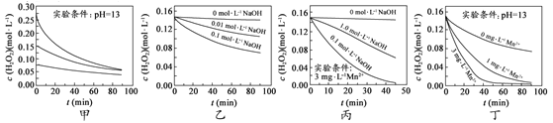
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒“现代工业的味精”,是发展现代工业、现代国防和现代科学技术不可缺少的重要材料,其氧化物二氧化钒(VO2)是一种新型热敏材料,五氧化二钒(V2O5)是接触法生成硫酸的催化剂.下列某化学小组从废钒催化剂(V2O5、V2O4、K2SO4、SiO2、Fe2O3、Al2O3等)中回收V2O5并且利用回收的V2O5制备VO2的氧钒(Ⅳ) 碱式碳酸铵晶体
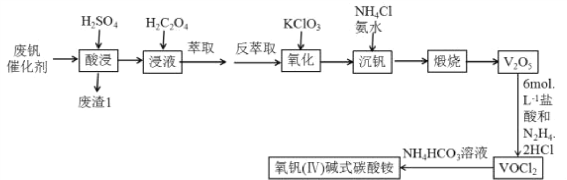
已知:①“酸浸”时V2O5转化为VO2+,V2O4转成VO2+
②有机萃取剂萃取VO2+的能力比萃取VO2+要强。
③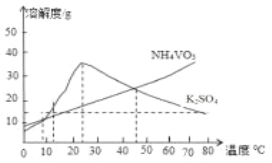
回答下列问题:
(1)写出“废渣1”的主要成分的用途________(填两条)。
(2)“萃取”之前加入H2C2O4的主要目的_____________________。
(3)“氧化”过程中发生的离子方程式___________________________。
(4)该工艺中加入氯化铵“沉钒”是回收钒的关键之一,加入氯化铵、氨水之后的操作是____________,该流程用到了过滤操作,过滤和萃取分液都需用到的一种玻璃仪器是__________。
(5)工艺中生成VOC12的同时生成一种无色无污染的气体,该反应中氧化产物与还原产物的物质的量之比为___________;也可只用浓盐酸与V2O5来制备VOC12 溶液,该方法的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯可用下图所示装置。请回答下列问题:

(1)关闭G夹,打开B夹,从装有少量苯的三颈烧瓶的A口加少量溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生的主要反应的化学方程式为___________________。
(2)试管C中苯的作用是_________________。试管D中出现的现象是______________。试管E中出现的现象是_______________。
(3)待三颈烧瓶中的反应进行到仍有气泡冒出时打开G夹,关闭B夹,可以看到的现象是__________________。
(4)三颈烧瓶中的溴苯经过下列步骤分离提纯:
①向三颈烧瓶中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是除去多余的溴;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是干燥产品。
④经过上述分离操作后,要进一步提纯,下列操作中必须的是_________(填入正确选项前的字母)。
A 重结晶 B 过滤 C 蒸馏 D 萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醚是有机合成中常用的溶剂.某实验小组在实验室利用乙醇脱水制备乙醚, 装置示意图( 夹持和加热装置已略去)、有关数据和实验步骤;

物质 | 相对分子质量 | 密度(g/mL) | 沸点(℃) | 在水中的溶解性 |
乙醇 | 46 | 0.816 | 78 | 互溶 |
乙醚 | 74 | 0.713 | 34.6 | 不容 |
已知:①相同条件下,乙醚在饱和食盐水中比在水中更难溶。
②氯化钙可与乙醇形成络合物 CaCl26C2H5OH.
请回答下列问题:
(1)由乙醇制备乙醚的总反应为2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O . 此反应分两步进行,第一步反应的化学方程式 : CH3CH2OH +H2SO4
CH3CH2OCH2CH3 + H2O . 此反应分两步进行,第一步反应的化学方程式 : CH3CH2OH +H2SO4 ![]() CH3CH2OSO2OH + H2O ,则第二步反应的化学方程式为 _____________________________。
CH3CH2OSO2OH + H2O ,则第二步反应的化学方程式为 _____________________________。
(2)仪器 D 中盛有冰水混合物 ,其作用为_____________________________。
(3)操作1 的名称为 ________,操作2 的名称为 ___________。
(4)若省略步骤 II会导致的后果是_________________________________。
(5)若实验过程中加入18mL 乙醇,最终得到 8.7g 乙醚.则乙醚的产率为_____ (计算结果精确到0.1%).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组经资料检索后发现,药物贝诺酯能可由乙酸水杨酸和对乙酰氨基酚在一定条件下反应制得,其反应的化学方程式为
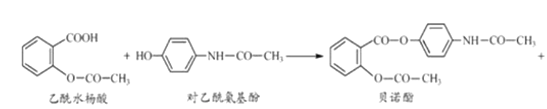 H2O
H2O
下列有关叙述错误的是( )
A.贝诺酯、乙酰水杨酸分子中都有酯基
B.对乙酰氨基酚的分子式为C8H9O2N
C.乙酰水杨酸能与NaHCO3溶液反应,并放出二氧化碳气体
D.贝诺酯与足量 NaOH 溶液共热,最终产物之一是乙酰水杨酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26届会议新修订了阿伏加德罗常数的值(NA=6.02214076×1023 mol-1),并于2019年5月20日正式生效,下列叙述正确的是
A.32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
B.含16 g氧原子的二氧化硅晶体中含有的σ键数目为NA
C.1.2 g金刚石与石墨的混合物中含有碳碳单键的数目为0.4NA
D.在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com