
【题目】国际计量大会第26届会议新修订了阿伏加德罗常数的值(NA=6.02214076×1023 mol-1),并于2019年5月20日正式生效,下列叙述正确的是
A.32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
B.含16 g氧原子的二氧化硅晶体中含有的σ键数目为NA
C.1.2 g金刚石与石墨的混合物中含有碳碳单键的数目为0.4NA
D.在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA
【答案】A
【解析】
A.在32 g S8单质含有的S—S键个数为:[32/(32×8)]×8×NA=NA,A正确;
B.在二氧化硅晶体中,每个氧原子与邻近的2个硅原子形成共价键,16g氧原子的物质的量为1mol,所以含有的σ键数目为2NA,B错误;
C.在金刚石中,每个碳原子与邻近的4个碳原子形成共价键,形成一个共价键需要2个碳原子,所以平均每个碳原子可形成2个共价键,故1.2g金刚石含碳原子0.1mol,所以含有的共价键数目为0.2NA;石墨晶体中,每个碳原子与邻近的3个碳原子形成共价键,形成一个共价键需要2个碳原子,所以平均每个碳原子可形成1.5个共价键,1.2g石墨含碳原子0.1mol,所以含有的共价键数目为0.15NA。所以1.2 g金刚石与石墨的混合物中含有碳碳单键的数目不是0.4NA,C错误;
D.N2+3H2![]() 2NH3,该反应为可逆反应,故在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数小于NA,D错误;
2NH3,该反应为可逆反应,故在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数小于NA,D错误;
答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】运用现代科技从苦艾精油中分离出多种化合物,其中四种的结构如下:

下列说法不正确的是( )
A.②③分子中所有碳原子不可能处于同一平面内
B.②④互为同分异构体
C.④的一氯代物有6种
D.①②③均能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
(1)物质的量浓度均为0.1molL﹣1的四种溶液:pH由小到大排列的顺序是_______(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_____(填字母)_______
A. c(H+) B.![]() C. c(H+)c(OH﹣) D.
C. c(H+)c(OH﹣) D. ![]() E.
E. ![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________________
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(5)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____________________________________
(6)标准状况下,将1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: c(OH﹣)=2c(H2CO3)+_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素可形成很多重要的化合物,其中叠氮化钠(NaN3)被广泛应用于汽车安全气囊。叠氮化钠的制取方法是:①金属钠与液态氨反应得NaNH2②NaNH2与N2O按物质的量2:1反应可生成NaN3、NaOH和一种气体。
(1)请写出反应②的化学方程式为:____________。
(2)与N3-互为等电子体的分子有:______(写一种)由此可推知N3-的空间构型是:_________; 比较NH2-和NH3的键角∠HNH的大小:NH2- ____ NH3(填“>”或“<”或“=”),请用价层电子对互斥规律解释_______。
(3)叠氮化钠(NaN3)分解可得纯N2,有关说法正确的是:________(选填代号)
A.氮气常温下很稳定,是因为氮元素的电负性大
B.NaN3与KN3结构类似,前者晶格能较小
C.第一电离能(I1):N>P>S
D.热稳定性NH3强于PH3和H2S是因为NH3分子间有氢键
(4)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+ Fe2O3 = 3Na2O + 2Fe+ 9N2 ;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如下图所示):
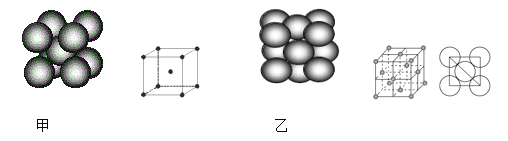
晶胞甲中铁原子的配位数为:_______,晶胞乙中铁原子的堆积方式为:________。晶胞乙中铁原子半径为a cm,NA表示阿伏加德罗常数,摩尔质量为M g/mol。则该晶体的密度可表示为:___________ g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应方向的描述中正确的是
A.某吸热反应能自发进行,因此该反应是熵增反应
B.知道了某过程有自发性之后,可预测反应过程发生的快慢
C.CaCO3(s)![]() CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关
CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关
D.冰融化为水的过程中:△H<0,△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下列要求作答。
(1)第二周期中,第一电离能介于B和N之间的元素共有_________种。
(2)第四周期中,原子核外电子排布有两个未成对电子的元素有_________种。
(3)硅烷(Si,H2H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________________________。
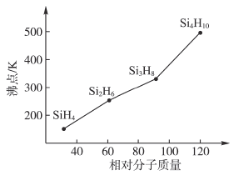
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】痛灭定钠是一种吡咯乙酸类的非甾体抗炎药,其合成路线如下:
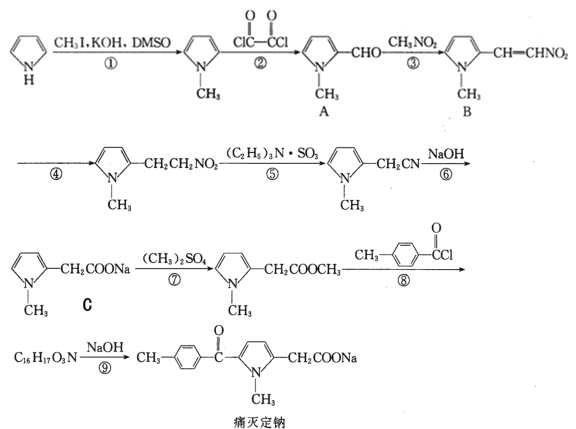
回答下列问题:
(1)化合物 C 中含氧官能团的名称是_____。
(2)化学反应①和④的反应类型分别为_____和_____。
(3)下列关于痛灭定钠的说法正确的是_____。
a.1mol 痛灭定钠与氢气加成最多消耗 7molH2 b.核磁共振氢谱分析能够显示 6 个峰 c.不能够发生还原反应 d.与溴充分加成后官能团种类数不变 e.共直线的碳原子最多有 4 个
(4)反应⑨的化学方程式为_____。
(5)芳香族化合物 X 的相对分子质量比 A 大 14,遇 FeCl3 溶液显紫色的结构共有_____种(不考虑立体异构),核磁共振氢谱分析显示有 5 个峰的 X 的结构简式有_____。
(6) 根据该试题提供的相关信息,写出由化合物![]() 及必要的试剂制备有机化合物
及必要的试剂制备有机化合物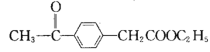 的合成路线图。________________
的合成路线图。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物![]() 题目中所有物质中均无支链
题目中所有物质中均无支链![]() 在一定条件下具有如下所示的转化关系。
在一定条件下具有如下所示的转化关系。

回答:
(1)![]() 的结构简式为______,C和D的相互关系为______。
的结构简式为______,C和D的相互关系为______。
(2)指出下列转化的有机反应类型:![]() 属______类型;
属______类型;![]() 属______类型。
属______类型。
(3)生成B的反应方程式为:______。
(4)生成C的反应方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂(Li)-空气电池的工作原理如图所示。下列说法不正确的是( )
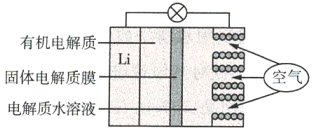
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O2+4e-=2O2-
D.电池总反应:4Li+O2+2H2O=4LiOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com