
����Ŀ��ijѧϰС��Ժ�+4����Ԫ�ص��������ʽ���̽����ʵ�鷽���Ͳ������£�
���� | ���� | ���� | |||
| ����һ | �Թ� | 0.3g����Na2SO3(s) | 0.3g����Na2SO3(s)+1.17gNaCl(s) | |
�ι� | 10mL2molL-1 ���� | 10mL2molL-1 HNO3 | 10mL2molL-1HNO3 | ||
���� | ������ɫ���ݲ���������������ɫ�仯 | ||||
����� | �ι� | ��������Һ�У��ֱ�μ�4��0.1molL-1BaCl2��Һ | |||
���� | 4min����Һ����� | 2.5h����Һ����� | 20min����Һ����� | ||
��֪Na+�Ĵ��ڶԸ�ʵ����Ӱ�죬���������ʵ�������������ȷ���ǣ� ��
A.����һ�в�������ķ�ӦΪSO2
B.ʵ�颡�е�������ΪBaSO3
C.��ʵ���֪����+4����Ԫ�ص����ʿɱ�O2����
D.ͨ��ʵ�颡�͢������͢��ĶԱȣ���֪��NO3-��Cl-�Ĵ��ڶ���Һ��+4����Ԫ�ص�����������Ӱ��
���𰸡�B
��������
A������һȡ![]() ����
����![]() ���壬�����м���
���壬�����м���![]() ���ᣬ������ɫ����Ϊ
���ᣬ������ɫ����Ϊ![]() ���壬��Ӧ�ķ���ʽΪ
���壬��Ӧ�ķ���ʽΪ![]() ����A��ȷ��
����A��ȷ��
B��ʵ��![]() �������������
�������������![]() ����Һ����ǣ�˵��
����Һ����ǣ�˵��![]() ��������
��������![]() ��������
��������![]() �����
�����![]() ����
����![]() ����B����
����B����
C�������Ϸ���˵��������![]() Ҳ����������
Ҳ����������![]() ����Ԫ�صĻ������C��ȷ��
����Ԫ�صĻ������C��ȷ��
D��ʵ��![]() ��
��![]() �Աȣ�
�Աȣ�![]() ������ͬ��
������ͬ��![]() ������ͬ���Աȿɵ�
������ͬ���Աȿɵ�![]() ����
����![]() ����Ԫ�ص�������ʵ��
����Ԫ�ص�������ʵ��![]() ��
��![]() �Աȣ���ͬ����
�Աȣ���ͬ����![]() ���Աȿɵ�
���Աȿɵ�![]() ����
����![]() ����Ԫ�ص���������D��ȷ��
����Ԫ�ص���������D��ȷ��
�ʴ�ΪB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��SO2ͨ��ʢ��H2S����Һ�г��ֵ���ɫ���ǣ��÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
(2)����������ͨ���Ȼ�����Һ�����������Ƶ���ˮ�а�ɫ�������ɣ�д����Ӧ�����ӷ���ʽ��_________________________��
(3)���������[(NH4)2Fe(SO4)2]��������������500��ʱ����ȫ�ֽ⣬�ֽ�����к�����������������������������ˮ��������Ӧ�Ļ�ѧ����ʽΪ__________________��
(4)���Ȼ�ͭ��Һ��ͨ��SO2����������CuCl��ɫ���������ӷ���ʽΪ___________________��
(5)������ͨ��Cu��Ũ���ᷴӦ��ʣ�����Һ�У�ͭƬ�����ܽ⣬��Ӧ�Ļ�ѧ����ʽΪ________________________________________��
(6)������(PH3)ͨ��ʢ��Fe2(SO4)3��Һ���Թ��У���ɫ���ػ�ɫ��ɵ���ɫ��ͬʱ���а�ɫ��״�������ɣ���Ӧ�����ӷ���ʽ��____________________��
��PH3�о綾����CuSO4��Һ���գ�����������Cu3P��H3PO4��д����Ӧ�Ļ�ѧ����ʽ��_____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҩ�����ٴ����������Ӧ�ã�����ȥ�ȡ���ʹ����Ч�������Ǹ�ҩ��ĺϳ�·�ߣ�
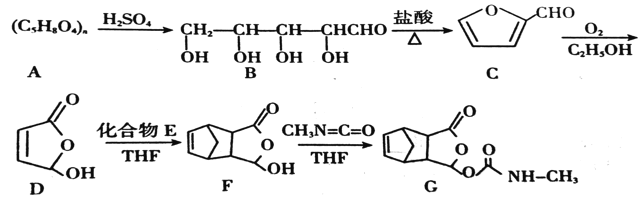
��֪��CH2=CH��CH2=CH2+CH2=CH2![]()
(1)������C�ķ���ʽΪ__��B�к��������ŵ�������__��
(2)E��һ�ȴ�����__�֣�F��G�ķ�Ӧ����Ϊ__��
(3)д��D��F�Ļ�ѧ����ʽ__��
(4)F��ͬ���칹���ж��֣���������������ͬ���칹����__�֣�д������һ�ֵĽṹ��ʽ__��
�����ڶ�ȡ�����㻯��������ϵ�һ�ȴ���������
������FeCl3��Һ������ɫ��Ӧ
������̼�����Ʒ�Ӧ��������
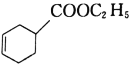
(5)д����2���嶡�顢��ϩ����Ҵ�Ϊԭ�Ϻϳ���ͼ���ʵĺϳ�·�ߣ�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ʱ���������CO��NOx�ȶ�����Ⱦ���壬�漰�����·�Ӧ��
��N2(g)+O2(g)![]() 2NO(g)
2NO(g)
��2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g)
��NO2(g)+CO(g)![]() CO2(g)+NO(g)
CO2(g)+NO(g)
Ū��������Ӧ����ػ������Ա����������������شش��������⣺
��ѧ���о�����һ�ָ�Ч���������Խ�CO��NO2����ת��Ϊ����Ⱦ���壬��Ӧ����ʽΪ��2NO2(g)+4CO(g)=4CO2(g)+N2(g) ��H<0
ij�¶��£���10L�ܱ������зֱ����0.1molNO2��0.2molCO������������Ӧ�����ŷ�Ӧ�Ľ��У������ڵ�ѹǿ�仯�����ʾ��
ʱ��/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
ѹǿ/kPa | 75 | 73.4 | 71.95 | 70.7 | 69.7 | 68.75 | 68.75 |
�ش��������⣺
�����¶Ƚ��ͣ��ٴ�ƽ�����ԭƽ�������ϵѹǿ(p��)��α仯��___(����������������С������������)��ԭ����____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽�����ᣨH2C2O4�����ʣ���������ʵ�顣����֪�������£�0.1 mol��L1 H2C2O4��pH=1.3��
ʵ�� | װ�� | �Լ�a | ���� |
�� |
| Ca(OH)2��Һ������̪�� | ��Һ��ɫ��������ɫ���� |
�� | ����NaHCO3��Һ | �������� | |
�� | ����KMnO4��Һ | ��ɫ��Һ��ɫ | |
�� | C2H5OH��Ũ���� | ���Ⱥ��������ζ���� |
������ʵ�����ò�����������Ӧ�ķ���ʽ����ȷ����
A. H2C2O4�����ԣ�Ca(OH)2+ H2C2O4![]() CaC2O4��+2H2O
CaC2O4��+2H2O
B. ���ԣ�H2C2O4> H2CO3��NaHCO3+ H2C2O4![]() NaHC2O4+CO2��+H2O
NaHC2O4+CO2��+H2O
C. H2C2O4���л�ԭ�ԣ�2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2��+ 8H2O
2Mn2++10CO2��+ 8H2O
D. H2C2O4�ɷ���������Ӧ��HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��BMO��Bi2MoO6����һ�ָ�Ч������������ڹ�����ⱽ�ӣ�ԭ����ͼ��ʾ������˵������ȷ����

A. �ù��̵��ܷ�Ӧ��C6H6O+7O2![]() 6CO2+3H2O
6CO2+3H2O
B. �ù�����BMO���ֽ�ǿ������
C. �������ķ�����ֻ���м��Թ��ۼ�
D. �ٺ͢��б�����ı��ӵ����ʵ���֮��Ϊ3:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ͬ���������������ֱ�ʢװһ��������ɫ��ͬ��NO2(g)��Br2(g)��Ѹ�ٽ�������ͬʱѹ����ԭ����һ��(�������岻Һ��)������˵����ȷ����(����)

A.a��a������У���ɫͻȻ���Ȼ����dz��������ɫ��ԭ����dz
B.a�䣬b�����ɫһ����
C.a���ѹǿ��a��ѹǿ2��ҪС��b���ѹǿΪb��ѹǿ��2��
D.a���е�c(NO2)һ����b���е�c(Br2)С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3O4�к���![]() ��
��![]() ���ֱ��ʾΪFe����Fe������Fe3O4/PdΪ�����ϣ���ʵ����H2�������Է�ˮ�е��°���NO2�����䷴Ӧ����ʾ��ͼ��ͼ��ʾ������˵������ȷ����
���ֱ��ʾΪFe����Fe������Fe3O4/PdΪ�����ϣ���ʵ����H2�������Է�ˮ�е��°���NO2�����䷴Ӧ����ʾ��ͼ��ͼ��ʾ������˵������ȷ����

A. Pd�Ϸ����ĵ缫��ӦΪ��H2 - 2e�� 2H��
B. Fe������Fe�����ת�����˴��ݵ��ӵ�����
C. ��Ӧ������NO2����Fe����ԭΪN2
D. �ø÷�������ˮ���pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶Ⱥ㶨���ݻ��̶����ܱ������У��������淴Ӧ
mA(s)+nB(g) ![]() pC(g)+qD(g)����֪n=p+q���Ҹ÷�ӦΪ���ȷ�Ӧ����Ӧ�ﵽƽ��ı�־�ǣ� ��
pC(g)+qD(g)����֪n=p+q���Ҹ÷�ӦΪ���ȷ�Ӧ����Ӧ�ﵽƽ��ı�־�ǣ� ��
����ϵ��ѹǿ���ٸı� ��������ܶȲ��ٸı�
�۸������Ũ�Ȳ��ٸı� �ܸ�����������������ٸı�
�ݷ�Ӧ����v(C)��v(D)=p��q
��λʱ����nmol B�ϼ���Ӧ,ͬʱpmol CҲ�ϼ���Ӧ
A. �ڢۢܢ� B. �٢ڢۢ� C. �٢ڢۢܢ� D. �ܢݢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com