
【题目】食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用![]() 溶液检验
溶液检验
B.苯酚和菠萝酯均可与酸性![]() 溶液发生反应
溶液发生反应
C.苯氧乙酸和菠萝酯均可与![]() 溶液发生反应
溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
【答案】D
【解析】
A.苯酚和氯化铁反应发生显色反应,2-氯乙酸和苯氧乙酸都不和氯化铁反应,所以步骤(1)产物中残留的苯酚可用FeCl3溶液检验,故A正确;
B.酚羟基、碳碳双键都能被酸性高锰酸钾溶液氧化,苯酚中含有酚羟基、菠萝酯中含有碳碳双键,所以苯酚和菠萝酯均可与KMnO4酸性溶液发生反应,故B正确;
C.羧基和酯基都能和NaOH溶液反应,苯氧乙酸中含有羧基、菠萝酯中含有酯基,所以二者都能和NaOH反应,前者发生中和反应、后者发生水解反应,故C正确;
D.丙烯醇和菠萝酯中都含有碳碳双键,二者都能和溴发生加成反应而使溴水褪色,所以不能用溴水检验步骤(2)产物中残留的丙烯醇,故D错误;
故答案为D。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0. 1 mol· L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与pH关系如图所示。下列说法正确的是

A. A点对应溶液中:c(Na+)>c(A-)>c(H+)>c(OH-)
B. 25℃时,HA酸的电离常数为1. 0× 10-5.3
C. B点对应的NaOH溶液体积为10 mL
D. 对C点溶液加热(不考虑挥发),则c(A-)/[c(HA)c(OH-)]一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】旧键断裂重组新键是有机反应的特点。如图是乙醇的结构式,乙醇在下列反应中化学键的断裂方式不正确的是( )

A.与金属钠反应:①B.与乙酸进行酯化:②
C.催化氧化:①③D.实验室制取乙烯:②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电解法可提纯含有某些含氧酸根杂质的粗KOH溶液,其工作原理如图所示。下列有关说法错误的是
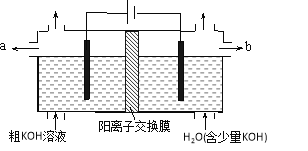
A. 通电后阴极区附近溶液pH会增大
B. 阳极反应式为4OH--4e-=2H2O+O2↑
C. 纯净的KOH溶液从b出口导出
D. K+通过交换膜从阴极区移向阳极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)有机物A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知:
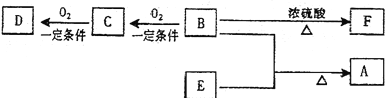
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是: 、 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:
。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2—甲基—1—丙醇和甲酸在一定条件下制取E。该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
B.已知Ksp(AgBr)<Ksp(AgCl) ,故AgBr不可能转化为AgCl
C.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(发现问题)研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
(实验探究)在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如图所示。请你一起参与。
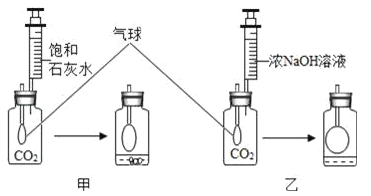
(现象结论)甲装置中产生该实验现象的化学方程式为______________________。解释通常用石灰水而不用NaOH溶液检验CO2的原因________________________________________________;乙装置中的实验现象是___________________________。吸收CO2较多的装置是__________________。
(计算验证)另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH。因此,他认为通过吸收CO2应该用饱和石灰水。
(思考评价)请你对小李同学的结论进行评价:________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常以铜铁矿(主要成分为CuO和Fe3O4,还含少量SiO2等杂质)为原料,冶炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下
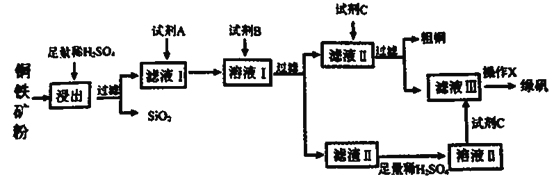
已知:滤渣II的主要成分为Fe(OH)3。请回答下列问题:
(1)如何提高黄铜矿的浸出率___________、___________?(至少答两种方法)
(2)试剂A为___________,其反应的离子方程式为_____________。
(3)试剂B不可能是
A.NH3·H2O B.CuO C.NaOH D.Cu2(OH)2CO3
(4)溶液II中溶质的成分为_______________。
(5)操作X的步骤是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca3N2是重要的化学试剂,易潮解、被氧化,实验室用N2和金属钙在加热条件下制备Ca3N2的装置如图所示(已知:钙能在CO2中燃烧)。请回答下列问题:
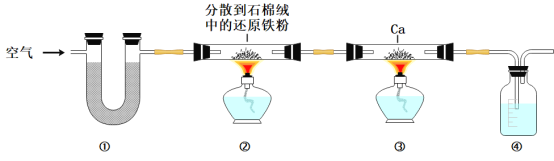
(1)Ca3N2中所含化学键的类型为____________。
A.离子键 B.共价键 C.氢键
(2)装置①中的U型管中的物质为___________,其作用为________________。
(3)装置②的作用为___________________________。
(4)组装好仪器,装入药品,通入空气后,应先点燃____________处酒精灯,再点燃另一个酒精灯。
(5)写出Ca3N2潮解时的化学方程式__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com