
【题目】化合物J是一种重要的医药中间体,其合成路线如图:
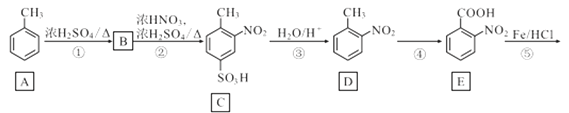
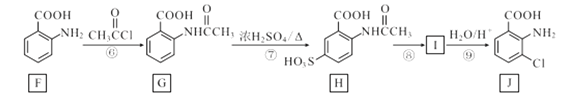
回答下列问题:
(1)G中官能团的名称是__;③的反应类型是__。
(2)通过反应②和反应⑧推知引入—SO3H的作用是__。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。写出F与足量氢气反应生成产物的结构简式,并用星号(*)标出其中的手性碳__。
(4)写出⑨的反应方程式__。
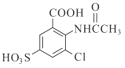
(5)写出D的苯环上有三个不相同且互不相邻的取代基的同分异构体结构简式_。
(6)写出以对硝基甲苯为主要原料(无机试剂任选),经最少步骤制备含肽键聚合物的合成路线__。
【答案】羧基、肽键(或酰胺键) 取代反应 定位 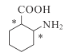
 +2H2O
+2H2O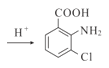 +CH3COOH+H2SO4
+CH3COOH+H2SO4 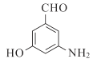 或
或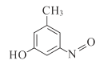 (任写1种)
(任写1种) 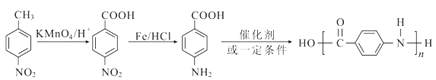
【解析】
(1)根据流程图中的结构简式和反应物转化关系分析;
(2)通过反应②和反应⑧推知引入—SO3H的作用是控制反应中取代基的位置;
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳,根据结构简式分析;
(4)根据流程图中H和J的结构简式可断定I的结构简式为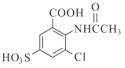 ;
;
(5)根据题目要求分析,结合取代基位置异构,判断同分异构体的数目。
(6)先用酸性高锰酸钾溶液将甲基氧化为羧基,然后用“Fe/HCl”将硝基还原为氨基,得到对氨基苯甲酸,然后在催化剂作用下,发生缩聚反应生成含肽键的聚合物。
(1)根据G的结构图,G中官能团的名称是羧基和肽键(或酰胺键);反应③中C的—SO3H被取代生成D,则反应类型是取代反应;
(2)通过反应②和反应⑧推知引入—SO3H的作用是控制反应过程中取代基的连接位置,故起到定位的作用;
(3) F是邻氨基苯甲酸,与足量氢气发生加成反应生成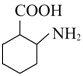 ,与羧基、氨基连接的碳原子是手性碳原子,可表示为:
,与羧基、氨基连接的碳原子是手性碳原子,可表示为: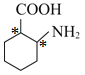 ;
;
(4) 根据流程图中H和J的结构简式可断定I的结构简式为 ,⑨的反应方程式:
,⑨的反应方程式: +2H2O
+2H2O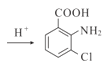 +CH3COOH+H2SO4;
+CH3COOH+H2SO4;
(5) D的结构简式为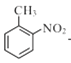 ,苯环上有三个不相同且互不相邻的取代基的同分异构体,即三个取代基在苯环上处于邻间对位置上,同分异构体结构简式
,苯环上有三个不相同且互不相邻的取代基的同分异构体,即三个取代基在苯环上处于邻间对位置上,同分异构体结构简式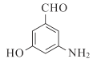 或
或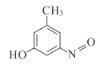 (任写1种);
(任写1种);
(6)先用酸性高锰酸钾溶液将甲基氧化为羧基,然后用“Fe/HCl”将硝基还原为氨基,得到对氨基苯甲酸,然后在催化剂作用下,发生缩聚反应生成含肽键的聚合物,不能先把硝基还原为氨基,然后再氧化甲基,因为氨基有还原性,容易被氧化,故合成路线如下: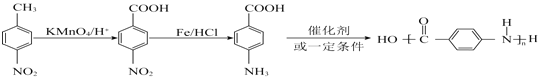 。
。


科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
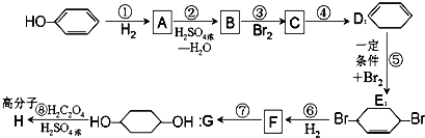
请回答下列问题:
(1)B,F的结构简式为:B___,F_______;
(2)反应①~⑦中属于消去反应的是(填代号)_______;
(3)根据反应![]() +Br2
+Br2![]()
![]() ,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
(4)写出第④步C→![]() 的化学方程式(有机物写结构简式,注明反应条件)__;
的化学方程式(有机物写结构简式,注明反应条件)__;
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A﹣G这七种有机物分子中含有手性碳原子的是(填序号)__;
(6)核磁共振谱是测定有机物分子结构最有用的工具之一,在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目,例如:乙醛的结构式为:![]() ,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
A ![]() B
B ![]() C
C ![]() D
D ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
![]() +KMnO4→
+KMnO4→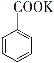 + MnO2
+ MnO2 +HCl→
+HCl→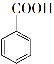 +KCl
+KCl
名称 | 相对分 子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL1) | 溶解性 |
甲苯 | 92 | 95 | 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | —— | 微溶于冷水,易溶于乙醇、热水 |
实验步骤:
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25. 00 mL溶液,用0.01000 mol·L1的KOH标准溶液滴定,三次滴定平均消耗21. 50 mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(2)在反应装置中应选用______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是___________;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______。
(6)本实验制备的苯甲酸的纯度为_______;据此估算本实验中苯甲酸的产率最接近于_______(填标号)。
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中__________的方法提纯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
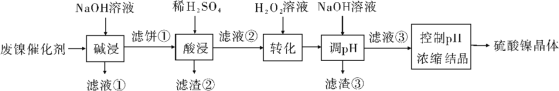
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀时(c=0.01 mol·L1)的pH 沉淀完全时(c=1.0×105 mol·L1)的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代H2O2的物质是______________。若工艺流程改为先“调pH”后“转化”,即
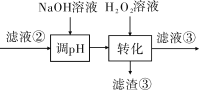
“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=______________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L1,则“调pH”应控制的pH范围是______________。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列物质①过氧化钠、②氧化铝、③硅、④二氧化硅、⑤NaHCO3。请填空:(填序号)
可用来制计算机芯片的是_________。可用于呼吸面具中作为氧气来源的是______。能作光导纤维的是_________。能作耐火材料的是_______。属于电解质的是 _________________。属于盐的是 ______,该盐受热分解的化学方程式为:_____________________________。
(2)除去FeCl2溶液中混有的FeCl3,相应的离子方程式是_______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯基环丁烯酮(![]() PCBO)是一种十分活泼的反应物,可利用它的开环反应合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如下:
PCBO)是一种十分活泼的反应物,可利用它的开环反应合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如下:
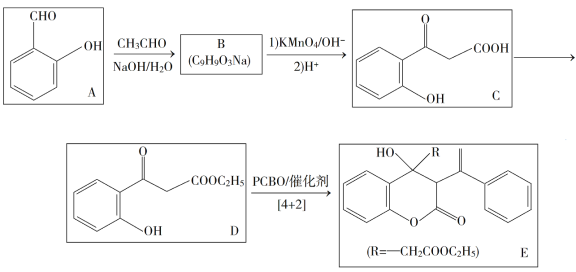
已知如下信息:

回答下列问题:
(1)A的化学名称是___________。
(2)B的结构简式为___________。
(3)由C生成D所用的试别和反应条件为___________;该步反应中,若反应温度过高,C易发生脱羧反应,生成分子式为C8H8O2的副产物,该副产物的结构简式为________。
(4)写出化合物E中含氧官能团的名称__________;E中手性碳(注:连有四个不同的原子或基团的碳)的个数为___________。
(5)M为C的一种同分异构体。已知:1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧化碳;M与酸性高锰酸钾溶液反应生成对苯二甲酸。M的结构简式为__________。
(6)对于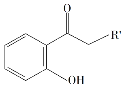 ,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深入研究,R'对产率的影响见下表:
,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反应进行深入研究,R'对产率的影响见下表:
R' | —CH3 | —C2H5 | —CH2CH2C6H5 |
产率/% | 91 | 80 | 63 |
请找出规律,并解释原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①硫酸比次氯酸稳定②硫酸的酸性弱于高氯酸③![]() 比HCl易被氧化④
比HCl易被氧化④![]() 比
比![]() 更容易由单质合成⑤盐酸的酸性比氢硫酸强。上述事实能说明硫的非金属性比氯弱的是
更容易由单质合成⑤盐酸的酸性比氢硫酸强。上述事实能说明硫的非金属性比氯弱的是
A.①②③B.③④⑤C.②③④D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com