
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为__________。
(3)若甲、乙、丙溶液体积均为500 mL,当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状 况),乙池中溶液PH=_______,丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
(5)某溶液中可能含有下列离子中的两种或几种:Ba2+、H+、SO42-、 SO32- 、HCO3-、 Cl-。
①当溶液中有大量H+存在时,则不可能有_______________________离子存在。
②当溶液中有大量Ba2+存在时,溶液中不可能有_________________离子存在。
③采用惰性电极从上述离子中选出适当离子组成易溶于水的电解质,对其溶液进行电解若两极分别放出气体,且体积比为1∶1,则电解质化学式是________________。
【答案】原电池 CH3OH + 8OH - 6e = CO32- + 6H2O 阳极 4AgNO3 + 2H2O![]() 4Ag + O2↑ + 4HNO3 280 1 D 1.6 减小 增大 SO32- 、HCO3- SO42-、 SO32- HCl、BaCl2
4Ag + O2↑ + 4HNO3 280 1 D 1.6 减小 增大 SO32- 、HCO3- SO42-、 SO32- HCl、BaCl2
【解析】
串联电路的电化学的计算题,注意紧扣“串联电路中电流处处相等”规律,即抓住每个电极上转移的电子数目一样解题即可。
(1)甲池为原电池,燃料CH3OH在负极失电子,发生氧化反应,在碱溶液中生成碳酸盐,故甲池中通入CH3OH电极的电极反应为:CH3OH-6e-+8OH-═CO32-+6H2O;
(2)乙池是电解池,A为阳极,电解OH-。B为阴极,电解Ag+。电池中电解硝酸银溶液生成银、硝酸和氧气,电池反应为:4AgNO3 + 2H2O![]() 4Ag + O2↑ + 4HNO3;
4Ag + O2↑ + 4HNO3;
(3)当乙池中B极质量增加5.4g为Ag,n(Ag)=![]() =0.05mol,依据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=
=0.05mol,依据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=![]() 22,4L/mol=0.28L=280ml。乙池中Ag~H+,n(H+)=0.05mol,c(H+)=
22,4L/mol=0.28L=280ml。乙池中Ag~H+,n(H+)=0.05mol,c(H+)=![]() =0.1mol/L,故乙池中溶液PH=1。依据电子守恒计算,2Ag~Cu,丙池中阴极D极析出m(Cu)=0.05mol
=0.1mol/L,故乙池中溶液PH=1。依据电子守恒计算,2Ag~Cu,丙池中阴极D极析出m(Cu)=0.05mol![]() 64g/mol=1.6g;
64g/mol=1.6g;
(4)若丙中电极不变,将其溶液换成NaCl溶液,则乙中电解NaCl溶液生成氢氧化钠,所以溶液的pH增大;
(5)①当溶液中有大量H+存在时,SO32- 、HCO3-离子会与H+反应生成气体和水,则不可能有SO32- 、HCO3-离子存在;
②当溶液中有大量Ba2+存在时,SO42-、 SO32-离子会与Ba2+反应生成沉淀,则溶液中不可能有SO42-、 SO32-离子存在;
③采用惰性电极从上述离子中选出适当离子组成易溶于水的电解质,两极分别放出气体且为1∶1,则应是放出H2、Cl2,符合要求的有:HCl、BaCl2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中不正确的是
A. 14g由N2和13C2H2组成的混合物中,所含中子数为7NA
B. CH4与白磷(P4)都为正四面体结构,则1mol CH4与lmolP4所含共价键的数目均为4NA
C. 反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
D. 常温下,含0.5molNH4NO3与xmolNH3·H2O的中性溶液中,含有NH4+的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液中粒子浓度的关系式中,正确的是
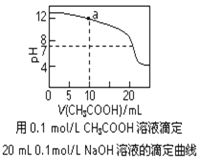
A. pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B. 0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C. 图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D. 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
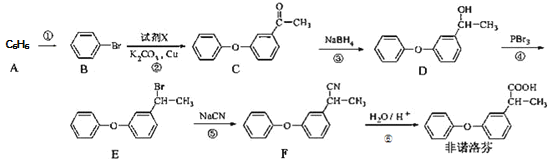
回答下列问题
(1)![]() 的化学名称是_____________,
的化学名称是_____________,![]() 中含氧官能团的名称为___________。
中含氧官能团的名称为___________。
(2)上述反应中,反应①的条件是___________,过程①属于______反应
(3)反应②发生的是取代反应,且另一种产物有![]() ,写出由
,写出由![]() 生成
生成![]() 的化学方程式______。
的化学方程式______。
(4)有机物![]() 与非诺芬互为同分异构体,
与非诺芬互为同分异构体,![]() 满足下列条件:
满足下列条件:
I.能与NaHCO3溶液反应,且能与FeCl3溶液发生显色反应
II.分子中有6种不同化学环境的氢,且分子中含有两个苯环
![]() 的结构有_____种,写出其中一种不能与浓溴水发生取代反应的
的结构有_____种,写出其中一种不能与浓溴水发生取代反应的![]() 的结构简式_________。
的结构简式_________。
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备
为原料制备 路线流程图(无机试剂任用)_________
路线流程图(无机试剂任用)_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜品油烯(D)可用作香料的原料,它可由A合成得到如下所示,下列说法正确的是 ( )
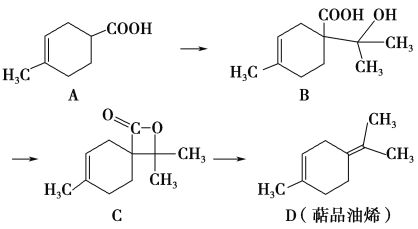
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 1 mol有机物A中含有1.204×1024个双键
D. 有机物C的同分异构体中不可能有芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中下列各物质间不能实现 (“→”表示一步完成)转化的是
(“→”表示一步完成)转化的是
选项 | A | B | C | D |
a | CH3CH2OH | CH2=CH2 | Cl2 | C |
b | CH3CHO | CH3CH2Br | HClO | CO |
c | CH3COOH | CH3CH2OH | HCl | CO2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料M的一种合成流程如下:

已知:①![]()
②R1COOH![]() R1COOR
R1COOR
请回答下列问题:
(1)M中含碳的官能团名称是___________;设计R→X和Y→Z步骤的目的是___________。
(2)A→B的反应类型是___________,R分子中最多有___________个原子共平面。
(3)R和M在下列仪器中信号完全相同的是___________(填字母)
a红外光谱仪 b质谱仪 c元素分析仪 d核磁共振氢谱仪
(4)写出C和Z反应生成M的化学方程式:______________________。
(5)在Y的同分异构体中,同时满足下列条件的结构有___________种(不考虑立体异构)。
①能发生银镜反应
②遇氯化铁溶液发生显色反应
③1mol有机物最多能消耗3 mol NaOH
(6)已知苯环上有烃基时,新引入取代基主要取代邻位、对位氢原子。参照上述合成流程,设计以苯和异丙醇为原料制备Br![]() 的合成路线:_________________(无机试剂任选)
的合成路线:_________________(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种芳香族化合物都是某些植物挥发油中主要成分,有的是药物,有的是香料。它们的结构简式如下所示:
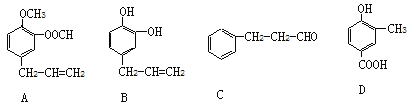
(1)写出上述有机物A中官能团的名称_______________________________________。
(2)能与新制Cu(OH)2反应的有________________________(用A、B、C、D填写)。写出含碳原子数较少的物质与新制Cu(OH)2反应生成砖红色沉淀的化学反应方程式:________________________________
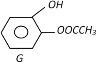
(3)① D一种同分异构体G的结构简式如上图:写出G与足量NaOH溶液共热反应方程式:_____________
② D的另一种同分异构体H,其苯环上有两个相邻的取代基,它既能使FeCl3溶液变紫色,又能与NaHCO3溶液反应放出CO2气体,H的结构简式是______________________________。
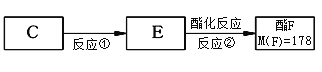
(4)按上图,C经一步反应可生成E,E是B的同分异构体,则反应①属于__________反应,F结构简式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g) ![]() xQ(g)+3R(g),10 s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10 s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为________。
(2)前10 s内用M表示的化学反应速率为________。
(3)化学方程式中x值为________。
(4)在恒温恒容条件下,往容器中加入1 mol氦气,反应速率________(填“增大”、“减小”或“不变”,下同)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com