
【题目】800℃时,在2L的密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2,n(NO)随时间的变化如下表所示。
2NO2,n(NO)随时间的变化如下表所示。
时间∕s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)∕mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)从0~3s内,用NO表示的平均反应速率υ(NO)=_____________。
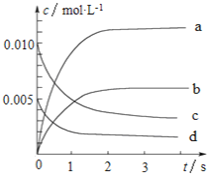
(2)图中表示NO浓度变化的曲线是_______(填字母代号)。
(3)达平衡时NO的转化率为________。
(4)能说明该反应已达到平衡状态的是_________(填序号)。
A.混合气体的颜色保持不变
B.混合气体的密度保持不变
C.υ逆 (NO2)=2υ正 (O2)
D.混合气体的平均相对分子质量保持不变
(5)若升温到850℃,达平衡后n(NO)=n(NO2),则反应向________(填“正反应方向”、“逆反应方向”)移动。
(6)若在一定条件下0.2molNO气体与氧气反应,达平衡时测得放出的热量为akJ,此时NO转化率为80%,则2molNO气体完全反应放出的热量为____________。
【答案】(1)2.17×103mol·L1·s1;(2)c;(3)65%;(4)ACD;(5)逆反应方向;(6)12.5akJ;
【解析】
试题(1)根据题意可知,在3s时,反应用去的NO为0.02mol-0.007mol=0.013mol,所以NO的反应速率v=![]() =2.17×103mol·L1·s1,故答案为:2.17×103mol·L1·s1;
=2.17×103mol·L1·s1,故答案为:2.17×103mol·L1·s1;
(2)根据2NO(g)+O2(g)![]() 2NO2,右图中表示NO浓度变化的曲线是c,故答案为:c;
2NO2,右图中表示NO浓度变化的曲线是c,故答案为:c;
(3)达平衡时NO的转化率为![]() ×100%=65%,故答案为:65%;
×100%=65%,故答案为:65%;
(4)A.混合气体的颜色保持不变,表示,二氧化氮的浓度不变,能说明该反应已达到平衡状态,正确;B.容器的体积不变,气体的质量不变,混合气体的密度始终保持不变,不能说明该反应已达到平衡状态,错误;C.υ逆(NO2)=2υ正(O2) 表示正逆反应速率相等,能说明该反应已达到平衡状态,正确;D.该反应属于气体的物质的量发生变化的反应,混合气体的平均相对分子质量保持不变,能说明该反应已达到平衡状态,正确,故选ACD;
(5)在800℃时,得到平衡时,n(NO)=0.007mol,根据方程式n(NO2)=0.013mol,若升温到850℃,达平衡后n(NO)=n(NO2),则反应向逆反应方向移动,故答案为:逆反应方向;
(6)转化的NO的物质的量为0.2mol×80%=0.16mol,放出的热量为akJ,所以0.2molNO反应放出的热量为![]() ×akJ=12.5aKJ,故答案为:12.5akJ。
×akJ=12.5aKJ,故答案为:12.5akJ。


科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾 病的药物。以2氯苯甲醛为原料合成该药物的路线如下:

(1)A中官能团名称为_____,A发生银镜反应的化学方程式为_____。
(2)C生成D的反应类型为_____。
(3)X(C6H7BrS)的结构简式为_____。
(4)写出C聚合成高分子化合物的化学反应方程式:_____。
(5)物质G是物质A的同系物,比A多一个碳原子,符合以下条件的G的同分异构体共有______种。
①除苯环之外无其他环状结构;②能发生银镜反应。 其中核磁共振氢谱中有5个吸收峰,且峰值比为2∶2∶1∶1∶1的结构简式为_____。
(6)已知: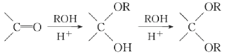 ,写出以乙烯、甲醇为有机原料制备化 合物
,写出以乙烯、甲醇为有机原料制备化 合物![]() 的合成路线(无机试剂任选)__________
的合成路线(无机试剂任选)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上运用电化学方法降解含NO3-废水的原理如图所示,下列有关说法不正确的是

A. 相同条件下,Pt电极上产生O2和Pt-A电极上产生N2的体积比为5:2
B. 通电时电子的流向:b电极→导线→Pt-Ag电极→溶液→Pt电极→导线→a极
C. Pt-Ag电极上的电极反应式:2NO3-+12H++10e-=N2+6H2O
D. 通电时,Pt电极附近溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物在工业生产、生活中具有非常广泛的用途。
(1)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H1=akJ·mol-1
②PbS(s)2PbO(s)=3Pb(s)+SO2(g) △H2=b kJ·mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) △H3=c kJ·mol-1
反应3PbS(s)+6O2(g)=3PbSO4(s) △H=____________kJ·mol-1(用含a、b、c的代数式表示)
(2)以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:
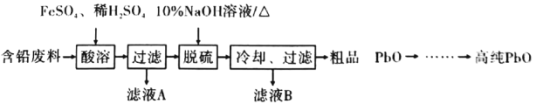
①“酸溶”时,在Fe2+催化下,Pb和PbO2反应成1 mol PbSO4时转移电子的物质的量为_________ mol。
②已知:PbO溶解在NaOH溶液中,存在化学平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq),其溶解度曲线如图1所示:
NaHPbO2(aq),其溶解度曲线如图1所示:

结合上述信息,完成由粗品PbO(所含杂质不溶于NaOH溶液)得到高纯PbO的操作:将粗品PbO溶解在一定量________(填“35%”或“10%”)的NaOH溶液中,加热至110℃,充分溶解后,_______________(填 “趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO固体。
(3)将粗品PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图2所示:

①阴极的电极反应式为______________________;
②当有4.14gPb生成时,通过质子交换膜的n(H+)=______________________。
(4)PbI2可用于人工降雨。取一定量的PbI2固体,用蒸馏水配制成t℃饱和溶液,准确移取25.00 mL PbI2饱和溶液分次加入阳离子交换树脂RH+(发生反应:2RH++PbI2 =R2Pb+2H++2I-),用250ml洁净的锥形瓶接收流出液,后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并盛放到锥形瓶中(如图3)。加入酚酞指示剂,用0.0050mol·L-1NaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液10.00mL。可计算出t℃时Ksp(PbI2)为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表标出的是元素周期表的一部分元素,回答下列问题:
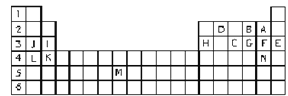
①表中用字母标出的14种元素中,化学性质最不活泼的是____________(用元素符号表示,下同),金属性最强的是____________,常温下单质为液态的非金属元素是____________。
②B、F、C气态氢化物中以________(填分子式)最不稳定。
Ⅱ. 有短周期的A、B、C、D、E 五种元素,它们在周期表的位置如图所示。已知A原子最外层电子数是次外层电子数的2倍。试回答下列问题:
![]()
(1) 元素E在周期表中位于第_______周期_______族。
(2) 元素A的最高价氧化物的电子式为________,元素D的原子结构示意图为________;
(3) 比较C、D两种元素最高价氧化物对应水化物的酸性强弱:______ > ______。(用分子式表示)
(4)元素C的气态氢化物与元素E的最高价氧化物对应水化物化合生成的正盐的化学式为___________,该盐的晶体类型为________。
(5) ①元素B所在周期的简单离子半径最小的是______。(用离子符号表示)
②元素C、D的简单氢化物沸点较高的是______。(用分子式表示)
(6)请用电子式表示Na2S的形成过程____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是
A.Na+、OH-、SiO32-、Cl-B.Fe3+、 NH4+、SCN-、Cl-
C.Fe2+ 、H+、Na+ 、MnO4-D.Na+、AlO2-、SO42-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖授予研究“分子机器的设计与合成”的三位科学家。轮烷是一种分子机器的轮子,合成轮烷的基本原料有苯、丙烯、二氯甲烷、戊醇。下列说法正确的是( )
A. 苯能与溴水发生加成反应 B. 丙烯能被酸性KMnO4氧化
C. 戊醇易溶于水 D. 二氯甲烷有两种同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com