
【题目】电子云上面的黑点表示的是_______。
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列四种元素中,单质的氧化性最强的是 ( )
A. 原子最外层电子数为次外层电子数的2倍 B. 第16号元素
C. 原子核外L层电子数为K层电子数的三倍 D. 第三周期IIIA族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”,工业上用钛矿石(主要成分:FeO、TiO2,SiO2等)为原料制取钛,工艺流程如下,回答下列问题:

已知:TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是__________。
(2)操作1名称为_______,固体2的主要成分是______, 写出金属钠与TiCl4共热的化学反应方程式_________________。
(3)一定温度下,在一个固定容积的容器中发生反应:TiO2(s)+2Cl2(g)+2C(s)![]() TiCl4(g)+2CO(g),反应中氧化剂是________,下列说法能够说明该反应已达化学平衡状态的是_________________。
TiCl4(g)+2CO(g),反应中氧化剂是________,下列说法能够说明该反应已达化学平衡状态的是_________________。
A.反应每断裂2个Cl一Cl键,同时生成2 个C![]() O键
O键
B. 容器内压强不再发生变化
C. Cl2和TiCl4的浓度不再变化
D.v(TiCl4)正=2v(C)逆
(4)将50吨钛矿石经上述变化后,最终可得金属钛12吨,假设各步反应均完全,则原矿石中TiO2的百分含量为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题.

(1)该浓盐酸中HCl的物质的量浓度为 ______ molL-1.
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______ .
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl-的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次并在操作步骤空白处填上适当仪器名称) ______ .
A.用30mL水洗涤 ______ 2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用 ______ 加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括 号内填“偏大”,“偏小”,或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面 ______
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 在共价化合物中一定含有共价键
B. 由非金属元素组成的化合物一定是共价化合物
C. 含有离子键的化合物一定是离子化合物
D. 双原子单质分子中的共价健一定是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
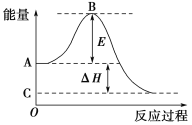
(1)图中A点表示:________________________________________;
C点表示:________________。E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:

(1)表中硫酸的质量分数W1为_____(不写单位,用含c1、p1的代数式表示)。
(2)物质的量浓度为c1mol· L-1质量分数为w1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为________ mol· L-1,质量分数_______w1/2(填“大于”、“小于”或“等于”,下同)。
(3)质量分数为w2的氨水与w2/5的氨水等质量混合,所得溶液的密度_____![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com