
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
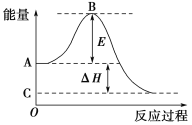
(1)图中A点表示:________________________________________;
C点表示:________________。E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】化学方程式为3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O,下列说法中正确的( )
3K2MnO4+KCl+3H2O,下列说法中正确的( )
A. 反应中MnO2是氧化剂 B. 该反应属于复分解反应
C. KClO3在反应中失去电子 D. 反应中每生成lmol K2MnO4,氧化剂得到2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式 。
(2)根据等电子原理,写出CO分子的结构式 。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O 沉淀。
①甲醇的沸点比甲醛的高,其主要原因是 ;
甲醛分子中碳原子轨道的杂化类型为 。
②甲醛分子的空间构型是 ;
1mol甲醛分子中σ键的数目为 。
③在1个Cu2O 晶胞中(结构如图所示),

所包含的Cu 原子数目为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z。反应2min 后,测得参加反应的X2为0.6mol/L,用Y2的变化表示的反应速率v(Y2) =0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应的化学方程式是
A. X2+2Y2 ![]() 2XY2 B. 2X2+Y2
2XY2 B. 2X2+Y2![]() 2X2Y
2X2Y
C. 3X2+Y2![]() 2X3Y D. X2+3Y2
2X3Y D. X2+3Y2![]() 2XY3
2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素的原子间在形成化合物时容易形成共价键的是
原子 | a | b | c | d | e | f | g |
M层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
A. a和c B. a和f
C. d和g D. b和g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是最普通、最常见的物质之一。
(1)“水”有很多种。下列“水”属于纯净物的是 ________ (填字母序号)。
A.河水 B.自来水 C.矿泉水 D.蒸馏水
(2)电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为________ 。
(3)水是重要的溶剂和化工原料。氯碱工业以饱和食盐水为原料获得烧碱等化工产品,反应原理为:![]() 。
。
①20℃时,NaCl 的溶解度是36 g。该温度下,饱和食盐水中溶质与溶剂的质量比为______。
②烧碱可用于处理硫酸泄漏,反应的化学方程式为__________。
(4)水在化学实验中具有重要作用。将铁丝放在潮湿的空气中(如下图所示),一段时间后,观察到导管内液面下降,导管口有气泡冒出,关闭 K。请解释导管内液面上升和下降的原因:___________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、社会、生产、生活等关系密切,下列有关说法不正确的是( )
A.部分卤代烃可用作灭火剂
B.福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜
C.提倡人们购物时不用塑料袋,是为了防止白色污染
D.石油分馏是物理变化,可得到汽油、煤油和柴油等产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com