
【题目】下列有关活化分子的说法正确的是( )
A.增大反应物浓度可以提高活化分子百分数
B.增大体系的压强一定能提高活化分子百分数
C.使用合适的催化剂可以增大活化分子的能量
D.升高温度能提高活化分子百分数
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】三氯化硼的熔点为-107.3℃,沸点为12.5℃,易水解生成硼酸和氯化氢,可用于制造高纯硼、有机合成催化剂等。实验室制取三氯化硼的原理为:B2O3+3C+3Cl2![]() 2BCl3+3CO
2BCl3+3CO
(1)甲组同学拟用下列装置制取纯净干燥的氯气(不用收集)。

①装置B中盛放的试剂是 ,装置C的作用是 。
②装置A中发生反应的离子方程式为 。
(2)乙组同学选用甲组实验中的装置A、B、C和下列装置(装置可重复使用)制取BCl3并验证反应中有CO生成。

①乙组同学的实验装置中,依次连接的合理顺序为
A→B→C→ → → → → →F→D→I。
②实验开始时,先通入干燥N2的目的是 。
③能证明反应中有CO生成的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七铝十二钙 (12CaO·7Al2O3)是一种新型的超导材料和发光材料,它是用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后锻烧沉淀制备。工业上制备AlC13溶液用图示流程(已知A1C13易升华)。
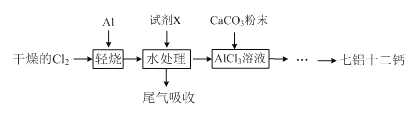
(1)轻烧后的气体用水处理前导气管为何要保温?
(2)用水处理添加的试剂X是 ,其目的是 。
(3)AlC13溶液溶解CaCO3时,要控制碳酸钙和AlC13的量,要求n(CaCO3): n(A1C13)> 12:14,其原因是 。用氨水沉淀、过滤后的滤液主要成分是 。
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12·2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水, 。(实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计)。
已知:几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
开始沉淀的pH | 完全沉淀的pH | |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.5 | 4.7 |
补全实验步骤: 冰水洗涤,干燥,得到CaC12·2H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1mol/L的氢氧化钠与0.06mol/L硫酸溶液等体积混合,该混合溶液的PH等于( )
A. 1.7 B. 2.0 C. 12.0 D. 12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)=4C(g)+2D(g),在相同时间内,用不同物质表示的平均反应速率如下,则反应速率最快的是( )
A.v(A)=0.4 mol/(L·s)
B.v(B)=0.8 mol/(L·s)
C.v(C)=1.2 mol/(L·s)
D.v(D)=0.7 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁可用于水的净化,其化学式可表示为[Fea(OH)b(SO4)c]m。取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的BaCl2溶液,得到白色沉淀6.99 g。另一份溶液,先将Fe3+还原为Fe2+,再用0.1600 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液25.00 mL。该聚合硫酸铁样品中a:b的比值为(已知:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O)。
A.1∶1 B.2∶1 C.3∶1 D.2∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)E、F、G三种元素的原子序数依次增大,其原子的最外层电子排布均为4s1。则F元素在其化合物中最高化合价为 。
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体;基态Ni原子的电子占有 种能量不同的原子轨道。
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。
如①CH2=CH2 ②CH≡CH③![]() ④
④![]() 等,其中C原子为sp2杂化的分子有 (填序号),预测HCHO分子的立体结构为 形。
等,其中C原子为sp2杂化的分子有 (填序号),预测HCHO分子的立体结构为 形。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com