
已知NaHSO4在水中的电离方程式为:NaHSO4===Na++H++SO 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性
B.水电离出来的c(H+)=1×10-10 mol·L-1
C.c(H+)=c(OH-)+c(SO )
)
D.该温度高于25 ℃
科目:高中化学 来源: 题型:
下列关于电离平衡常数(K)的说法正确的是
A.电离平衡常数(K)越小,表示弱电解质电离能力越弱
B.电离平衡常数(K)与温度无关
C.不同浓度的同一弱电解质,其电离平衡常数(K)不同
D.多元弱酸各步电离平衡常数相互关系为:K1<K2<K3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铁的叙述正确的是( )
A.在空气中,铁丝如同镁条一样能被点燃,并发出耀眼的强光
B.铁是地壳里含量最多的金属元素
C.铁在高温下与水蒸气反应生成氢气和四氧化三铁
D.铁能与稀盐酸、浓硫酸、碳酸等酸反应生成氢气和亚铁盐
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用0.200 0 mol·L-1的标准N aOH溶液滴定未知浓度的盐酸,其操作为如下几步:
aOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00 mL待 测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是________________(填编号),该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)________________。
(2)判断滴定终点的现象是:锥形瓶中溶液从________色变为________色,且半分钟内不变色。
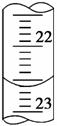
(3)如图是某次滴定时的滴定管中的液面,其读数为________ mL。
(4)根据下列数据:请计算待测盐酸溶液的浓度为________ mol·L-1。
| 滴定 次数 | 待测液 体积(mL) | 标准NaOH溶液读数记录(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 2 | 4.0 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将pH=1的盐酸平均分成两份,一份加入适量水,另一份加入与该盐酸物质的量浓度相同的适量NaOH溶液,pH都升高了1,则加入的水与NaOH溶液的体积比为
A.9 B.10
C.11 D.12
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验方法或试剂不能达到实验目的的是( )
A.鉴别SO2和CO2气体:用澄清石灰水
B.证明溶液中含有NH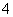 :用浓NaOH溶液和蓝色石蕊试纸
:用浓NaOH溶液和蓝色石蕊试纸
C.鉴别Br-和I-用双氧水和淀粉溶液
D.鉴别NO2和溴蒸气:用蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解得到溶液A,并产生大量气体B。实验室现有下列试剂:0.01 mol/L酸性KMnO4溶液、0.1 mol/L KI溶液,3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他人探究所得溶液和气体的成分。
[提出猜想]
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体可能含有________中的一种或两种。
| 实验操作 | 预期现象 | 结论 | |
| 验证 猜想Ⅰ | 步骤①:取少量0.01 mol/L酸性KMnO4溶液,滴入所得溶液 | ||
| 步骤② | 含有Fe3+ | ||
| 验证 猜想Ⅱ | 将所得气体通入如下装置 | 含有两 种气体 |
[实验探究]
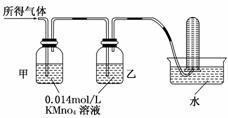
[问题讨论]
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,判断该方法是否正确并进行评价:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)常温时,四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液。
①Ⅲ和Ⅳ的溶液中水电离的c(H+)浓度之比_____________________________________。
②下列有关叙述正确的是________。
A.Ⅱ、Ⅲ的溶液分别与10 g铝粉反应,生成H2的量Ⅲ更多
B.将Ⅰ和Ⅲ等体积混合后,溶液pH小于7
C.四种溶液各10 mL分别加水稀释至100 mL后,溶液的pH:Ⅲ>Ⅳ> Ⅰ>Ⅱ
Ⅰ>Ⅱ
(2)CH3COOH溶液的Ka=1.6×10-5,则1.0 mol·L-1的CH3COONa溶液 中c(OH-)=________________________________________________________________________。
中c(OH-)=________________________________________________________________________。
(3)将CO2通入NaOH溶液中,回答下列问题。
①当CO2与NaOH物质的量之比为1∶2时,溶液中离子浓度的大小顺序为________________________________________________________________________。
②当c(Na+)=c(CO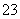 )+c(HCO
)+c(HCO )+c(H2CO3)时,反应后溶液中的溶质为________。
)+c(H2CO3)时,反应后溶液中的溶质为________。
(4)用NaOH溶液滴定醋酸溶液的过程中,锥形瓶中的溶液其离子浓度关系有如下式子,在滴定过程中这些式子出现的先后顺序为________(请选出正确的顺序)。
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
②c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
③c(CH3COO-)>c(H+)=c(Na+)>c(OH-)
④c(Na+)>c(CH3COO-)=c(OH-)>c(H+)
⑤c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
⑥c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
⑦c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
A.⑦④①⑥②③⑤ B.⑤②③①⑥④⑦
C.③⑤②①⑥④⑦ D.⑤③②⑥①④⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com