
【题目】钛是一种性能非常优越的金属,21世纪将是钛的世纪。
(1)TiO2薄膜中掺杂铬能显著提高光催化活性。基态Ti原子的价电子排布图为___________。
(2)四乙醇钛能增加橡胶在金属表面的粘附性。其制备原理如下:TiCl4+4CH3CH2OH+4NH3=Ti(OCH2CH3)4+4NH4Cl。
①Ti(OCH2CH3)4可溶于有机溶剂,常温下为淡黄色透明液体,其晶体类型为_________。
②N和O位于同一周期,O的第二电离能大于N的第二电离能的原因是___________。
③NH4Cl中存在的作用力有________,NH4Cl熔沸点高于CH3CH2OH的原因是________,Ti(OCH2CH3)4分子中C原子的杂化形式均为__________。
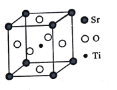
(3)钛酸锶(SrTiO3)可作电子陶瓷材料和人造宝石,其中一种晶胞结构如图所示。若Ti位于顶点位置,O位于__________位置;已知晶胞参数为a nm,Ti位于O所形成的正八面体的体心,则该八面体的边长为__________m(列出表达式)。
【答案】 分子晶体 O和N分别失去一个电子后的电子排布式1s22s22p3和1s22s22p2,前者是半充满结构,比后者稳定,所以第二电离能,前者大于后者 配位键、离子键、共价键 前者为离子晶体,后者为分子晶体(或离子键强于分子间作用力),离子晶体的熔沸点高于分子晶体的熔沸点 sp3杂化 棱心
分子晶体 O和N分别失去一个电子后的电子排布式1s22s22p3和1s22s22p2,前者是半充满结构,比后者稳定,所以第二电离能,前者大于后者 配位键、离子键、共价键 前者为离子晶体,后者为分子晶体(或离子键强于分子间作用力),离子晶体的熔沸点高于分子晶体的熔沸点 sp3杂化 棱心 ![]()
【解析】
根据核外电子的排布规则写出Ti的核外电子排布式;根据相似相容原理,判断晶体的类型;从氯化铵的电子式,判断化学键的类型;从晶体的类型不同判断熔沸点差异的原因;Ti(OCH2CH3)4分子中C原子的成键数目判断杂化方式;从晶胞的内部结构,根据Ti的位置,判断氧的位置;根据Ti和O的距离,计算八面体的边长,据此分析。
(1)Ti原子是22号元素,核外电子排布式为[Ar]3d24s2,其价电子排布图为 ;
;
(2)①Ti(OCH2CH3)4可溶于有机溶剂,有机溶剂大多数都是分子晶体,根据相似相溶,Ti(OCH2CH3)4是分子晶体;
②O和N分别失去一个电子后的价电子排布式2s22p3和2s22p2,前者是半充满结构,比后者稳定,所以第二电离能,前者大于后者;
③根据氯化铵的电子式: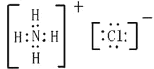 ,可以看出氯化铵中的化学键有铵根离子和氯离子间的离子键,氮原子和氢原子间共价键,氮原子与三个氢原子形成三对共价键,剩余一对电子与氢原子形成一对配位键,所以氯化铵中存在的作用力有离子键,共价键,配位键;Ti(OCH2CH3)4分子中C均形成四对σ键,故杂化方式为sp3杂化;
,可以看出氯化铵中的化学键有铵根离子和氯离子间的离子键,氮原子和氢原子间共价键,氮原子与三个氢原子形成三对共价键,剩余一对电子与氢原子形成一对配位键,所以氯化铵中存在的作用力有离子键,共价键,配位键;Ti(OCH2CH3)4分子中C均形成四对σ键,故杂化方式为sp3杂化;
(3)图中,Ti的原子坐标为(1/2,1/2,1/2),Sr的原子坐标为(0,0,0),O的原子坐标为(1/2,1/2,0),(1/2,0,1/2),(0,1/2,1/2),若Ti位于顶点位置,相当于将晶胞整体沿(1/2,1/2,1/2)方向平移,对于O,(1/2,1/2,0)+(1/2,1/2,1/2)=(0,0,1/2),(1/2,0,1/2)+(1/2,1/2,1/2)=(0,1/2,0),(0,1/2,1/2)+(1/2,1/2,1/2)=(1/2,0,0),可见O占据的为棱心;Ti位于O所形成的正八面体的体心,八面体中Ti和O构成了一个等腰直角三角形,直角边长为![]() a,斜边长为
a,斜边长为![]() =
=![]() a nm=
a nm=![]() a×10-9 m。
a×10-9 m。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
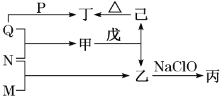
【题目】短周期元素W、X、Y、Z的原子序数依次增加。M、N、P、Q分别是这些元素形成的单质,甲、乙、丙、丁、戊是由这些元素形成的二元化合物。其中,乙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丙是一种高能燃料,其组成元素与乙相同;丁是常见的两性氧化物。上述物质的转化关系如图所示。下列说法正确的是( )
A.原子半径的大小:W<X<Y<Z
B.戊的沸点低于乙
C.丙中只含非极性共价键
D.乙可与X元素的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
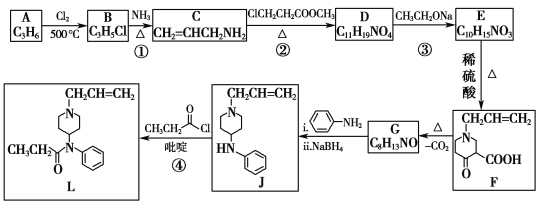
【题目】芬太尼类似物L具有镇痛作用,它的合成方法如图:
已知:
Ⅰ.![]() +Cl—R3
+Cl—R3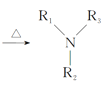 +HCl
+HCl
Ⅱ.R1COOR2+R3CH2COOR4![]()
![]() +R2OH
+R2OH
Ⅲ.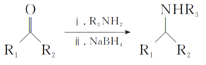 (R1、R2、R3、R4为氢原子或烃基)
(R1、R2、R3、R4为氢原子或烃基)
Ⅳ.RCH=CHR′![]() RCOOH+R′COOH,R、R′为烃基。
RCOOH+R′COOH,R、R′为烃基。
回答下列问题:
(1)A是一种烯烃,化学名称为__,其分子中最多有__个原子共面。
(2)B中官能团的名称为__、__。②的反应类型为__。
(3)③的化学方程式为__。
(4)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳原子。用星号(*)标出F中的手性碳原子__。G的结构简式为__,符合以下条件的G同分异构体有___种。
①能发生银镜反应
②结构中只含有一个环,该环结构为![]() ,环上只有一个侧链
,环上只有一个侧链
(5)已知④有一定的反应限度,反应进行时加入吡啶(一种有机碱),其作用是__。
(6)参照上述合成路线,写出以环己烯(![]() )和乙醇为起始原料制备化合物
)和乙醇为起始原料制备化合物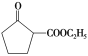 的合成路线(其他试剂任选)。___。
的合成路线(其他试剂任选)。___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中三种物质的物质的量随时间的变化曲线如下图所示。由图中数据分析,该反应的化学方程式和反应开始至2min末Z的平均反应速率为( )
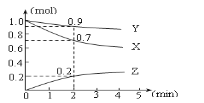
A.3X + Y ![]() 2Z;0.05mol·L-1·min-1B.2X + Y
2Z;0.05mol·L-1·min-1B.2X + Y![]() 2Z;0.1mol·L-1·min-1
2Z;0.1mol·L-1·min-1
C.X + 2Y =Z;0.1mol·L-1·min-1D.X + 3Y =2Z;0.05mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某“84”消毒液部分标签如下图所示,回答下列问题:
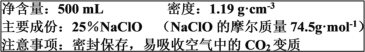
(1)NaClO变质的反应属于__________(填“氧化还原反应”或“非氧化还原反应”)
(2)计算该“84”消毒液的物质的量浓度________mol·L-1(保留小数点后一位)。
(3)某实验需用480 mL 2.0 mol·L-1NaClO的消毒液,现用NaClO固体配制。
a.需要用托盘天平称量NaClO的固体质量为________g
b.配制时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却
正确的操作顺序为:____________________________________(填序号)
(4)在配制过程中,除需要烧杯、托盘天平外还必需的仪器有______________(写两种)
(5)下列操作可能使配制溶液浓度偏低的是________
A.移液时,未洗涤烧杯内壁和玻璃棒 B.溶解后未经冷却就移液
C.移液时,有少量液体溅出 D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下发生反应:2A(?) ![]() B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小B.若正反应是放热反应,则A为气态
C.物质A一定为非气态,且正反应是吸热反应D.若向容器中充入惰性气体,则平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g)![]() 2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率为______。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志______.
A.消耗1molN2同时生成1molO2![]() 混合气体密度不变
混合气体密度不变
C.混合气体平均相对分子质量不变D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是______(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态![]() 与原平衡状态相比,此时平衡混合气中NO的体积分数______
与原平衡状态相比,此时平衡混合气中NO的体积分数______![]() 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变”![]()
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应______(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L恒容密闭容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t1 min 时达到平衡。
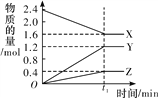
(1)请写出该反应的化学方程式:_____________________________。
(2)若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol 氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为________;在此t1 min时间内,用H2表示该反应的平均速率v(H2)为__________。下列叙述能判断该反应达到平衡状态的是________(填字母代号)。
A.容器内各气体组分的质量分数不再发生改变
B.正反应速率与逆反应速率相等
C.容器内气体的密度不再发生改变
D.混合气体的平均相对分子质量不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复合氢化物可作为储氢和固体电解质材料,在能源与材料领域得到了深入的研究。
如:①Mg(NH2)2 ②NaNH2 ③ H3N-BH3 ④NaAlH4 ⑤Li3AlH6
(1)复合氢化物升温加热可逐步分解放出氢气,理论上单位质量的上述复合氢化物其储氢能力最低的是__________(填标号)。
(2)在Mg(NH2)2和NaNH2中均存在NH2-,NH2-的空间构型为_________,中心原子的杂化方式为____________。
(3)H3N-BH3与水反应生成一种盐和H2的化学方程式:_____________________。写出基态B原子的价电子轨道表达式:__________________________。
(4)Li3AlH6晶体的晶胞参数为a=b=801.7 pm,c=945.5 pm,α=β=90°、γ=120°,结构如图所示:
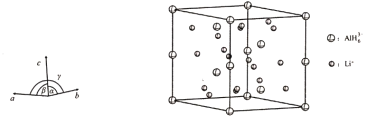
①已知AlH63-的分数坐标为(0,0,0)、(0,0,![]() ),(
),(![]() ,
,![]() ,
,![]() ),(
),(![]() ,
,![]() ,
,![]() ),(
),(![]() ,
,![]() ,
,![]() )和(
)和(![]() ,
,![]() ,
,![]() ),晶胞中Li+的个数为____________。
),晶胞中Li+的个数为____________。
②如图是上述Li3AlH6晶胞的某个截面,共含有10个AlH63-,其中6个已经画出(图中的○),请在图中用○将剩余的AlH63-画出____________。
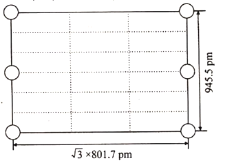
③此晶体的密度为____g·cm-3(列出计算式,已知阿伏加德罗常数约为6.02×1023mol-1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com