
ΓΨΧβΡΩΓΩΕΧ÷ήΤΎ‘ΣΥΊWΘ§XΘ§YΘ§ZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ωΦ”Θ§”…“‘…œΥΡ÷÷‘ΣΥΊΉι≥…ΒΡ“Μ÷÷Μ·ΚœΈοm‘Ύ400ΓφΆξ»ΪΖ÷ΫβΘ§ΤδΖ¥”Π ΫΈΣ3m![]() 4n+p+3q+6rΘ§nΡή Ι Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕΘ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
4n+p+3q+6rΘ§nΡή Ι Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕΘ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.‘≠Ή”ΑκΨΕΘΚW<X<Y<Z
B.ΦρΒΞ«βΜ·ΈοΒΡΈ»Ε®–‘X>Y>Z
C.WΓΔXΓΔY–Έ≥…ΒΡΜ·ΚœΈο“÷÷ΤΥ°ΒΡΒγάκ
D.mΒΡΖ÷Ϋβ≤ζΈο÷–pΈΣ―θΜ·≤ζΈοΘ§qΈΣΜΙ‘≠≤ζΈο
ΓΨ¥πΑΗΓΩD
ΓΨΫβΈωΓΩ
ΗυΨίnΡή Ι Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕΘ§nΈΣ![]() Θ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§qΈΣ
Θ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§qΈΣ![]() Θ§ΕΧ÷ήΤΎ‘ΣΥΊWΓΔXΓΔYΓΔZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ωΦ”Θ§‘ρWΈΣHΘ§XΈΣNΘ§YΈΣOΘ§ZΈΣSΘ§mΈΣ
Θ§ΕΧ÷ήΤΎ‘ΣΥΊWΓΔXΓΔYΓΔZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ωΦ”Θ§‘ρWΈΣHΘ§XΈΣNΘ§YΈΣOΘ§ZΈΣSΘ§mΈΣ![]() Θ§“‘¥ΥΖ÷ΈωΫβ¥πΓΘ
Θ§“‘¥ΥΖ÷ΈωΫβ¥πΓΘ
nΡή Ι Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ±δάΕΘ§nΈΣ![]() Θ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§qΈΣ
Θ§qΡή”ΟΤΖΚλ ‘“ΚΦλ―ιΘ§qΈΣ![]() Θ§ΕΧ÷ήΤΎ‘ΣΥΊWΓΔXΓΔYΓΔZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ωΦ”Θ§‘ρWΈΣHΘ§XΈΣNΘ§YΈΣOΘ§ZΈΣSΘ§mΈΣ
Θ§ΕΧ÷ήΤΎ‘ΣΥΊWΓΔXΓΔYΓΔZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ωΦ”Θ§‘ρWΈΣHΘ§XΈΣNΘ§YΈΣOΘ§ZΈΣSΘ§mΈΣ![]() Θ§”…‘ΣΥΊΦΑ‘≠Ή” ΊΚψΩ…÷ΣΖΔ…ζ3(NH4)2SO4
Θ§”…‘ΣΥΊΦΑ‘≠Ή” ΊΚψΩ…÷ΣΖΔ…ζ3(NH4)2SO4![]() 4NH3
4NH3![]() +N2
+N2![]() +3SO2
+3SO2![]() +6H2OΓΘ
+6H2OΓΘ
A.ΒγΉ”≤ψ‘ΫΕύΘ§‘≠Ή”ΑκΨΕ‘Ϋ¥σΘ§Ά§÷ήΤΎ¥”Ήσœρ”“‘≠Ή”ΑκΨΕΦθ–ΓΘ§‘ρ‘≠Ή”ΑκΨΕΘΚ![]() Θ§Ι A¥μΈσΘΜ
Θ§Ι A¥μΈσΘΜ
B.Ζ«Ϋπ τ–‘‘Ϋ«ΩΘ§Ε‘”Π«βΜ·Έο‘ΫΈ»Ε®Θ§‘ρΦρΒΞ«βΜ·ΈοΒΡΈ»Ε®–‘![]() Θ§Ι B¥μΈσΘΜ
Θ§Ι B¥μΈσΘΜ
C.WΓΔXΓΔY–Έ≥…ΒΡΜ·ΚœΈοΈΣœθΥα ±“÷÷ΤΥ°ΒΡΒγάκΘ§»τΈΣœθΥαοß ±¥ΌΫχΥ°ΒΡΒγάκΘ§Ι C¥μΈσΘΜ
D. 3(NH4)2SO4![]() 4NH3
4NH3![]() +N2
+N2![]() +3SO2
+3SO2![]() +6H2O÷–N‘ΣΥΊΒΡΜ·ΚœΦέ…ΐΗΏΘ§S‘ΣΥΊΒΡΜ·ΚœΦέΫΒΒΆΘ§‘ρqΈΣΜΙ‘≠≤ζΈοΘ§pΈΣ―θΜ·≤ζΈοΘ§Ι D’ΐ»ΖΘΜ
+6H2O÷–N‘ΣΥΊΒΡΜ·ΚœΦέ…ΐΗΏΘ§S‘ΣΥΊΒΡΜ·ΚœΦέΫΒΒΆΘ§‘ρqΈΣΜΙ‘≠≤ζΈοΘ§pΈΣ―θΜ·≤ζΈοΘ§Ι D’ΐ»ΖΘΜ
¥πΑΗΘΚDΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «(ΓΓΓΓ)
A.»γΆΦΩ…±μ ΨΥ°Ζ÷ΫβΙΐ≥Χ÷–ΒΡΡήΝΩ±δΜ·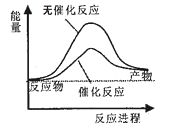
B.»τ2C(s)+O2(g)=2CO(g)ΓΓΠΛH=-221.0 kJ/molΘ§‘ρΧΦΒΡ»Φ…’»»ΈΣ110.5 kJ/mol
C.–η“ΣΦ”»»ΒΡΖ¥”Π“ΜΕ® «Έϋ»»Ζ¥”ΠΘ§≥ΘΈ¬œ¬ΡήΖΔ…ζΒΡΖ¥”Π“ΜΕ® «Ζ≈»»Ζ¥”Π
D.“―÷ΣΔώΘΚΖ¥”ΠH2(g)+Cl2(g)=2HCl(g)ΓΓΠΛH=-a kJ/molΘ§
ΔρΘΚΦϋΡήH-HΘΚb kJ/molΘ§Cl-ClΘΚc kJ/molΓΘ‘ρΕœΩΣ1 mol H-ClΦϋΥυ–ηΡήΝΩΈΣ![]() kJ
kJ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”Ο»γΆΦΥυ ΨΉΑ÷ΟΫχ––œ¬Ν– Β―ιΘ§aΓΔbΚΆc÷–ΥυΉΑ ‘ΦΝ»γœ¬±μΥυ ΨΘ§Τδ÷– Β―ιœ÷œσ”κΫα¬έΕ‘”ΠΙΊœΒ≤Μ’ΐ»ΖΒΡ «“ΜΉι «

―Γœν | a | b | c | œ÷œσ | Ϋα¬έ |
A | ±ΞΚΆ ≥―ΈΥ° | ΧΦΜ·ΗΤ | Υα–‘ | c÷–»ή“ΚΉœ…ΪΆ »Ξ | ““»≤ΨΏ”–ΜΙ‘≠–‘ |
B | ≈®―ΈΥα |
| NaBr»ή“Κ | c÷–»ή“Κ”…Έό…Ϊ±δ≥»…Ϊ |
|
C | œΓ―ΈΥα | ¥σάμ · |
| c÷–”–ΑΉ…ΪΫΚΉ¥≥ΝΒμ…ζ≥… | ΧΦΥαΒΡΥα–‘±»ΙηΥα«Ω |
D | ΝρΥα |
| ΤΖΚλ»ή“Κ | c÷–»ή“ΚΚλ…ΪΆ »Ξ |
|
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σ2FeSO4![]() Fe2O3+SO2Γϋ+SO3ΓϋΓΘœ¬Ν–”–ΙΊ≤ΌΉςΓΔΉΑ÷ΟΓΔ‘≠άμΦΑΕ‘œ÷œσΒΡ±μ ω’ΐ»ΖΒΡ «
Fe2O3+SO2Γϋ+SO3ΓϋΓΘœ¬Ν–”–ΙΊ≤ΌΉςΓΔΉΑ÷ΟΓΔ‘≠άμΦΑΕ‘œ÷œσΒΡ±μ ω’ΐ»ΖΒΡ «
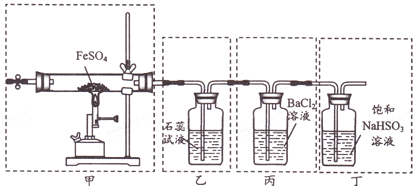
A. ”ΟΉΑ÷ΟΦΉΗΏΈ¬Ζ÷ΫβFeSO4Θ§Βψ»ΦΨΤΨΪ≈γΒΤ«Α”Πœ»œρΉΑ÷ΟΡΎΆ®“ΜΕΈ ±ΦδN2
B. ”ΟΉΑ÷Ο““Ω…Φλ―ιΖ÷Ϋβ≤ζ…ζΒΡSO2Θ§œ÷œσ « ·»ο ‘“Κœ»±δΚλΚσΆ …Ϊ
C. ”ΟΉΑ÷Ο±ϊΩ…Φλ―ιΖ÷Ϋβ≤ζ…ζΒΡSO3Θ§œ÷œσ «≤ζ…ζΑΉ…Ϊ≥ΝΒμ
D. ”ΟΉΑ÷ΟΕΓΩ…Έϋ ’Έ≤ΤχΘ§±ήΟβΈέ»ΨΜΖΨ≥
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ¥σΤχ÷–ΒΡSO2 «‘λ≥…Υα”ξΒΡ÷ς“ΣΈέ»ΨΈοΓΘΉν–¬―–ΨΩ±μΟςΘ§άκΉ”ΨßΧε[N(CH3)4]2SO4(s)Ρή”κSO2Ϋχ––»γœ¬Ω…ΡφΖ¥”ΠΘ§ ΙΤδΩ…Ρή≥…ΈΣ¬Χ…ΪΒΡSO2Έϋ ’ΦΝΘΚ
[N(CH3)4]2SO4(s)+SO2(g)![]() [N(CH3)4]2S2O6(s)
[N(CH3)4]2S2O6(s)
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A.[N(CH3)4]+÷–÷ΜΚ§Ι≤ΦέΦϋ
B.ΗΟΖ¥”Π÷–Θ§SO2Ής―θΜ·ΦΝ
C.SO2Τ·ΑΉΤΖΚλ «άϊ”ΟΤδ«Ω―θΜ·–‘
D.ΟΩΈϋ ’±ξΉΦΉ¥Ωωœ¬ΒΡSO211.2LΘ§…ζ≥…15.4g[N(CH3)4]2S2O6
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σœ¬Ν–»»Μ·―ßΖΫ≥Χ ΫΘΚ
Θ®1Θ©CH3COOH(l)+2O2(g) == 2CO2(g)ΘΪ2H2O(l) ΠΛH1ΘΫΘ≠870.3 kJΓΛmol-1
Θ®2Θ©C(s)+ O2(g) == CO2(g) ΓςH2ΘΫΘ≠393.5 kJmol-1
Θ®3Θ©H2(g) +![]() O2(g) == H2O(l) ΓςH3ΘΫΘ≠285.8kJΓΛmol-1
O2(g) == H2O(l) ΓςH3ΘΫΘ≠285.8kJΓΛmol-1
‘ρΖ¥”Π2C(s)+2H2(g) +O2(g) == CH3COOH(l)ΒΡΓςHΈΣΘ® Θ©
A. Θ≠488.3 kJΓΛmol-1 B. Θ≠244.15 kJΓΛmol-1 C. +488.3 kJΓΛmol-1 D. +244.15 kJΓΛmol-1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”Ά÷§ «”Ά”κ÷§ΖΨΒΡΉή≥ΤΘ§Υϋ «Εύ÷÷ΗΏΦΕ÷§ΖΨΥαΒΡΗ ”ΆθΞΓΘ”Ά÷§Φ» «÷Ί“Σ ≥Έο,”÷ «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΓΘ”Ά÷§ΒΡ“‘œ¬”ΟΆΨ”κΤδΚ§”–ΒΡΧΦΧΦ≤Μ±ΞΚΆΦϋ(![]() )”–ΙΊΒΡ «
)”–ΙΊΒΡ «
A. “¬Ζΰ…œΒΡ”Ά÷§Ω…”ΟΤϊ”Άœ¥»Ξ
B. ΝΩ…ψ»κ”Ά÷§,”–άϊ”Ύ»ΥΧεΈϋ ’Εύ÷÷÷§»ή–‘Έ§…ζΥΊΚΆΚζ¬ή≤ΖΥΊ
C. ÷≤Έο”ΆΆ®Ιΐ«βΜ·Ω…“‘÷Τ‘λ÷≤ΈοΡΧ”Ά(»Υ‘λΡΧ”Ά)
D. ÷§ΖΨ «”–ΜζΧεΉι÷·άο¥Δ¥φΡήΝΩΒΡ÷Ί“ΣΈο÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩx molΒΡΧζ¬ΝΚœΫπΆξ»Ϊ»ή”Ύ1LΡ≥œΓœθΥαΚσΘ§…ζ≥…ΝΥy molΒΡNO(ΈόΤδΥϊΜΙ‘≠≤ζΈο).‘ρΙΊ”ΎΗΟΖ¥”ΠΒΡœ¬Ν–ΥΒΖ®÷–Θ§≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.‘ΎΗΟΖ¥”Π÷–Θ§œθΥαΦ»œ‘―θΜ·–‘Θ§”÷œ‘Υα–‘
B.ΗυΨίΧβ÷–ΥυΗχΧθΦΰΘ§ΈόΖ®ΦΤΥψ≥ωœθΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»
C.≤ΈΦ”Ζ¥”ΠΒΡœθΥαΒΡΈο÷ ΒΡΝΩΈΣ4y mol
D.»τΫΪ…ζ≥…ΒΡNO”κO2ΜλΚœ»ή”ΎΥ°±ΜΆξ»ΪΈϋ ’Θ§–η±ξΉΦΉ¥Ωωœ¬O2ΒΡΧεΜΐ «11.2y L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œΘ§Ά®≥Θ≤…”ΟΒγΫβΖ®¥ΠάμΥα–‘ΖœΥ°÷–ΒΡ![]() Θ§ΉΑ÷Ο Ψ“βΆΦ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
Θ§ΉΑ÷Ο Ψ“βΆΦ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
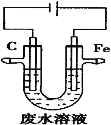
A. ·ΡΪΦΪ…œΖΔ…ζ―θΜ·Ζ¥”Π
B.―τΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ![]()
C.≥ΐ»Ξ![]() ΒΡΖ¥”ΠΘΚ
ΒΡΖ¥”ΠΘΚ![]()
D.ΥφΉ≈ΒγΫβΒΡΫχ––Θ§ ·ΡΪΦΪΗΫΫϋΒγΫβ÷ »ή“ΚΒΡpHΜαΦθ–Γ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com