
【题目】下列离子方程式正确的是
A.向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O
B.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2=Fe3++2H2O
C.Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.向含 0.5 mol的FeBr2溶液中通入13.44L(标准状况下)Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-
【答案】D
【解析】
A.硝酸具有强氧化性,向稀HNO3中滴加Na2SO3溶液的离子反应为2NO3-+3SO32-+2H+=3SO42-+2NO↑+H2O,故A错误;
B.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液的离子反应为2Fe2++2H++H2O2═2Fe3++2H2O,故B错误;
C.Mg(HCO3)2溶液中加入过量石灰水反应生成氢氧化镁、碳酸钙和水,反应的离子方程式为Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓,故C错误;
D.13.44L(标准状况下)Cl2的物质的量为![]() =0.6mol,向含0.5mol的FeBr2溶液中通入0.6molCl2,亚铁离子全被氧化,溴离子部分被氧化,反应的离子方程式为10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-,故D正确;
=0.6mol,向含0.5mol的FeBr2溶液中通入0.6molCl2,亚铁离子全被氧化,溴离子部分被氧化,反应的离子方程式为10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如右所示。下列关于分枝酸的叙述正确的是

A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸分子中含2mol—OH(羟基)
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X由三种元素(其中一种是第四周期元素)组成,现进行如下实验:

已知:气体A在标准状况下密度为0.714 g·L-1;碱性溶液焰色反应呈黄色。
(1)X中非金属元素的名称为__________,X的化学式__________。
(2)X与水反应的化学方程式为_________。
(3)化合物Y由X中金属元素和第四周期元素构成,设计实验证明Y的晶体类型__________。
(4)补充焰色反应的操作:取一根铂丝,________,蘸取待测液灼烧,观察火焰颜色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸的电离方程式为![]()
![]()
![]() +H+,其Ka=6.25×10-5,苯甲酸钠(
+H+,其Ka=6.25×10-5,苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,H2CO3的Ka1=4.17×l0-7,Ka2=4.90×l0-11。在生产碳酸饮料的过程中,除了添加NaA外, 还需加压充入CO2气体。下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,H2CO3的Ka1=4.17×l0-7,Ka2=4.90×l0-11。在生产碳酸饮料的过程中,除了添加NaA外, 还需加压充入CO2气体。下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
A. H2CO3的电离方程式为 H2CO3![]() 2H++CO32-
2H++CO32-
B. 提高CO2充气压力,饮料中c(A-)不变
C. 当pH为5.0时,饮料中 =0.16
=0.16
D. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在用稀硫酸与过量的锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是___________________;并用简单的装置图来表明你所阐述的理由______________________________;
(2)要加快上述实验中气体产生的速率,还可采取的措施有_______________;
(3)下列物质的加入能减慢氢气生成速率但不影响生成氢气的体积的是_____
A.加入碳酸钠溶液 B.加入硫酸钠溶液
C.加入硝酸钠溶液 D.加入醋酸钠溶液
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到 6 个盛有过量 Zn 粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
混合溶液实验 | 1 | 2 | 3 | 4 | 5 | 6 |
4mol·mol-1H2SO4/mL | 40 | V1 | V2 | V3 | V4 | V5 |
饱和 CuSO4 溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V6、V8 分别是_____________;
②该同学最后得出的结论为:当加入少量 CuSO4 溶液时,生成氢气的速率会大大提高,随着加入的 CuSO4 溶液增多时,生成氢气的速率会______(填加快、减慢或不变)。理由___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
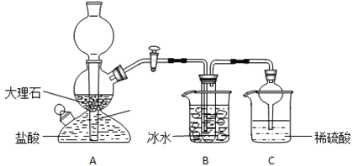
(1)A装置中所发生反应的离子方程式为:_________________。C装置中稀硫酸的作用为:________________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为________________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 ______装置____之间(填写字母)连接一个盛有_________ 的洗气装置,其作用是___________
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结论:______________。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL、浓度均为0.1mol·L-1的氢氧化钠溶液、氨水中分别滴加0.1mol·L-1盐酸,溶液导电性如图所示(已知:溶液导电性与离子浓度相关)。下列说法正确的是

A.a点溶液pH=11
B.曲线1中c与e之间某点溶液呈中性
C.c点溶液中:c(H+)=c(OH-)+c(N3H·H2O)
D.在a、b、c、d、e中,水电离程度最大的点是d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基烯酸酯在碱性条件下能快速聚合为 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:

已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;

回答下列问题:
(1)A的化学名称为____________。
(2)G的结构简式为________________,G中的含氧官能团是________________。(填官能团名称)
(3)由B生成C的反应类型为_______________,由C生成D的反应类型为_____________。
(4)由E生成F的化学方程式为________________________________。
(5)H的同分异构体中,含有酯基,能发生银镜反应、核磁共振氢谱之比是1:1:3的同分异构体结构简式_____________________________________________。(写两种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,11.2LCl2溶于水生成Cl-的数目为0.5NA
B.常温常压下,3.4g羟基(-OH)所含的电子数目为1.8NA
C.等物质的量的A1分别与足量盐酸和NaOH溶液反应,转移的电子数均为3NA
D.25℃时,1LpH=8的CH3COONa溶液中,水电离出的OH-数目为10-8NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com