
【题目】在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
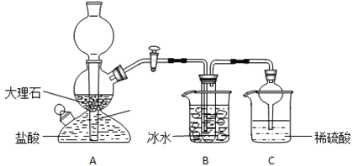
(1)A装置中所发生反应的离子方程式为:_________________。C装置中稀硫酸的作用为:________________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为________________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 ______装置____之间(填写字母)连接一个盛有_________ 的洗气装置,其作用是___________
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结论:______________。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为__________。
【答案】CaCO3+2H+=Ca2++CO2↑+H2O 吸收从B装置中的试管内逸出的氨气,减少对环境的污染 温度越低,碳酸氢钠的溶解度越小,便于析出 A B 饱和NaHCO3溶液 除去CO2中混有的HCl气体 取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则晶体不是NH4HCO3 70%
【解析】
A装置是制备二氧化碳气体的装置;B装置中的试管内是溶有氨和氯化钠的饱和溶液,氨水易挥发,C装置是尾气处理装置,据此分析解答。
(1)A装置是制取二氧化碳气体的装置,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O;C装置稀硫酸是尾气处理装置吸收挥发出来的的氨气,防止污染环境,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;吸收从B装置中的试管内逸出的氨气,减少对环境的污染;
(2)B装置中的试管内是溶有氨和氯化钠的饱和溶液,通入二氧化碳气体会发生反应生成碳酸氢钠和氯化铵,依据表格数据分析可知温度越低,碳酸氢钠的溶解度越小,所以温度越低,越有利于碳酸氢钠的晶体析出,故答案为:温度越低碳酸氢钠溶解度越小,便于析出;
(3)盐酸易挥发,制得的二氧化碳气体中含有氯化氢气体,通入后和氨气反应不能生成碳酸氢钠,所以得不到碳酸氢钠晶体,需要在A与B之间加一个洗气装置,用饱和碳酸氢钠溶液除去二氧化碳中的氯化氢气体,故答案为:A;B;饱和NaHCO3溶液;除去CO2中混有的HCl气体;
(4)碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,反应为:2NaHCO3 ![]() Na2CO3+H2O+CO2↑,有白色固体碳酸钠剩余,碳酸氢铵(NH4HCO3)受热分解,生成氨气(NH3)、二氧化碳和水,反应的化学方程式为:NH4HCO3
Na2CO3+H2O+CO2↑,有白色固体碳酸钠剩余,碳酸氢铵(NH4HCO3)受热分解,生成氨气(NH3)、二氧化碳和水,反应的化学方程式为:NH4HCO3 ![]() NH3↑+CO2↑+H2O,无固体剩余,所以判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体的方法为:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则晶体不是NH4HCO3,故答案为:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则晶体不是NH4HCO3;
NH3↑+CO2↑+H2O,无固体剩余,所以判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体的方法为:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则晶体不是NH4HCO3,故答案为:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则晶体不是NH4HCO3;
(5)饱和食盐水中含NaCl的质量为5.85g,依据化学方程式计算NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3(晶体),理论得到碳酸氢钠质量为8.4g。实验后得到干燥的NaHCO3晶体的质量为5.88g,则碳酸氢钠的产率=![]() ×100%=70%,故答案为:70%。
×100%=70%,故答案为:70%。


科目:高中化学 来源: 题型:
【题目】阿克他利M(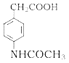 )是一种抗风湿性关节炎药物,其合成路线如图:
)是一种抗风湿性关节炎药物,其合成路线如图:
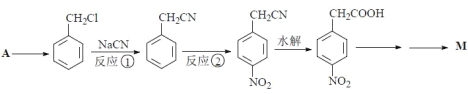
完成下列填空:
(1)反应①的反应类型为_____。
(2)反应②所用的试剂为_____。
(3)![]() 的相邻同系物可以通过两步反应制得苯乙醛。请写出第二步反应的化学方程式_____。苯乙醛的同类别同分异构体有_____种。
的相邻同系物可以通过两步反应制得苯乙醛。请写出第二步反应的化学方程式_____。苯乙醛的同类别同分异构体有_____种。
(4)写出由对硝基苯乙酸(![]() )得到对硝基苯乙酸乙酯的化学方程式_____。
)得到对硝基苯乙酸乙酯的化学方程式_____。
(5)A的分子式为C7H8,写出由A合成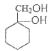 的合成路线_____。
的合成路线_____。
(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物在生产和生活中有重要意义。海水中CO2的吸收能力取决于溶解的碳酸盐和硼酸盐生成的CO32-和B(OH)4-浓度。已知:298K时,H3BO3+H2O![]() H++B(OH)4-,Ka=5.7×10-10,碳酸的电离平衡常数:Ka1=4.3×10-7;Ka2=5.6×10-11
H++B(OH)4-,Ka=5.7×10-10,碳酸的电离平衡常数:Ka1=4.3×10-7;Ka2=5.6×10-11
(1)298K时,相同浓度的碳酸钠溶液和硼酸钠溶液,pH较大的是_______溶液。
(2)少量CO2与B(OH)4-反应的离子方程式为___________。
(3)采用高温熔融混合碳酸盐LiaNabKcCO3作电解质吸收并电解CO2制得无定型炭是CO2 资源化利用的一种新途径。此法的阴极电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 △H=+88.6kJ/mol
△H=+88.6kJ/mol
则M与N相比,较稳定的是____。
(2)已知CH3OH⑴的燃烧热为726.5kJ·mol-1,CH3OH(l) + l/2O2(g)=CO2(g)+2H2(g)
△H=-akJ·mol-1,则a_______726.5 (填“>”、“<”或 “=”)
(3)将Cl2和H2O(g)通过灼热的木炭层,生成HCl和CO2。当有1mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:______________________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, 4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则27g铝粉完全反应放出的热量为_____________。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ mol-1
CO(g)+l/2O2(g)=CO2(g) △H=-283. 0kJ mol-1
C (石墨)+O2(g)=CO2(g) △H=-393.5kJ mol-1
则4Fe (s)+3O2(g) =2Fe2O3 (s) △H=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O
B.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2=Fe3++2H2O
C.Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.向含 0.5 mol的FeBr2溶液中通入13.44L(标准状况下)Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH﹣的物质的量浓度分别为A和B,则A和B的关系为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由芳香烃A制备M(可用作消毒剂、抗氧化剂、医药中间体)的一种合成路线如下:
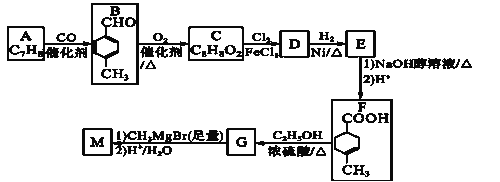
已知: R1COOR2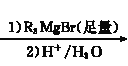
请回答:
(1)A的结构简式为_____;D中官能团的名称为 ___ 。
(2)由D生成E的反应类型为 ____;G的分子式为 ___ 。
(3)由E与足量氢氧化钠的乙醇溶液反应的化学方程式为 ____。
(4)M的结构简式为 ____。
(5)芳香化合物H为C的同分异构体,H既能发生银镜反应又能发生水解反应,其核磁共振氢谱有4组吸收峰。写出符合要求的H的一种结构简式 ______。
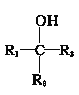
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备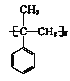 的合成路线_____。
的合成路线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表(已知:偏铝酸钡易溶于水)。以下推断正确的是


A. OA段产生的沉淀为BaSO4和Fe(OH)3
B. 据图计算原溶液中c(Cl-)=c(SO42-)
C. AB段可能发生的反应是:2SO42-+ 2Ba2++ Al3++3OH-=2BaSO4+Al(OH)3
D. C点溶液呈碱性的原因是AlO2-水解,其离子方程式为:AlO2-+2H2O=Al(OH)3+OH一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅氧化还原液流电池作为一种新型铅电池,具有一定的应用前景,正在逐渐成为电化学储能领域的一个研究热点。该电池以酸性甲基磺酸铅溶液为电解液,简化的工作原理如图所示,下列说法正确的是( )

A.放电时,H+经过循环泵向Pb电极移动
B.放电时,正极反应式为PbO2+4H++2e-=Pb2++2H2O
C.充电时,阴极反应式为2H++2e-=H2↑
D.该电解液可用稀H2SO4替代,放电效果相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com