
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��COת��ΪCO2���Ȼ�ѧ����ʽΪ2CO��g��+O2��g���T2CO2��g����H=-566 kJ?mol-1 | ||
B��COȼ���ȵ��Ȼ�ѧ����ʽΪCO��g��+
| ||
| C�����ȷ�Ӧ������Ҫ���Ȳ��ܽ��У������ȷ�Ӧһ����Ҫ���Ȳ��ܽ��� | ||
| D��1mol H2��ȫȼ������1mol Һ̬ˮ���ų�����������242 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
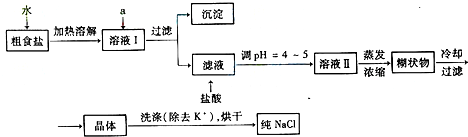
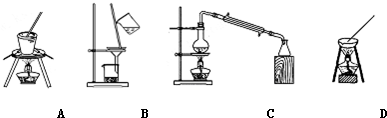
| ��ѧʽ | CaCO3 | CaSO4 | Ca��OH��2 | MgCO3 | Mg��OH��2 |
| Ksp | 2.8��10-9 | 9.1��10-6 | 1.0��10-4 | 3.5��10-5 | 1.6��10-11 |
| 0�� | 10�� | 20�� | 30�� | 40�� | 50�� | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | ||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
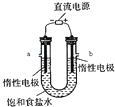
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
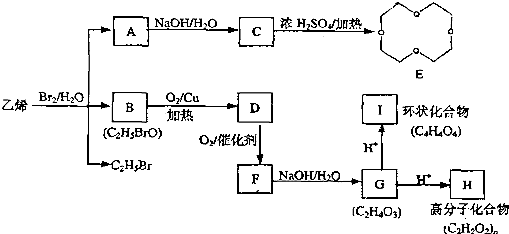
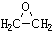 ���Ľṹ�ɼ�дΪ
���Ľṹ�ɼ�дΪ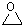 ����E�ķ���ʽ��
����E�ķ���ʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
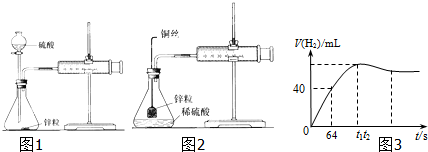
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ʵ����� | 1 | 2 | 3 | 4 |
| ����Na2S2O3����Һ��mL�� | 25.00 | 25.02 | 26.20 | 24.98 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Al-Mg�Ͻӹ�����ʹ�õı�����ΪN2 |
| B����ҵ�Ͽɲ��õ������NaCl�ķ����Ʊ������� |
| C����0.5molN2��1.5molH2����һ�ܱ������г�ַ�Ӧ���ų�����19.6KJ������Ȼ�ѧ����ʽΪN2��g��+3 H2��g��?2NH3��g����H=-39.2 KJ?mol-1 |
| D����֪��2H2��g��+O2��g��?2H2O��g����H=-486 KJ?mol-1����H2��ȼ���ȡ�HΪ-243 KJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| M |
| M |
| ѡ �� | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | NaOH | Na2SO3 | NaHSO3 | SO2 |
| C | Al2O3 | NaAlO2 | Al��OH��3 | NaOH |
| D | Mg | C | CO | CO2 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com