
| c(CH3COO-) |
| c(Na+) |
| A、只有①③ | B、①③④ |
| C、②④⑤⑥ | D、③④⑥ |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |
| c(CH3COO-) |
| c(Na+) |


科目:高中化学 来源: 题型:
| A、甲苯能使酸性KMnO4溶液褪色,而甲基环己烷不能使酸性KMnO4溶液褪色 |
| B、乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应 |
| C、苯酚与溴水可以直接反应,而苯与液溴反应则需要铁作催化剂 |
| D、苯酚可以与NaOH反应,而乙醇不能与NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 改变的条件 | 生成NH3的速率 |
| ① | 升高温度 | |
| ② | 增大N2的浓度 | |
| ③ | 使用催化剂 | |
| ④ | 压缩体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
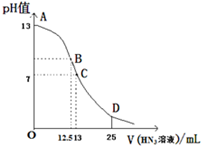 纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).
纯叠氮酸(HN3)是无色液体,对热十分稳定,但受撞击就爆炸,常用作引爆剂,如图为常温下向25ml0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1的HN3溶液过程中溶液的pH的变化曲线(溶液混合时体积变化忽略不计).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 H++2e-═H2↑ |
| B、O2+2H2O+4e-═4OH- |
| C、Fe-2e-═Fe2+ |
| D、4 OH--4e-═2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com