
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。……
请回答下列问题(提示B分液漏斗中为浓氨水,滴入烧瓶可产生氨气):
(1)装置的连接顺序是:(a)接________,________接________;(b)接________

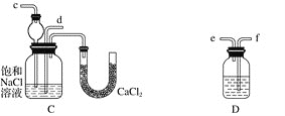
(2)A中常选用的固体反应物为______________;D中应选用的液体为________________(填化学式)。
(3)第二步骤中必须先让__________装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是______________________________,C中广口瓶内产生固体的总化学方程式为______________________ 。
(5)在第四步中分离NH4Cl晶体的操作是____________________(填操作名称);其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验证明所得固体的成分中含有Na+,简要写出操作和现象____________________________________。
【答案】f e d c CaCO3 NaHCO3 B 防倒吸 H2O+CO2+NH3+NaCl===NaHCO3↓+NH4Cl 过滤 用一根洁净的铂金丝蘸取少量固体进行焰色反应,若火焰呈黄色,则含有Na+
【解析】
(1)根据装置A制取CO2,装置B制取NH3,装置D除去二氧化碳中的HCl,二氧化碳与氨气通入C中应防止倒吸,据此分析连接仪器装置;
(2)根据A装置是制备二氧化碳气体,二氧化碳气体中含有氯化氢气体分析解答;
(3)氨气易溶于水,二氧化碳在水中的溶解度较小,据此判断;
(4)根据氨气极易溶于水判断C中用球形干燥管的原因;C中广口瓶内产生固体NaHCO3,依据侯氏制碱法原理书写方程式;
(5)分离氯化铵沉淀通常用过滤操作,检验钠离子一般用焰色反应分析解答。
(1)根据题干信息可知装置A产生CO2,装置B产生NH3,由于生成的二氧化碳中含有氯化氢会干扰实验,所以装置D除去二氧化碳中的HCl,氨气极易溶于水,氨气通入C中应防止倒吸,则b接c,a接f、e接d;
(2)A装置是制备二氧化碳气体的反应,所以固体为CaCO3,生成的二氧化碳气体中含有氯化氢,若不除去碳酸氢钠难以形成,所以应该用饱和碳酸氢钠溶液除去;
(3)候氏制碱方法是利用氨气溶解性大极易溶解于水,二氧化碳气体水中溶解性较小,实验时饱和食盐水中先通入氨气,再通入二氧化碳气体,因此实验操作过程中,应让B装置先发生反应;
(4)氨气极易溶于水,用直导管向饱和氯化钠溶液中通入氨气,容易发生倒吸,C中用球形干燥管球形部分液面上升慢起缓冲作用,可以防止倒吸;侯氏制碱法,也称为联合制碱法,化学反应原理是用氨气和二氧化碳与氯化钠饱和溶液反应生成碳酸氢钠,然后加热碳酸氢钠制取碳酸钠,所以C中广口瓶内产生固体的总化学方程式为H2O+CO2+NH3+NaCl=NaHCO3↓+NH4Cl;
(5)第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出,分离固体和液体用过滤的方法。证明所得固体的成分中含有Na+的实验操作和现象为:用一根洁净的铂金丝蘸取少量固体进行焰色反应,若火焰呈黄色,则含有Na+。


科目:高中化学 来源: 题型:
【题目】T0℃时,在2 L的密闭容器中发生反应:X(g)+Y(g)![]() Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是( )
图a 图b
图b
A.该反应的正反应是吸热反应
B.T1℃时,若该反应的平衡常数K =50,则T1<T0
C.图a中反应达到平衡时,Y的转化率为37.5%
D.T0℃,从反应开始到平衡时:v(X)=0.083 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒的味道主要来自于辣椒素类化合物,辣椒素F的合成路线如下
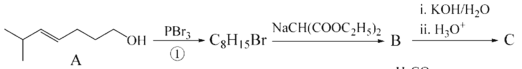
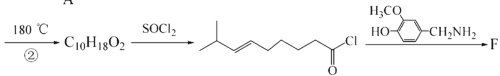
(1)化合物A中官能团的名称是____________。
(2)反应①的类型为_______________。已知某有机反应原理为![]() ,写出化合物C的结构简式_________。化合物C可与C2H6O2 (核磁共振氢谱显示2种峰,峰面积比1∶2)按1∶1反应形成环状化合物,写出此反应的化学反应方程式______________。
,写出化合物C的结构简式_________。化合物C可与C2H6O2 (核磁共振氢谱显示2种峰,峰面积比1∶2)按1∶1反应形成环状化合物,写出此反应的化学反应方程式______________。
(3)已知反应2的另一生成物为CO2,请写出该反应的化学方程式___________,该反应类型为________。
(4)写出满足下列条件的同分异构体有_______种。
①含有5个碳原子②与上述流程中产物C10H18O2含有相同种类和数目的官能团
(5)写出由乙烯合成正丁酸的合成路线________(其他试剂任选,写出必要的试剂及反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的容器中加入一定量的A和B,发生反应∶2A(g)+B(g)![]() 2C(g), 在相同时间内,测得不同温度下A的转化率如下表所示,下列说法正确的是
2C(g), 在相同时间内,测得不同温度下A的转化率如下表所示,下列说法正确的是
温度/°C | 100 | 200 | 300 | 400 | 500 |
转化率 | 30% | 75% | 75% | 50% | 18% |
A.该反应随着温度升高,反应速率先变大后变小
B.200°C,A的转化率为75%时,反应达到平衡状态
C.当单位时间内生成n mol B的同时消耗2n molC时,反应达到平衡状态
D.400°C时,B的平衡浓度为0.5 mol/L,则该反应的平衡常数K=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作,回答问题:
(1)将在空气中久置的铝箔放在酒精灯火焰上加热,观察到的现象是_________________,上述变化的原因是______________。
(2)将用砂纸仔细打磨过的铝箔放在酒精灯火焰上加热,观察到的现象是_________________,上述变化的原因是____________________。
(3)将铝箔在氧气中点燃,观察到的现象是__________,反应的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按要求填空
①4.8gO3和0.2molCH4,在同温同压下的体积之比是____。②同温同压下,NH3和H2S气体的密度比是___;③同温同体积下,同质量的NH3和H2S气体的压强之比是___。
(2)写出下列物质在水中的电离方程式:
NaHSO4:___
H2SO4:___
NaHCO3:___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g)![]() 3Z(g) △H=-a kJ·mol-1(a>0)。下列说法不正确的是
3Z(g) △H=-a kJ·mol-1(a>0)。下列说法不正确的是
A. 达到化学平衡状态时,反应放出的总热量可能达到akJ
B. 升高反应温度,逆反应速率增大,正反应速率减小
C. 达到化学平衡状态时,X、Y、Z的浓度不再发生变化
D. 0.1 mol X和0.2 molY充分反应生成Z的物质的量一定小于0.3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙炔和乙醛为原料制备1,3-丁二烯的合成路线如图所示:下列说法不正确的是
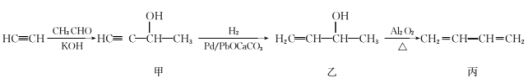
A.甲、乙两种有机化合物中均含有手性碳原子
B.CH3CHO既可被氧化为CH3CH2OH,又可被还原为CH3COOH
C.丙(1,3-丁二烯)形成的高聚物的结构简式为![]()
D.合成路线中涉及到的反应类型有加成反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+![]() O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=
O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
③H2S(g)+![]() O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为
A.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)B.ΔH4=
(ΔH1+ΔH2-3ΔH3)B.ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)D.ΔH4=
(ΔH1+ΔH2-3ΔH3)D.ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com