
| A、原子半径:丁>丙>甲 |
| B、单质的还原性:丁>丙>甲 |
| C、甲、乙、丙的氧化物为共价化合物 |
| D、乙、丙、丁的最高价氧化物对应的水化物相互反应 |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
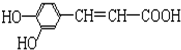
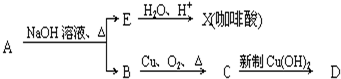
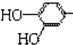 结构;②能发生水解反应;R的结构简式为
结构;②能发生水解反应;R的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入过量的Ba(OH)2溶液时:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓ |
| B、溶液恰好呈中性时:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C、SO42-离子恰好完全沉淀时:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D、明矾与Ba(OH)2按物质的量比1:1反应时:Al3++SO42-+Ba2++3OH-→Al(OH)3↓+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、Ca2+、ClO-、NO-3 |
| B、Na+、K+、SiO2-3、Cl- |
| C、K+、Cr2O2-7、CH3CHO、SO2-4 |
| D、Al3+、NH+4、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
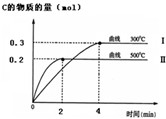 (1)已知在25℃时:①2CO (s)+O2(g)═2CO2(g)△H1=-566KJ/mol
(1)已知在25℃时:①2CO (s)+O2(g)═2CO2(g)△H1=-566KJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2 |
| B、IO3- |
| C、MnO4- |
| D、HNO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com