
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是( )
A.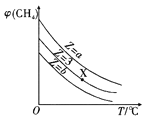 表示一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)
表示一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)平衡时φ(CH4)的体积分数与Z(Z=
CO(g)+3H2(g)平衡时φ(CH4)的体积分数与Z(Z=![]() )和T(温度)的关系,则该反应的焓变△H>0,且b>3>a
)和T(温度)的关系,则该反应的焓变△H>0,且b>3>a
B.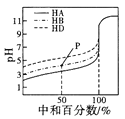 表示室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线,可以看出三种酸的电离常数关系为KHA>KHB>KHD,且滴定至P点时,溶液中:c(HB)>c(Na+)>c(B- )>c(H+)>c(OH-)
表示室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线,可以看出三种酸的电离常数关系为KHA>KHB>KHD,且滴定至P点时,溶液中:c(HB)>c(Na+)>c(B- )>c(H+)>c(OH-)
C.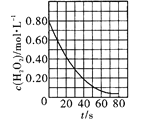 是室温下H2O2催化分解放出氧气的反应中c(H2O2)随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
是室温下H2O2催化分解放出氧气的反应中c(H2O2)随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
D.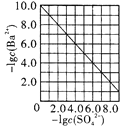 是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明溶液中c(SO42-)越大c(Ba2+)越小
是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明溶液中c(SO42-)越大c(Ba2+)越小
【答案】B
【解析】
A.升高温度,甲烷的体积分数减小,说明升高温度平衡正向移动,则该反应的焓变△H>0;起始![]() =Z,Z越小,说明甲烷相对越多,达到平衡时甲烷的含量越多,则Z的大小为a<3<b,故A正确;
=Z,Z越小,说明甲烷相对越多,达到平衡时甲烷的含量越多,则Z的大小为a<3<b,故A正确;
B.相同物质的量浓度的一元酸,酸的pH越小,氢离子浓度越大,说明酸的电离程度越大,则该酸的酸性越强,其电离平衡常数越大,根据图知,未加NaOH溶液时,pH:HA<HB<HD,说明酸的电离程度HA>HB>HD,则KHA>KHB>KHD;中和50%即P点,溶液中溶质为等物质的量浓度的酸(HB)和盐(NaB),由图可知溶液呈酸性,则c(H+)>c(OH-),且酸的电离程度大于酸根离子水解程度;①NaB完全电离:NaB=Na++B-,这一步的c(B-)=c(Na+),②HB少部分电离:HBH++B-,则c(HB)>c(H+),③NaB少部分水解:B-+H2OHB+OH-,由于酸的电离程度大于盐的水解程度,则HB电离产生的B-相对NaB水解消耗的B-多,所以c(B-)>c(Na+),由于HB电离消耗得多,水解生成的HB少,所以c(Na+)>c(HB),则c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-),故B错误;
C.反应物浓度越大,反应速率越大,根据图知,随着时间的进行,双氧水浓度逐渐降低,则随着反应的进行H2O2分解速率逐渐减小,故C正确;
D.温度不变,溶度积常数不变,Ksp(BaSO4)=c(Ba2+)·c(SO42-),c(Ba2+)与c(SO42-)成反比,则c(SO42-)越大c(Ba2+)越小,故D正确;
故答案为B。


科目:高中化学 来源: 题型:
【题目】现有如下3个热化学方程式:
H2(g)+![]() O2(g)=H2O(g) ΔH1= -a kJ·mol-1①
O2(g)=H2O(g) ΔH1= -a kJ·mol-1①
H2(g)+![]() O2(g)=H2O(l) ΔH2= -b kJ·mol-1②
O2(g)=H2O(l) ΔH2= -b kJ·mol-1②
2H2(g)+O2(g)=2H2O(l) ΔH3= -c kJ·mol-1③
则由下表所列的原因能推导出后面结论的是( )
选项 | 原因 | 结论 |
A | H2的燃烧是放热反应 | a、b、c均大于零 |
B | ①和②中物质的化学计量数均相同 | a=b |
C | ①和③中H2O的状态不同,化学计量数不同 | a、c不会有任何关系 |
D | ③的化学计量数是②的2倍 | ΔH2<ΔH3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中正确的是( )
A. 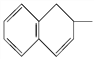 中所有碳原子可能在同一平面上
中所有碳原子可能在同一平面上
B. 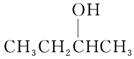 的命名为2-甲基-1-丙醇
的命名为2-甲基-1-丙醇
C. 乙烯、聚氯乙烯和苯分子中均含有碳碳双键
D. C4H8属于烯烃的同分异构体共有4种(含顺反异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)浓度均为0.01 mol·L-1的8种溶液:①HNO3 ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤NaOH
⑥CH3COONa ⑦KCl ⑧NH4Cl,这些溶液pH由小到大的顺序是(填写编号)_________。
(2)pH=2的某酸HnA(An+为酸根)与pH=12的某碱B(OH)m混合,恰好反应生成正盐,混合液pH=8。
①反应生成的正盐的化学式为________。
②该盐中____离子一定能水解,其第一步水解的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A是来自石油的基本化工原料。A是气态烃,B和D是生活中两种常见的有机物,F是高分子化合物,相互转化关系如图所示.
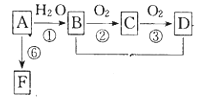
(1)A分子的电子式是___;
(2)乙醇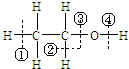 在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
(3)写出下列反应的化学方程式:
①B→C:___;
②A→B:___;
③比A多一个碳原子的 A的同系物发生加聚反应的方程式:___。
Ⅱ.苯和苯的同系物在化工生产中应用十分广泛。
(1)分子式为C8H10为的苯的同系物的同分异构有___种;
(2)CH4、CH2=CH2、C6H6等质量时消耗氧气最多的气态烃是___(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CO2中,Mg燃烧生成MgO和C。下列说法正确的是( )
A. 元素C的单质只存在金刚石和石墨两种同素异形体
B. Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C. 在该反应条件下,Mg的还原性强于C的还原性
D. 该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取冰晶石(Na3AlF6)的化学方程式如下:2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O,根据题意完成下列填空:
(1) 在上述反应的反应物和生成物中,属于非极性分子的电子式______,属于弱酸的电离方程式______。
(2)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是______(选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为______。
(4) Na2CO3俗称纯碱,属于______晶体。工业上制取纯碱的原料是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+2B2(g)![]() 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol A2、2molB2 | 2molAB3 | 2mol AB3 |
反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时AB3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是( )
A.v甲=v丙B.c乙<c丙C.a甲 +a乙<1D.K乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com