
【题目】Ⅰ.A是来自石油的基本化工原料。A是气态烃,B和D是生活中两种常见的有机物,F是高分子化合物,相互转化关系如图所示.
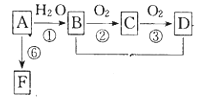
(1)A分子的电子式是___;
(2)乙醇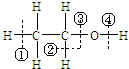 在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
(3)写出下列反应的化学方程式:
①B→C:___;
②A→B:___;
③比A多一个碳原子的 A的同系物发生加聚反应的方程式:___。
Ⅱ.苯和苯的同系物在化工生产中应用十分广泛。
(1)分子式为C8H10为的苯的同系物的同分异构有___种;
(2)CH4、CH2=CH2、C6H6等质量时消耗氧气最多的气态烃是___(填分子式)。
【答案】![]() ②④ 2CH3CH2OH+O2
②④ 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH2=CH2 + H2O
2CH3CHO+2H2O CH2=CH2 + H2O ![]() CH3CH2OH n
CH3CH2OH n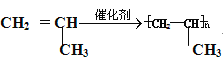 4种 CH4
4种 CH4
【解析】
Ⅰ.A是来自石油的基本化工原料,A是气态烃,B和D是生活中两种常见的有机物,A与水反应生成B,B连续氧化生成D,B为醇,D为羧酸,则A为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,CH3CHO进一步氧化生成D为CH3COOH,CH2=CH2发生加聚反应生成高聚物F为聚乙烯,据此解答;
Ⅱ. (1)分子式为C8H10的芳香烃,分子中含有1个苯环,其不饱和度=![]() =4,故侧链为烷基,若有1个侧链,为-CH2-CH3;若有2个侧链,为-CH3,有邻、间、对三种,据此解答;
=4,故侧链为烷基,若有1个侧链,为-CH2-CH3;若有2个侧链,为-CH3,有邻、间、对三种,据此解答;
(2)等质量的各烃完全燃烧,烃中H元素质量分数越大,耗氧量越多。
Ⅰ.A是来自石油的基本化工原料,A是气态烃,B和D是生活中两种常见的有机物,A与水反应生成B,B连续氧化生成D,B为醇,D为羧酸,则A为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,CH3CHO进一步氧化生成D为CH3COOH,CH2=CH2发生加聚反应生成高聚物F为聚乙烯。
(1)A为乙烯,分子的电子式是![]() ;
;
(2)乙醇 在铜催化下与氧气反应生成乙醛,断裂的是羟基上的氢氧键、与羟基所连的碳上的碳氢键,断键的位置为②④;
在铜催化下与氧气反应生成乙醛,断裂的是羟基上的氢氧键、与羟基所连的碳上的碳氢键,断键的位置为②④;
(3)①B→C是乙醇氧化生成乙醛,反应方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
②A→B是乙烯水化催化发生加成反应生成乙醇,反应的化学方程式为CH2=CH2 + H2O ![]() CH3CH2OH;
CH3CH2OH;
③比A多一个碳原子的 A的同系物为丙烯,发生加聚反应生成聚丙烯,反应的化学方程式为:n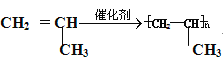 ;
;
Ⅱ. (1)分子式为C8H10的芳香烃,分子中含有1个苯环,其不饱和度=![]() =4,故侧链为烷基,若有1个侧链,为-CH2-CH3,有一种;若有2个侧链,为-CH3,有邻、间、对三种,故符合条件的结构共有4种;
=4,故侧链为烷基,若有1个侧链,为-CH2-CH3,有一种;若有2个侧链,为-CH3,有邻、间、对三种,故符合条件的结构共有4种;
(2)等质量的各烃完全燃烧,烃中H元素质量分数越大,耗氧量越多,CH4、CH2=CH2、C6H6中C、H原子数目之比分别为1:4、


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1 mL,分别加水稀释到1 000 mL,其中pH与溶液体积V的关系如图所示,下列说法正确的是

A. 稀释前,A、B两酸溶液的物质的量浓度一定相等
B. 稀释后,A酸溶液的酸性比B酸溶液强
C. a=5时,A是强酸,B是弱酸
D. 稀释导致B酸的电离程度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量的浓度和混合液的pH如下表所示:
实验编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还弱酸? 。
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)= mol/L。
Ⅱ.某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB-![]() H++B2-
H++B2-
回答下列问题:
(5)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是( )
A.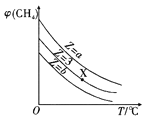 表示一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)
表示一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)平衡时φ(CH4)的体积分数与Z(Z=
CO(g)+3H2(g)平衡时φ(CH4)的体积分数与Z(Z=![]() )和T(温度)的关系,则该反应的焓变△H>0,且b>3>a
)和T(温度)的关系,则该反应的焓变△H>0,且b>3>a
B.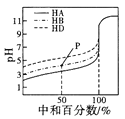 表示室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线,可以看出三种酸的电离常数关系为KHA>KHB>KHD,且滴定至P点时,溶液中:c(HB)>c(Na+)>c(B- )>c(H+)>c(OH-)
表示室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线,可以看出三种酸的电离常数关系为KHA>KHB>KHD,且滴定至P点时,溶液中:c(HB)>c(Na+)>c(B- )>c(H+)>c(OH-)
C.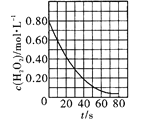 是室温下H2O2催化分解放出氧气的反应中c(H2O2)随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
是室温下H2O2催化分解放出氧气的反应中c(H2O2)随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
D.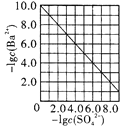 是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明溶液中c(SO42-)越大c(Ba2+)越小
是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明溶液中c(SO42-)越大c(Ba2+)越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应X(g)+Y(g) ![]() nZ(g) ΔH >0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
nZ(g) ΔH >0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
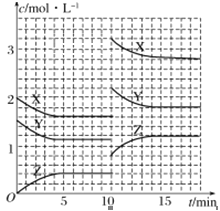
A.反应方程式中n=1
B.10min时,曲线发生变化的原因是升高温度
C.10min时,曲线发生变化的原因是增大压强
D.前5min后,用X表示的反应速率为v(X)=0.08mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应a A(g)+b B(g)![]() c C(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
c C(g) ΔH<0在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
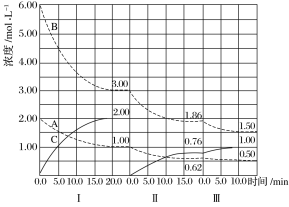
(1)反应的化学方程式中a∶b∶c为_____________________________________________。
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为______________。
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是________,其值是________。
(4)由第一次平衡到第二次平衡,平衡向________移动,采取的措施是________________________。
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2________(填“<”“>”或“=”)T3,判断的理由是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母)。
a.碳棒b.锌板c.铜板

(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的________(填“正”或“负”)极。F电极上的电极反应式为____________________________________________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_________________________________________________________________________。

(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_______________________________________________________。
②若有2mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示,其中A为带支管口的试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:
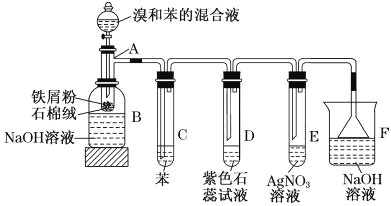
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):_____;
(2)试管C中苯的作用是_____,反应开始后,观察D和E两试管,D中看到的现象为____,E中发生的反应为(写离子方程式)______。
(3)反应2min~3min后,在B中可观察到的现象是______,B中NaOH溶液的作用是:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com