
����Ŀ����.�����£���ijһԪ��HA(�ס��ҡ�������������ͬ��һԪ��)��NaOH��Һ�������ϣ�������Һ�����ʵ�����Ũ�Ⱥͻ��Һ��pH���±���ʾ��
ʵ���� | HA����������Ũ��(mol��L-1) | NaOH����������Ũ��(mol��L-1) | ��Ϻ���Һ��pH |
�� | 0.1 | 0.1 | pH��a |
�� | 0.12 | 0.1 | pH��7 |
�� | 0.2 | 0.1 | pH��7 |
�� | 0.1 | 0.1 | pH��10 |
��1�������������������������HA��ǿ�ỹ������ ��
��2�����������Һ������Ũ��c(A-)��c(Na+)�Ĵ�С��ϵ�� ��
A��ǰ�ߴ� B�����ߴ� C��������� D�����ж�
��3��������ʵ������������������Һ������Ũ���ɴ�С��˳���� ��
��4����������ʵ�����ݣ�д���������Һ��������ʽ�ľ�ȷ����(��ʽ)��c(Na+)��c(A-)�� mol/L��
��.ij��Ԫ��(����ʽ��H2B��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2B=H++HB-��HB-![]() H++B2-
H++B2-
�ش��������⣺
��5����0.1 mol/L��Na2B��Һ�У���������Ũ����ϵʽ��ȷ���� ��
A��c(B2-)+c(HB-)��0.1mol/L
B��c(B2-)+c(HB-)+c(H2B)��0.1mol/L
C��c(OH-)��c(H+)+c(HB-)
D��c(Na+)+c(OH-)��c(H+)+c(HB��)
���𰸡���1��a=7ʱ��HA��ǿ����a>7ʱ��HA������
��2��C(3������3��c(Na+)>c(A-)>c(OH-)>c(H+)(3����
��4��10-4-10-3(3������5��A��C(3����
��������
�����������1��һԪ��HA��NaOH�����ʵ�����Ӧ������ǿ��ȡ������ȫ�кͺ��ε�pH����a=7Ϊǿ������a��7Ϊ������
��2���ݵ���غ�����c(Na+)+c(H+)��c(A-)+c(OH-)����c(H+)��c(OH-)������c(Na+)��c(A-)����ѡC��
��3����Ϊ��Ũ�ȵ�HA��NaA�Ļ����Һ����pH��7֪A-ˮ��̶ȴ���HA�ĵĵ���������Ũ�ȴ�С��ϵΪc(Na+)��c(A-)��c(OH-)��c(H+)��
��4���ݵ���غ�c(Na+)+c(H+)��c(A-)+c(OH-)���Ƶ�c(Na+)-c(A-)��c(OH-)��c(H+)����10-4-10-10��mol/L��
��5����Na2B�д���ˮ��ƽ�⣺B2-+H2O![]() HB- +OH-��HB-�����һ��ˮ�⣬������Һ��û��H2B���ӡ�A�����������غ��c( B2- )+c(HB- )��0.1 mol/L��A��ȷ��B����Һ��û��H2B���ӣ����Ը��������غ�ɵã�c(Na+)��2[c(B2-)+ c(HB- )]��B����C�����������غ��c(OH- )=c(H+)+c(HB- )��C����D�����ݵ���غ���֪c(Na+)+c(H+)��c(OH-)+c(HB-)+2c(B2- )��D��������ѡAC��
HB- +OH-��HB-�����һ��ˮ�⣬������Һ��û��H2B���ӡ�A�����������غ��c( B2- )+c(HB- )��0.1 mol/L��A��ȷ��B����Һ��û��H2B���ӣ����Ը��������غ�ɵã�c(Na+)��2[c(B2-)+ c(HB- )]��B����C�����������غ��c(OH- )=c(H+)+c(HB- )��C����D�����ݵ���غ���֪c(Na+)+c(H+)��c(OH-)+c(HB-)+2c(B2- )��D��������ѡAC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH=13����Һ�У��ܴ���������������ǣ�
A. Na+��NH4+��Cl����SO42�� B. K+��Na+��AlO2����Cl��
C. Mg2+��K+��NO3����Cl�� D. K+��Na+��Al3+��SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ���Ȼ�ѧ����ʽ:
(1)1 mol C2H5OH(l)��ȫȼ������CO2(g)��H2O(l),�ų�1 366.8 kJ����: ��
(2)1 mol C(ʯī)������H2O(g)��Ӧ����CO(g)��H2(g),����131.3 kJ����: ��
(3)1.7 g NH3(g)������������Ӧ������̬����,�ų�22.67 kJ������: ��
����֪���з�Ӧ�ķ�Ӧ��Ϊ
��CH3COOH(l)��2O2(g)��2CO2(g)��2H2O(l) ��H1����870.3kJ/mol
��C(s)��O2(g)��CO2(g) ��H2����393.5kJ/mol
��H2(g)��1/2O2(g)��H2O(l) ��H3����285.8kJ/mol
�Լ���������Ӧ�ķ�Ӧ�ȣ�2C(s)��2H2(g)��O2(g)��CH3COOH(l) ��H=_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̫���ܵ�ذ����̫��ʱ��һ���ֵ���ֱ�ӹ������칬һ������һ���ֵ������ڵ���������̫��ʱʹ�á����칬һ����ʹ�õ��������أ��������Һ�Լ��ԡ��䷴Ӧ����ʽΪ�� LaNi5+Ni(OH)2![]() LaNi5H+NiOOH�������й�˵������ȷ����
LaNi5H+NiOOH�������й�˵������ȷ����
A. �ŵ�ʱ������ԭ B. �ŵ�ʱ����LaNi5H+OH����e����LaNi5+H2O
C. ���ʱOH���������ƶ� D. ���ʱÿ����lmol Ni(OH)2ת��lmol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪����ʱ��0.1mol/LijһԪ��HA��ˮ����0.1%�������룬�����Һ��pH= ������ĵ���ƽ�ⳣ��K= ����HA�������H+��Ũ��ԼΪˮ�������H+��Ũ�ȵ� ����
��2����������HA��������NaA�Ļ����Һ���ڻ�ѧ�����������ܼ��������м�����������ʱ����Һ������Ա仯����
�������Һ�м�����������ʱ��������Ӧ�����ӷ���ʽ�� �������м�������KOH��Һʱ��������Ӧ�����ӷ���ʽ�� ��
���ֽ�0.04mol�qL-1HA��Һ��0.02mol�qL-1NaOH��Һ�������ϣ��õ�������Һ��
a����HAΪHCN������Һ������������Һ��c��Na+�� c��CN-�������������=����������
b����HAΪCH3COOH������Һ�����ԣ���Һ�����е����Ӱ�Ũ���ɴ�С���е�˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.50mol��L��1������50 mL 0.55mol��L��1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ���ش��������⣺
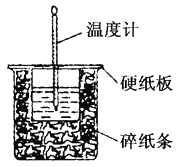
��1��С�ձ��з�����Ӧ�����ӷ���ʽΪ�� ________________________________��
��2����ʵ���з�Ӧ����������,�¶ȼ���ʾ�¶�����,˵���÷�Ӧ��__________��Ӧ(����ȡ������ȡ�)
��3���������ĽǶȿ�,�Ͽ���ѧ��Ҫ________________���γɻ�ѧ��Ҫ_________________________��
��4����ʵ���е�ҩƷ��Ϊ��Ƭ��ϡ���ᣬ�¶ȼ���ʾ�¶�������������Ӧ�Ļ�ѧ����ʽΪ______________________,��Ӧ���������__________�������������(����ڡ���С�ڡ�)
��5��Ŀǰ��ȫ������Ҫ���ڻ�ʯ��Դʱ�ڣ������й���Դ˵����ȷ����__________��
A��ú��ʯ�͡���Ȼ�����ڿ�ʯ��Դ����ȡ֮������֮���ߵģ����Դ���ʹ��
B����������Ҫ�ɷ��Ǽ״�����һ�������Դ
C��̫���ܡ����ܡ����ܵ��Ժ�Ϊ�ṩ��Դ����Ҫ��ʽ
D�������÷��ܷ����������ˮ���ڵĵ��ܲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2ͨ��BaCl2��Һ�����ͣ�δ���������ɣ�����ͨ����һ�����壬���������tͨ������������
A. CO2 B. NH3 C. NO2 D. Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. ������![]() ��������2-�һ�����
��������2-�һ�����
B. 2-�������2��2-�������黥Ϊͬϵ��
C. �����£���ϩ�ͱ����ܱ�����KMnO4������ʹKMnO4��Һ��ɫ
D. �����ʵ�������ϩ���Ҵ���ȫȼ�գ��������������ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ�����ʵ���������������ɵ���( )��
A. CuO��Cu B. H2SO4��H2 C. Fe��FeCl2 D. HNO3��N2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com