
【题目】苯和溴的取代反应的实验装置如图所示,其中A为带支管口的试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:
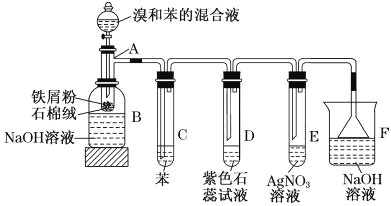
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):_____;
(2)试管C中苯的作用是_____,反应开始后,观察D和E两试管,D中看到的现象为____,E中发生的反应为(写离子方程式)______。
(3)反应2min~3min后,在B中可观察到的现象是______,B中NaOH溶液的作用是:_____。
【答案】![]() +Br2
+Br2![]() +HBr 除去HBr气体中混有的溴蒸气 紫色石蕊试液变红 Ag++Br-=AgBr↓ 瓶底有无色油状液体产生 除去溴苯中的Br2
+HBr 除去HBr气体中混有的溴蒸气 紫色石蕊试液变红 Ag++Br-=AgBr↓ 瓶底有无色油状液体产生 除去溴苯中的Br2
【解析】
向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。A中发生反应为苯与溴单质在铁粉作用下反应,生成溴苯和溴化氢;因为生成的HBr中混有Br2,会干扰HBr的检验,所以试管C中加苯除去,反应开始后,D中HBr与紫色石蕊试液反应,E中HBr与AgNO3反应。F中氢氧化钠溶液吸收尾气,同时防止倒吸。
(1)A中发生反应的化学方程式为![]() +Br2
+Br2![]() +HBr;
+HBr;
(2)因为生成的HBr中混有Br2,会干扰HBr的检验,所以试管C中苯的作用是除去HBr气体中混有的溴蒸气;反应开始后,D中HBr与紫色石蕊试液反应,紫色石蕊试液变红;E中HBr与AgNO3反应,离子方程式为Ag++Br-=AgBr↓。
(3)反应2min~3min后,在B中生成的溴苯进入NaOH溶液中,B中NaOH溶液去除溴苯中溶解的溴。在B中可观察到的现象是瓶底有无色油状液体产生,B中NaOH溶液的作用是除去溴苯中的Br2。


科目:高中化学 来源: 题型:
【题目】Ⅰ.A是来自石油的基本化工原料。A是气态烃,B和D是生活中两种常见的有机物,F是高分子化合物,相互转化关系如图所示.
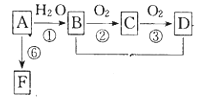
(1)A分子的电子式是___;
(2)乙醇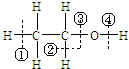 在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
在化学反应中断键位置:乙醇在铜催化下与氧气反应,在___位置断裂;
(3)写出下列反应的化学方程式:
①B→C:___;
②A→B:___;
③比A多一个碳原子的 A的同系物发生加聚反应的方程式:___。
Ⅱ.苯和苯的同系物在化工生产中应用十分广泛。
(1)分子式为C8H10为的苯的同系物的同分异构有___种;
(2)CH4、CH2=CH2、C6H6等质量时消耗氧气最多的气态烃是___(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2、NO是大气污染物,NH4NO3、H2SO4等是水体污染物,有效去除这些污染物是一项重要课题。
(1) NO、SO2可以先氧化,后用碱吸收。其氧化过程的反应原理如下:
NO(g)+O3(g)![]() NO2(g)+O2(g);ΔH1=-200.9 kJ·mol-1
NO2(g)+O2(g);ΔH1=-200.9 kJ·mol-1
SO2(g)+O3(g)![]() SO3(g)+O2(g);ΔH2=-241.6 kJ·mol-1
SO3(g)+O2(g);ΔH2=-241.6 kJ·mol-1
2SO2(g)+O2(g)![]() 2SO3(g);ΔH3=-196.6 kJ·mol-1
2SO3(g);ΔH3=-196.6 kJ·mol-1
则反应2NO2(g)![]() 2NO(g)+O2(g)的ΔH=____kJ·mol-1。
2NO(g)+O2(g)的ΔH=____kJ·mol-1。
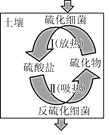
(2)土壤中的硫循环如图所示,土壤中的黄铁矿(FeS2)在过程Ⅰ中会转化成硫酸亚铁和硫酸,该过程发生的化学方程式为________________。
(3)电解法除去工业废水中的硝酸铵的装置示意图如图所示,阴极电极反应式为___。
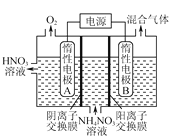
(4)向恒容密闭容器中充入1 mol NO和2 mol O3,发生如下反应:NO(g)+O3(g)![]() NO2(g)+O2(g);ΔH<0。不同温度下反应相同时间后,体系中NO转化率随温度变化曲线如图。温度低于100℃时,NO转化率随温度升高而增大的主要原因是____;当温度高时,O3分解生成活性极高的氧原子,NO转化率随温度升高而降低,可能的原因有:①______,②______。
NO2(g)+O2(g);ΔH<0。不同温度下反应相同时间后,体系中NO转化率随温度变化曲线如图。温度低于100℃时,NO转化率随温度升高而增大的主要原因是____;当温度高时,O3分解生成活性极高的氧原子,NO转化率随温度升高而降低,可能的原因有:①______,②______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)![]() COS(g)+H2O(g)
COS(g)+H2O(g)
实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
I | 607 | 0.11 | 0.41 | 0.01 | |
II | 607 | 0.22 | 0.82 | ||
III | 620 | 0.1 | 0.4 | 6.74×10-3 | |
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+2B2(g)![]() 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol A2、2molB2 | 2molAB3 | 2mol AB3 |
反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时AB3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是( )
A.v甲=v丙B.c乙<c丙C.a甲 +a乙<1D.K乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)是提取铝的原料,提取铝的工艺流程如图:

请回答下列问题:
(1)过滤操作需用到的玻璃仪器除烧杯、玻璃棒外,还需要__。
(2)流程图中固体B的成分为__,流程图中试剂X为__。
(3)为验证滤液A含Fe3+,可取少量滤液A滴加__溶液,溶液显红色。
(4)通入过量的CO2时发生的化学方程式为__。
(5)现有102 t含氧化铝50%的铝土矿,理论上可炼出__t金属铝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(g)cC(g)+dD(g)△H,根据图象判断,下列叙述正确的是( )

A.p1<p2,a+b<c+d,T1<T2,△H>0
B.p1<p2,a+b>c+d,T1>T2,△H>0
C.p1<p2,a+b<c+d,T1>T2,△H>0
D.以上答案均不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如表:

(1)上表的6种酸进行比较,酸性最弱的是:_____;HCOO-、S2-、HSO3-三种离子中,最难结合H+的是__________。
(2)在浓度均为0.1mol/L的HCOOH和H2C2O4混合溶液中,逐渐滴入0.1mol/L的NaOH溶液,被OH-先后消耗的酸及酸式酸根依次是:_________。
(3)已知HNO2具有强氧化性,弱还原性。将HNO2溶液滴加到H2S溶液中,同时有沉淀和无色气体生成,该气体遇空气立即变为红棕色,试写出两酸之间的化学反应方程式:___。
(4)下列离子方程式书写正确的是________。
A.HNO2+HS-=NO2-+H2S↑
B.2HCOOH+SO32-=2HCOO-+H2O+SO2↑
C.H2SO3+2HCOO-=2HCOOH+SO32-
D.H2SO3+SO32-=2HSO3-
E.H2C2O4+NO2-=HC2O4-+HNO2
(5)将少量的SO2通入Na2C2O4溶液,写出离子方程式___。
(6)已知HX为一元弱酸。HX的电离常数为5.5×10﹣8。某混合溶液中含有4molNaX、2molNa2CO3和1molNaHCO3。往溶液中通入3molCO2气体,充分反应后,气体全部被吸收,计算某些物质的量:Na2CO3______、NaHCO3______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的化学方程式中,书写正确的是
A.CH4和Cl2混合后光照:CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B.CH2=CH2通入Br2的CCl4溶液中:CH2=CH2+Br2→CH3CHBr2
C.CH3CH2OH在Cu作催化剂条件下与O2反应: CH3CH2OH+O2![]() CH3COOH+H2O
CH3COOH+H2O
D.CH3COOH与CH3CH2OH 发生酯化反应:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com