
【题目】SO2和H2S会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
(1)用氨水除去SO2:
已知 25℃,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,NH3·H2O的 Kb=1.8×l0-5。
①试写出H2SO3在水溶液中的电离方程式__________________,从电离平衡的角度解释Ka1、Ka2差别很大的原因_________________。
②若氨水的浓度为0.02 mol·L-1,溶液中的c(OH-)=____________mol·L-1、将SO2通入该氨水中,当溶液中的c(SO32-)/ c(HSO3-)=6.2时,溶液的pH=_____________。
(2)生物脱H2S:
原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______________ 。
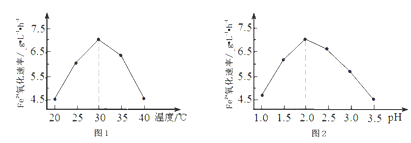
②由图1和图2判断使用硫杆菌的最佳条件为________________ ,若反应温度过高,反应速率下降,其原因是__________________________ 。
【答案】 H2SO3![]() HSO3-+H+ 第一步电离的H+抑制了第二步的电离 6.0×10-4 8.0 降低反应活化能(或作催化剂) 30 °C、pH=2.0 蛋白质变性(或硫杆菌失去活性)
HSO3-+H+ 第一步电离的H+抑制了第二步的电离 6.0×10-4 8.0 降低反应活化能(或作催化剂) 30 °C、pH=2.0 蛋白质变性(或硫杆菌失去活性)
【解析】试题分析:本题考查电离方程式的书写,电离平衡常数的计算,外界条件对化学反应速率的影响,图像的分析。
(1)①H2SO3属于弱酸,在水溶液中的电离方程式为:H2SO3![]() HSO3-+H+、HSO3-
HSO3-+H+、HSO3-![]() H++SO32-。Ka1
H++SO32-。Ka1![]() Ka2的原因是:第一步电离的H+抑制了第二步的电离。
Ka2的原因是:第一步电离的H+抑制了第二步的电离。
②在氨水中存在电离平衡:NH3·H2O![]() NH4++OH-,溶液中c(NH4+)
NH4++OH-,溶液中c(NH4+)![]() c(OH-),c(NH3·H2O)=0.02mol/L-c(NH4+),由于弱碱的电离微弱,则溶液中c(NH3·H2O)
c(OH-),c(NH3·H2O)=0.02mol/L-c(NH4+),由于弱碱的电离微弱,则溶液中c(NH3·H2O)![]() 0.02mol/L,Kb=1.8
0.02mol/L,Kb=1.8![]() 10-5=
10-5= ,c(OH-)=
,c(OH-)=![]() =6
=6![]() 10-4mol/L。H2SO3的Ka2=[c(H+)·c(SO32-)]/c(HSO3-)=6.2
10-4mol/L。H2SO3的Ka2=[c(H+)·c(SO32-)]/c(HSO3-)=6.2![]() 10-8,当溶液中的c(SO32-)/ c(HSO3-)=6.2时,c(H+)=10-8mol/L,溶液的pH=-lg c(H+)=8。
10-8,当溶液中的c(SO32-)/ c(HSO3-)=6.2时,c(H+)=10-8mol/L,溶液的pH=-lg c(H+)=8。
(2)①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用作催化剂,降低反应的活化能,加快反应速率。
②由图①判断最佳温度为30℃,由图②判断最佳pH为2.0,最佳条件为30℃、pH=2.0。若反应温度过高,反应速率下降的原因是:温度过高,蛋白质(或硫杆菌)发生变性,失去活性。


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 向小苏打溶液中加入足量澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
B. 向醋酸钠溶液中通入少量的二氧化碳:2CH3COO- + CO2 + H2O=2CH3COOH+CO![]()
C. 向溴化亚铁溶液通入过量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D. 向氢氧化钡溶液中加入硫酸氢钠溶液至恰好完全沉淀:Ba2+ +OH-+H++SO42- =BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KCl与KNO3在不同温度的溶解度数据如下表.则下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
A.KNO3比KCl的溶解度大
B.两种物质的溶解度相等的温度在20~30℃间
C.在20℃时,10g水中加入5gKCl可得到33.3% 的KCl溶液
D.在50℃时,两物质各5g分别加入l0g水中,充分溶解,均有固体剩余
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 在托盘天平上放两片大小、质量一样的纸,然后将氢氧化钠放在纸片上称量
B. 把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶
C. 用蒸馏水洗涤烧杯、玻璃棒2—3次,洗涤液也移入容量瓶
D. 沿玻璃棒往容量瓶中加入蒸馏水,到刻度线1—2cm时改用胶头滴管滴加,直到溶液凹液面恰好与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A | B | C | D | |
实验 | 用CCl4提取 溴水中的Br2 | 除去氢氧化铁 胶体中的氯化钠 | 从KI和I2的固体混合物中回收I2 | 配制100 mL0.1 mol·L-1 NaCl溶液 |
装置或 仪器 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,有与石墨相似的层状结构。层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是

A. 正硼酸晶体属于原子晶体 B. H3BO3分子的稳定性与氢键有关
C. 分子中B原子杂化轨道的类型为sp3 D. 含1mol H3BO3晶体中有3mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷中混有乙烯,欲将乙烯除去得到纯净的甲烷,将混合气体依次通入盛有下列试剂的洗气瓶,合理的是( )
A. 澄清石灰水,浓硫酸 B. 溴水,浓硫酸
C. 高锰酸钾酸性溶液,浓硫酸 D. 浓硫酸,高锰酸钾酸性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组顺序的排列正确的是
A. 最高正价:P<S<Cl<Ar B. 热稳定性:H2O>HF>HCl
C. 酸性强弱:HNO3<H2CO3<H3PO4 D. 还原性 F- <Cl-<Br-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com