
【题目】SO2是一种重要的氧化物,可用于生产三氧化硫、硫酸、亚硫酸盐、硫代硫酸盐,也可用作熏蒸剂、防腐剂、消毒剂、还原剂等。
(1)SO2性质多变,若将SO2气体通入氢硫酸中,能看到的现象为:__________,该反应中SO2表现出______性;若将SO2气体通入酸性高锰酸钾溶液中,离子反应方程式为_________,该反应中SO2表现出__________性。
(2)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2CaSO4·2H2O碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
余石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(3)在石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。
【答案】溶液中生成黄色沉淀 氧化性 2MnO4-+5SO2+2H2O=5SO42-+2Mn2++4H+ 还原性 SO2+2NaOH=Na2SO3+H2O 成本较高 NaOH CaO+H2O=Ca(OH)2 Ca(OH)2+Na2SO3=CaSO3↓+2NaOH
【解析】
(1)将SO2气体通入氢硫酸中,发生反应SO2+2H2S=3S↓+2H2O;将SO2气体通入酸性高锰酸钾溶液中,发生反应:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(2)二氧化硫和氢氧化钠的反应方程式为:2NaOH+SO2=Na2SO3+H2O,参照价格表,NaOH成本高;
(3)向Na2SO3溶液中加入CaO后,生成NaOH,故NaOH为循环利用的物质;CaO加入溶液中会先和水反应,即CaO+H2O=Ca(OH)2,生成的Ca(OH)2再和Na2SO3溶液反应,据此答题。
(1)二氧化硫具有弱氧化性,将SO2气体通入氢硫酸中,发生反应SO2+2H2S=3S↓+2H2O,
看到的现象为溶液中生成黄色沉淀,二氧化硫中S化合价由+4价→0价,化合价降低的反应物作氧化剂,体现氧化性;将SO2气体通入酸性高锰酸钾溶液中,高锰酸钾具有强氧化性,将二氧化硫溶于水后生成的亚硫酸氧化为硫酸,二氧化硫遇到强氧化剂时体现还原性,将MnO4-还原为Mn2+,S元素的化合价升高2价,锰元素的化合价降低5价,则高锰酸根系数为2,二氧化硫系数为5,根据原子守恒,硫酸根系数为5,Mn2+系数为2,根据电荷守恒,右侧补4个氢原子,最终根据H原子守恒,左侧补2个水,即方程式为:
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,二氧化硫中S元素的化合价由+4价→+6价,化合价升高的反应物作还原剂,体现还原性,故答案为:溶液中生成黄色沉淀,氧化性,2MnO4-+5SO2+2H2O=5SO42-+2Mn2++4H+,还原性。
(2)二氧化硫作为酸性氧化物,可以和氢氧化钠反应盐和水,参照二氧化碳和氢氧化钠反应的方程式,写出二氧化硫和氢氧化钠的反应方程式为:2NaOH+SO2=Na2SO3+H2O,由于石灰的碱性比氢氧化钠弱,吸收SO2的速率慢、效率低,但吸收成本比氢氧化钠低的多,故答案为:SO2+2NaOH=Na2SO3+H2O,成本较高。
(3)从流程图中可以看出,向Na2SO3溶液中加入CaO后,生成NaOH,生成的NaOH可以作为二氧化硫的吸收剂,故NaOH为循环利用的物质;CaO加入溶液中会先和水反应,即CaO+H2O=Ca(OH)2,生成的Ca(OH)2再和Na2SO3溶液反应,根据流程图,反应物之一为NaOH,再根据复分解反应原理,另一生成物为CaSO3,故反应方程式为:Ca(OH)2+Na2SO3=CaSO3↓+2NaOH,故答案为:NaOH,CaO+H2O=Ca(OH)2、Ca(OH)2+Na2SO3=CaSO3↓+2NaOH。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) △H=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=![]() ,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
,请写出此反应的热化学方程式:_______;下列措施能够增大此反应中NO的转化率的是(填字母代号)_________。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~5min内,以CO2表示的该反应速率v(CO2)=______,该条件下的平衡常数K=________。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______移动(填“正向”“逆向”或“不”);最终达平衡时NO的转化率a=______________。
(3)在25 ℃下,向浓度均0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_____沉淀(填化学式),当两种沉淀共存时,溶液中c(Mg2+)/c(Cu2+)=__________(已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;A、D同主族,D的焰色反应为黄色;E的简单阳离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C、G两种元素的原子最外层共有13个电子。则
(1)F在元素周期表中的位置为_______________。
(2)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为__________________________。
(3)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________。
(4)D2F溶液在空气中长期放置发生反应,生成一种强碱与D2F2。D2F2与过氧化钠的结构和化学性质相似,其溶液显黄色。D2F2的电子式为_______,写出D2F在空气中长期放置生成D2F2的化学反应方程式为:_____________。D2F2的溶液与稀硫酸反应产生的现象为_____________。
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________。
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。

则曲线Y表明M中的溶质为________;原NaOH溶液的物质的量浓度为_______;由曲线X、Y可知,两次实验通入的CO2的体积比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细,由此判断下表中所列的M、N、P物质,其中可以成立的是
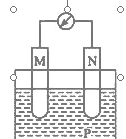
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸银溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用。

(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是_______,负极发生的电极反应方程式为:_____________________。若反应消耗16.25 g 负极材料,则电池中转移电子的物质的量为______mol。
(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A. ①③ B. ②④ C. ①④ D. ②③
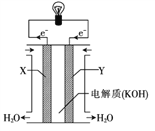
(3)右图为氢氧燃料电池的构造示意图,根据电子运动方向可知,则X极为电池的______(填“正”或“负”)极,Y极的电极反应方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列有关问题。
(1)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
阳离子 | K+ | Cu2+ | Fe3+ | Al3+ | Fe2+ |
阴离子 | Cl- | CO32— | NO3— | SO42— | SiO32— |
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:原溶液中所含阳离子是___________________,阴离子是_____________________。
(2)光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。
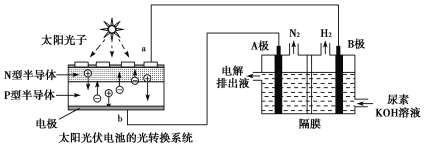
图1 图2
①图1中N型半导体为____________(填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___________________________________________。
③若A极产生7.00gN2,则此时B极产生_____________LH2(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产铅蓄电池时,在两极板上的铅、锑合金棚架上均匀涂上膏状的PbSO4,干燥后再安装,充电后即可使用,发生的反应是2PbSO4+2H2O![]() PbO2+Pb+2H2SO4下列对铅蓄电池的说法错误的是( )
PbO2+Pb+2H2SO4下列对铅蓄电池的说法错误的是( )
A. 需要定期补充硫酸
B. 工作时铅是负极,PbO2是正极
C. 工作时负极上发生的反应是Pb-2e-+SO42-===PbSO4
D. 工作时电解质的密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KC1O3和草酸(H2C2O4)在60℃时反应制得。某学生用下图所示的装置模拟工业制取及收集C1O2,其中A为C1O2的发生装置,B为C1O2的凝集装置,C为尾气吸收装置。

请回答下列问题:
(1)A中反应产物有K2CO3、C1O2和CO2等,请写出该反应的化学方程式:________________________。
A部分还应添加温水浴控制温度在60 °C,B部分还应补充什么装置:_________________。
(2)该装置按(1)补充完整后,装置A、B、C中还有一处设计明显不合理的是_____(填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),该反应的离子方程式为____________。若实验时需要450 mL 4 mol L-1的NaOH溶液,则在精确配制时,需要称取NaOH的质量是____g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室模拟以工业用菱铁矿(FeCO3)含碱式碳酸铜[Cu2(OH)2CO3]为原料制取纯净的FeCO3和氯化铜晶体(CuCl2·2H2O)的生产流程如下:
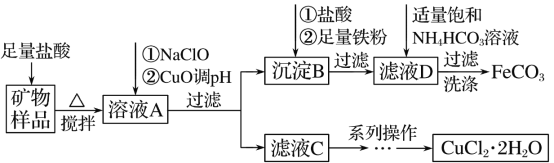
(1)盐酸溶解矿物样品时可能发生的离子方程式______。
(2)写出向溶液A中加入NaClO的离子方程式_________。
(3)向沉淀B中依次加入盐酸和铁粉时可能发生的离子方程式_________。
(4)处理滤液D时,除产生沉淀外,还产生无色气体,写出该反应的离子方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com