

| ||
| ||


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
| A、将适量的发酵粉(主要成分是碳酸氢钠)放在容器中加热,观察气体的产生 |
| B、往稀白粥中加入少量加碘食盐,检验加碘食盐中含有I2 |
| C、在洁净的水杯中先加入小苏打粉,再加入食醋,观察气体的产生 |
| D、在一瓣橘子上插入两根铜线并与小灯泡连接,验证电流的产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Al | Fe2O3 | Al2O3 | Fe |
| 熔点(℃) | 660 | 1462 | 2054 | 1535 |
| 沸点(℃) | 2467 | - | 2980 | 2750 |
| 所用试剂 | |
| 实验操作及现象 | |
| 有关反应的化学方程式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
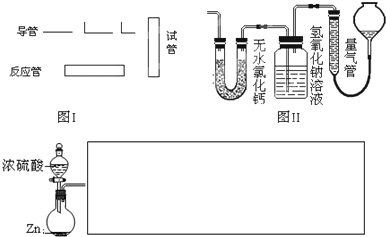
| 仪器符号 | 仪器中所加物质 | 作用 |
| 最后一种装置(作图时请对其编号) | 浓硫酸 | 防止空气中水蒸气进入E中干扰实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | n(CH4)/mol | n(H2O)/mol | n(CO)/mol | n(H2)/mo1 |
| 4 | 0.18 | 0.38 | 0.22 | 0.66 |
| n(CH4) |
| n(H2O) |
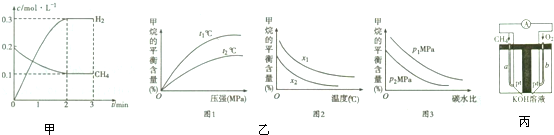
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com