
【题目】外观与氯化钠相似的亚硝酸钠(Na2NO2)在生活中应用十分广泛,如可用作建筑钢材缓蚀剂、肉制品发色剂等。已知:2NO+Na2O2=2NaNO2 2NO2+Na2O2=2NaNO3
I.某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)
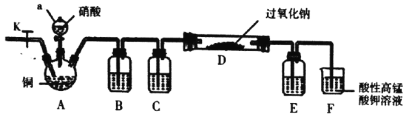
(1)仪器a的名称为________。
(2)装置B、C、E中的试制可选择___。
A 水、浓硫酸、浓硫酸
B 氢氧化钠溶液、浓硫酸、浓硫酸
C 酸性高锰酸钾溶液、浓硫酸、氢氧化钠溶液
D 水、浓硫酸、氢氧化钠溶液
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是________。
(4)装置D中的实验现象是________。
(5)装置F中发生反应的离子方程式为________。
Ⅱ.工业上可以用烧碱溶液吸收硝酸厂的尾气制得亚硝酸钠。某学习小组设计如下实验方案测定该产品中亚硝酸钠的质量分数。取1.500g产品配成250mL溶液,取25.00mL溶液于锥形瓶中加入过量的稀硫酸和碘化钾溶液充分反应后,加入适当的指示剂,用0.1000mol/L Na2S2O3标准溶液进行滴定,记录数据如下表。
实验序号 | 1 | 2 | 3 |
Na2S2O3标准溶液体积/mL | 20.02 | 19.98 | 20.00 |
已知: 2NaNO2+2KI+2H2SO4 =2NO↑+I2+2H2O+Na2SO4+K2SO4 2Na2S2O3+I2=Na2S4O6+2NaI
(6)合适的指示剂是________
(7)该产品的纯度为________。
(8)经过讨论,同学认为该产品中可能含有硝酸钠,它会使测定结果________(填“偏高”、“偏低”、“无影响”) 。
【答案】分液漏斗 A 排尽装置内的空气,防止过氧化钠或NO与其反应 淡黄色固体变成白色 5 NO+3MnO4—+4H+=5NO3—+3Mn2++2H2O 淀粉 92.00% 偏高
【解析】
I.A中铜与稀硝酸反应制取NO,获得一氧化氮所用的硝酸具有挥发性,这样会干扰实验结果,B装置是除去酸性气体,水也能与过氧化钠反应,装置C的作用是干燥NO,E是防止F中的水蒸气进入D中,D中NO能将过氧化钠还原,F中高锰酸钾具有氧化性,能将一氧化氮氧化。
Ⅱ.亚硝酸钠将碘离子氧化,生成碘单质,用硫代硫酸钠滴定,可用淀粉作指示剂,根据关系式2NaNO2~I2~2Na2S2O3计算出亚硝酸钠的含量,硝酸钠也能将碘氧化,使测定值偏大。
I.(1)仪器a的名称为分液漏斗。
(2)获得一氧化氮所用的硝酸具有挥发性,这样会干扰实验结果,B装置是除去酸性气体,水也能与过氧化钠反应,装置C的作用是干燥NO,E是防止F中的水蒸气进入D中,装置B、C、E中的试制可选择水、浓硫酸、浓硫酸;
故选A;
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是排尽装置内的空气,防止过氧化钠或NO与其反应。
(4)NO能将过氧化钠还原,装置D中的实验现象是淡黄色固体变成白色。
(5)高锰酸钾具有氧化性,能将一氧化氮氧化,装置F中发生反应的离子方程式为5 NO+3MnO4—+4H+=5NO3—+3Mn2++2H2O。
Ⅱ.(6)亚硝酸钠将碘离子氧化,生成碘单质,用硫代硫酸钠滴定,可用淀粉作指示剂,(7)2NaNO2+2KI+2H2SO4 =2NO↑+I2+2H2O+Na2SO4+K2SO4, 2Na2S2O3+I2=Na2S4O6+2NaI,
得关系式:2NaNO2~I2~2Na2S2O3,
n(NaNO2)=n(Na2S2O3)=0.1000mol/L×![]() =0.02mol,
=0.02mol,
该产品的纯度为=![]() ×100%= 92.00%;
×100%= 92.00%;
(8)硝酸钠也能将碘氧化,使测定值偏高。


科目:高中化学 来源: 题型:
【题目】已知0.1mol![]() L-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是
L-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中有:2c(Na+)=3c(A2-)+3c(HA-)+3c(HA)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分是甲烷,它是一种重要的化工原料。
(1)CH4与CO2经催化反应可制得合成气:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH
已知:反应1:CH4(g)=C(s)+2H2(g) ΔH1=+75kJ/mol
反应2: 2CO(g)=C(s)+CO2(g) ΔH2=-172kJ/mol 则该催化反应的ΔH=__________kJ/mol。
(2)工业上可用CO和H2合成二甲醚,其反应为: 2CO(g)+4H2 (g)=CH3OCH3 (g)+H2O(g) ΔH=-204.7 kJ/mol 初始条件相同时,分别在A(恒温)、B(绝热)两个容器内反应。反应初始时两容器的反应速率A_______B(填“>”、“<”或“=”,下同);平衡时CO的转化率A_______B。
(3)工业上可用CO和H2合成甲醇,其反应为CO(g)+2H2(g)=CH3OH(g) ΔH=-90.1kJ·md。温度T时,在容积为2L的某密闭容器中进行上述反应,反应过程中相关数据如图所示。
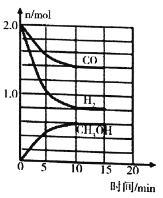
①下列能表明该反应已达到平衡状态的是__________。
a v(H2)=2v(CH3OH) b c( CO)/c( CH3OH)=7: 3时
c c(H2)/c( CH3OH)=2: 1时 d 容器中气体的压强不再变化
②该化学反应10min内生成CH3OH的反应速率v(CH3OH)= __________。
③该温度下,反应的平衡常数为__________ (列出计算式即可) 。
④若其他条件不变时,15mim时再向容器中加入2 mol CO和 x mol H2,平衡时CO的转化率与原平衡相同,则x=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不能达到实验目的的是( )
A. 用加热的方法除去碳酸钠固体中的碳酸氢钠
B. 加热蒸干溶液,可以得到CuCl2晶体
C. 放在流动的蒸馏水中可除去半透膜中蛋白质溶液里混有的(NH4)2SO4
D. 鉴别NaBr和KI溶液,可分别加新制氯水后,用CCl4萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产自来水的流程如图所示:回答下列问题.
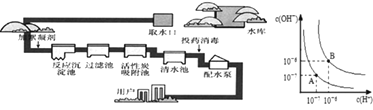
![]() 是常用的絮凝剂,它在水中最终生成 ______ 沉淀
是常用的絮凝剂,它在水中最终生成 ______ 沉淀![]() 填化学式
填化学式![]() .
.
![]() 天然水中含有较多的钙、镁离子,称为硬水.生活中常用 ______ 方法来降低水的硬度.
天然水中含有较多的钙、镁离子,称为硬水.生活中常用 ______ 方法来降低水的硬度.
![]() 过滤池利用了实验室过滤原理,在实验室过滤操作所用到的玻璃仪器是 ______ .
过滤池利用了实验室过滤原理,在实验室过滤操作所用到的玻璃仪器是 ______ .
![]() “投药消毒”中的“药”指漂白粉,请写出制取漂白粉的化学方程式 ______ .
“投药消毒”中的“药”指漂白粉,请写出制取漂白粉的化学方程式 ______ .
![]() 水的电离平衡曲线如图所示,若A点表示
水的电离平衡曲线如图所示,若A点表示![]() 时水的电离达平衡时的离子浓度,B点表示
时水的电离达平衡时的离子浓度,B点表示![]() 时水的电离达平衡时的离子浓度.
时水的电离达平衡时的离子浓度.
![]() 时
时![]() 的NaOH溶液中,由水电离出的
的NaOH溶液中,由水电离出的![]() ______
______ ![]() ,
,![]() ______
______ ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() .
.
![]() 时,向含100ml水的烧杯中逐渐加入一定量的冰醋酸,下列叙述正确的有 ______
时,向含100ml水的烧杯中逐渐加入一定量的冰醋酸,下列叙述正确的有 ______ ![]() 填字母
填字母![]() .
.
A.溶液中一直存在:![]()
B.加入过程中,水的电离程度逐渐减小,醋酸的电离程度逐渐增大
C.加入过程中,溶液中所有离子浓度逐渐增大
D.加完冰醋酸后,若升高烧杯温度,溶液pH值降低
E.用已知浓度的NaOH溶液滴定烧杯中的醋酸溶液,测定其浓度,最好选用甲基橙作指示剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期两种元素X、Y能形成XmYn型化合物.回答下列问题
(1)当n=2时,若同周期元素X、Y的最外层电子数之和为13.常温下,XY遇水易水解,并能产生能使品红溶液褪色的气体和淡黄色的单质X沉淀。则:
①元素X在周期表中的位置是________。②XmYn中含有的化学键的类型是________。
a 共价键 b 离子键 c 金属键 d 氢键
③写出XmYn与水反应的化学方程式________。
(2)若XmYn是烃类化合物.则
①当n=2时,XmYn的结构式为________。1mol XmYn能与2mol H2反应生成乙,乙能与氯气在光照下发生化学反应,最多可生成________种有机产物(不考虑立体异构).
②当n=6时,写出芳香烃XmYn与浓硝酸、浓硫酸在50℃-60℃时的化学方程式________。
③当n=8时,芳香烃XmYn的球棍模型可表示为 ,写出由XmYn聚合生成的高分子化合物的结构简式________。
,写出由XmYn聚合生成的高分子化合物的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O
B.向Ba(NO3)2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O=BaSO3↓+2H+
C.将Ca(HCO3)2溶液与少量Ca(OH)2溶液混合:OH+Ca2++HCO=CaCO3↓+H2O
D.往苯酚钠溶液中通入少量CO2:2![]() +CO2+H2O
+CO2+H2O![]() 2
2![]() +CO
+CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SiO2晶体说法正确的是( )
A.SiO2是由极性键构成的非极性分子
B.若NA表示阿伏加德罗常数,常温常压下60g SiO2中含有的共价键数目为2NA
C.碳和硅同主族,因此CO2和SiO2化学性质相似,物理性质也相似
D.SiO2晶体结构中的最小环为6个Si和6个O组成的12元环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环结构中不存在碳碳单键与碳碳双键交替的结构,下列可以作为证据的是( )
①苯不能使溴的四氯化碳溶液褪色
②苯在一定条件下既能发生取代反应,又能发生加成反应
③经测定,邻二甲苯只有一种结构
④经测定,苯环上碳碳键的键长相等,都是![]()
A.仅①B.仅①②C.仅①②④D.仅①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com