
| ||
| 28×11 |
| 28×11+100×8 |


科目:高中化学 来源: 题型:
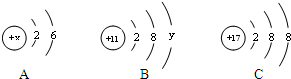 A、B、C三种元素的粒子结构示意图如图所示
A、B、C三种元素的粒子结构示意图如图所示查看答案和解析>>
科目:高中化学 来源: 题型:
 某溶液中可能含有的离子如下表:
某溶液中可能含有的离子如下表:| 可能大量含有的阳离子 | H+、NH4+、Al3+、K+ |
| 可能大量含有的阴离子 | Cl-、Br-、CO32-、[Al(OH)4]-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、40mL | B、30mL |
| C、20mL | D、10mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸溶液的pH大于盐酸 |
| B、醋酸溶液的pH小于盐酸 |
| C、与NaOH完全中和时,醋酸消耗的NaOH多于盐酸 |
| D、分别用水稀释相同倍数后,所得溶液中:n (Cl-)=n (CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com