
【题目】有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,其中1/3的铁显+2价,2/3的铁显+3价
C.FeO、Fe2O3都不溶于水,但都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法I | 用碳粉在高温条件下还原CuO |
方法II | 用肼(N2H4)还原新制Cu(OH)2 |
方法III | 电解法,反应为2Cu+H2O |
(1)已知:2Cu(s)+![]() O2(g)=Cu2O(s)△H=﹣akJmol﹣1
O2(g)=Cu2O(s)△H=﹣akJmol﹣1
C(s)+![]() O2(g)=CO(g)△H=﹣bkJmol﹣1
O2(g)=CO(g)△H=﹣bkJmol﹣1
Cu(s)+![]() O2(g)=CuO(s)△H=﹣ckJmol﹣1
O2(g)=CuO(s)△H=﹣ckJmol﹣1
则方法I发生的反应:2Cu O(s)+C(s)=Cu2O(s)+CO(g);△H= kJmol﹣1.
(2)工业上很少用方法I制取Cu2O,是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因: .
(3)方法II为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.
该制法的化学方程式为 .
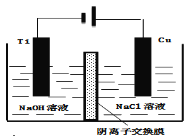
(4)方法III采用离子交换膜控制电解液中OH﹣的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式
并说明该装置制备Cu2O的原理 .
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)![]() 2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)
2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)
变化如下表所示.
序号 | Cu2O a克 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | 方法II | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 方法III | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | 方法III | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是 (填字母代号).
a.实验的温度:T2<T1
b.实验①前20min的平均反应速率v(O2)=7×10﹣5molL﹣1min﹣1
c.实验②比实验①所用的Cu2O催化效率高
d. 实验①、②、③的化学平衡常数的关系:K1=K2<K3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是 ( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是 ( )
A.N2O4的消耗速率与NO2的生成速率之比为1∶2
B.烧瓶内气体的颜色不再加深
C.烧瓶内气体的平均相对分子质量不再变化
D.烧瓶内气体的压强不再变化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学已经渗透到人类生活的方方面面。下列说法正确的是
A. “青蒿一握,以水二升渍,绞取汁”,该过程属于化学变化
B. 去皮苹果放在空气中久置变黄与纸张久置变黄原理相似
C. 高纯硅广泛用于制作光导纤维,光导纤维遇强碱会“断路”
D. 酸雨以及光化学烟雾的形成通常都与氮的含氧化合物有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用特殊方法把固体物质加工到纳米级(1~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同数量级的是
A.溶液
B.悬浊液
C.乳浊液
D.胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等。
已知①亚氯酸钠(NaClO2)受热易分解。
②NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
③纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
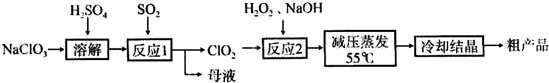
(1)“反应1”需要鼓入空气,空气的作用是_______________
(2)“反应2”的化学方程式为:_______________
(3)采取“减压蒸发”而不用“常压蒸发”,原因是_______________;结晶后需要对晶体洗涤,为了减少损失,可以用_______洗澡晶体。
(4)从“母液”中可回收的主要物质是___________;
(5)要得到纯的亚氯酸钠晶体(NaClO2·3H2O),对粗产品的必须进行的操作名称__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的气体摩尔体积比乙的气体摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式 。
(2)根据元素周期律,原子半径Ga As,第一电离能Ga As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为 ,其中As的杂化轨道类型为 。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是 。
(5)GaAs的熔点为1238℃,密度为![]() ,其晶胞结构如图所示。
,其晶胞结构如图所示。
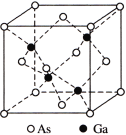
该晶体的类型为 。Ga与As的摩尔质量分别为![]() 和
和![]() ,原子半径分别为
,原子半径分别为![]() 和
和![]() ,阿伏加德罗常数值为
,阿伏加德罗常数值为![]() ,则
,则![]() 晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列名称的有机物实际上不可能存在的是( )
A. 2,2—二甲基丁烷 B. 2—甲基—4—乙基—1—己烯
C. 3—甲基—2—戊烯 D. 3,3—二甲基—2—戊烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com