
【题目】 100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是 ( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是 ( )
A.N2O4的消耗速率与NO2的生成速率之比为1∶2
B.烧瓶内气体的颜色不再加深
C.烧瓶内气体的平均相对分子质量不再变化
D.烧瓶内气体的压强不再变化。
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】华盛顿大学的研究团队采用新型的太阳能热过程生产水泥,可实现C02零排放。当电解低于800℃ 时,碳酸钙先分解成为CaO和CO2,电解质为熔融的碳酸钠,基本原理如图所示,下列说法不正确的是( )
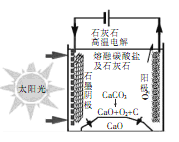
A.生产过程中能量转化方式是光能、电能转化为化学能
B.石墨电极的电极反应式为3CO2 +4e- =C+ 2CO32-
C.电解过程中熔融碳酸钠的物质的量不发生变化
D.电解过程中若产生11.2 LO2,则转移2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知—C4H9有4种同分异构体,不必写出C4H10O的结构简式,试说明其作为醇的同分异构体的数目( )
A. 2种 B. 4种 C. 3种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:
2SO2(g)+ O2(g)![]() 2SO3(g),△H=-196.6 kJ/mol.2 min时反应达到化学平衡,此时测得反应物O2还乘余0.8 mol,请填写下列空白:
2SO3(g),△H=-196.6 kJ/mol.2 min时反应达到化学平衡,此时测得反应物O2还乘余0.8 mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成SO3的平均反应速率为 ;平衡时SO2转化率为 。
(2)下列叙述能证明该反应已达到化学平衡状态的是(填标号,下同) 。
A.溶器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2nmolSO2的同时消耗nmolO2
E.相同时间内消耗2nmolSO2的同时生成nmolO2
(3)反应达到化学平衡后,以下操作将引起平衡向正反方向移动并能提高SO2转化率的是 。
A.向容器中通入少量O2 B.向容器中通入少量SO2
C.使用催化剂 D.降低温度
E.向容器中通入少量氦气(已知:氦气和SO2、O2、SO3都不发生反应)
(4)t2℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%,SO2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) ![]() 2C(g)。若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:其中正确的是
2C(g)。若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:其中正确的是
①用物质A表示的反应的平均速率为0.3mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6mol·L-1·s-1
③2s时物质B的浓度为0.7mol·L-1
④2s末,物质A的转化率为70%
A.①④ B.①④ C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,其中1/3的铁显+2价,2/3的铁显+3价
C.FeO、Fe2O3都不溶于水,但都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com