
����Ŀ���������岻��ȱ�ٵ���Ԫ�أ����뺬���Ļ�����ɲ��������������ơ����г���һ�ֳ����IJ���ҩƷ����˵���鲿������ժ¼���£� �����ÿƬ������������0.1g
����Ӧ֢������ȱ����ƶѪ֢��Ԥ���������ã�
�����ء��ܹ⡢�ܷ⡢�ڸ��ﴦ���森
��ҩ������á���ά����Cͬ���������ӱ�Ʒ���գ���ҩƬ��ˮ���Ҵ����ܽ�Ȳ���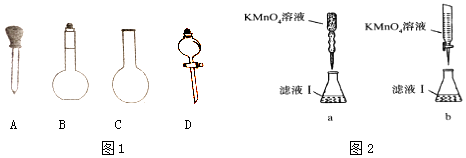
��ҩƷ��Fe2+�Ỻ�����������ҹ涨��ҩ����Fe2+�������ʣ��Ѿ�������Fe2+��������Fe2+�������ı�ֵ������10.00% �������ٷ��ã�
��1��ʵ���ҿɲ���H2SO4�ữ��KMnO4��Һ���ԡ������ơ��е�Fe2+���еζ�������ҩƷ�������ɷݲ���KMnO4��Ӧ�����ζ����̷������·�Ӧ���벹�������� Fe2++MnO4��+=Mn2+++ ��
��2��ʵ��ǰ����������Ԫ����������Ϊ20.00%�ġ������ơ�20.0g������ȫ������ϡH2SO4�У����Ƴ�250ml��Һ������ʱͼ1���������϶�����Ҫ���� �� �������ƣ�
��3��ȡ���ƺõ���Һ20.00ml����ƿ�У���0.1000mol/L��1��KMnO4��Һ�ζ���ijͬѧ�����ͼ2�ζ���ʽ���гֲ�����ȥ�������������������ĸ��ţ������ζ������У���ƿ�д���Һ�ɽ�������������Fe2+������������ƫ�ߡ�ƫ�ͻ䣩��
��4�����β����������£�
��� | V�� | Vĩ | V�� |
�� | 0.10mL | 9.71mL | 9.61mL |
�� | 1.50mL | 11.09mL | 9.59mL |
�� | 0.50mL | 11.10mL | 11.60mL |
����á������ơ�����ҩƷFe2+��������Ϊ%��
���𰸡�
��1��5��1��1��5Fe3+��4H2O
��2����ƿ������ƿ����Һ©��
��3��b��ƫ��
��4��16
���������⣺��1��MnO4����Mn�Ļ��ϼ���+7�۽�Ϊ+2�ۣ��仯5��Fe2+��Fe��+2����Ϊ+3�ۣ��仯1�ۣ����ݻ��ϼ�����������Ⱥ������غ�ã�MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��
���Դ��ǣ�5��1��8H+��1��5Fe3+��4H2O����2��ʵ��ǰ����������Ԫ����������Ϊ20.00%�ġ������ơ�20.0g������ȫ������ϡH2SO4�У����Ƴ�250ml��Һ������ʱͼ1���������϶�����Ҫ���Ƿ�Һ©����Բ����ƿ��
���Դ��ǣ���ƿ������ƿ�� ��Һ©������3�����Ը��������Һ����ǿ�����ԣ�Ӧ������ʽ�ζ���ʢ�ţ�����a����b��ȷ�����ζ������У���ƿ�д���Һ�ɽ��������ⶨ��������������������������������
���Դ��ǣ�b��ƫ�ߣ� ��4��ʵ��ǰ����������Ԫ����������Ϊ20.00%�ġ������ơ�20.0g����Ԫ������=20.00%��20.0g=4.0g������ȫ������ϡH2SO4�У����Ƴ�250ml��Һ��ȡ���ƺõ���Һ20.00ml����ƿ�У���0.1000mol/L��1��KMnO4��Һ�ζ���������֪����Һ�����ʵ��3���̫����ȥ��ƽ�����ı���Һ���V= ![]() =9.6ml��
=9.6ml��
MnO4��+ | 5Fe2++8H+�TMn2++5Fe3++4H2O |
1 | 5 |
0.0096L��0.1000mol/L��1 | n |
n=0.0048mol��
���Ƴ�250ml��Һ����Ԫ�����ʵ���= ![]() ��0.0048mol=0.06mol��
��0.0048mol=0.06mol��
�á������ơ�����ҩƷFe2+��ת����= ![]() ��100%=84%��
��100%=84%��
���ҹ涨��ҩ����Fe2+�������ʣ��Ѿ�������Fe2+��������Fe2+�������ı�ֵ������á������ơ�����ҩƷFe2+��������Ϊ16%��
���Դ��ǣ�16��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ���������800��ʱ��Ӧ2NO(g)+O2(g)![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.006 | 0.006 | 0.006 |
(1)������Ӧ�ڵ�5sʱNO��ת������___________����O2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������V(O2)=__________��
(2)��ͼ�б�ʾNO2�ı仯��������__________��

(3)��ʹ�÷�Ӧ�ķ�Ӧ�����������__________��
A.��ʱ�����NO2���� B.�ʵ������¶� C.����O2��Ũ�� D.ѡ���Ч����
(4)��˵���÷�Ӧ�Ѵﵽƽ��״̬����___________��
A.v(NO2)=2v(O2) B.������ѹǿ���ֲ���
C.v��(NO)=2v��(O2) D.�������������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��пͭԭ���װ����ͼ��ʾ�����������ӽ���Ĥֻ���������Ӻ�ˮ����ͨ���������й���������ȷ���ǣ������� 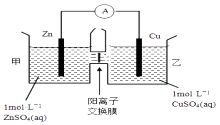
A.ͭ�缫�Ϸ�����ԭ��Ӧ
B.��ع���һ��ʱ��׳ص�c��SO42��������
C.��ع���һ��ʱ����ҳ���Һ������������
D.�����������ӷֱ�ͨ������Ĥ���������ƶ���������Һ�е��ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ,��0.10m/L������BOH�ζ�10.00 ml a mol/L������,��Һ��pH������BOH��Һ���(V)�Ĺ�ϵ��ͼ��ʾ����֪N����Һ�д��ڹ�ϵʽ:c(C1��)=c(B+)+c(BOH)������˵����ȷ����
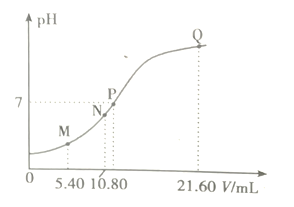
A. M����Һ�д���c(H+)=c(OH��)+2c(BOH)+c(B+)
B. N��Q������Һ��BOH����ƽ�ⳣ��:N<Q
C. P��BOH����,��ʱ��Һ��c(B+)>c(Cl��)
D. a<0.108
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��PbO�������ᣬ����ǿ����Һ���ڹ�ҵ����;�㷺������������Ǧ�ס�ɱ����ȡ�ij������Դ��ҵ�Ժ�Ǧ��������Ҫ��Pb��PbO��PbSO4�ͼ�������PbO2����ϡH2SO4Ϊԭ���Ʊ��ߴ�PbO�Ĺ�������������

��1����Ǧ�����е�PbO2��PbSO4�У�Ǧ�Ļ��ϼ۷ֱ�Ϊ____________��____________��
��2�����ܹ�����Ϊ�˼ӿ��ܽ����ʣ����˼���FeSO4�������⣬���ɲ�ȡ�Ĵ�ʩ��____________________����дһ������
��3����ҺA�к��е���Ҫ��������____________________�������ӷ�������
��4��������̷�������Ҫ��Ӧ�����ӷ���ʽΪ________________________________��
��5����ȴ�����˺�����õĹ������ϴ�Ӳ�������ʵ����ϴ��ʱ�����õ��IJ����������ձ���_________��_________����������Ƿ�ϴ�Ӹɾ��ķ�����________________________________��
��6��PbO�ܽ���NaOH��Һ�У�����ƽ����PbO(s)+NaOH(aq)![]() NaHPbO2(aq)��PbO���ܽ��������ͼ��ʾ����ϸ����ߣ������ɴ�ƷPbO�õ��ߴ�PbO�IJ�����_______________________________��
NaHPbO2(aq)��PbO���ܽ��������ͼ��ʾ����ϸ����ߣ������ɴ�ƷPbO�õ��ߴ�PbO�IJ�����_______________________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ�ϵ���ǽ���ѧ��ת��Ϊ���ܵ�װ�ã����������ʸߣ������Ѻã���δ����Դ����չ�ķ��� 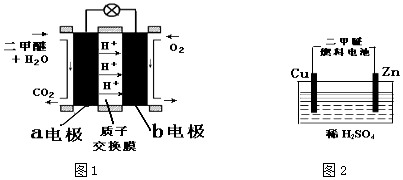
��1��ͼ1��Ϊ��ɫ��Դ�������ѡ���CH3��2O��ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ����ع���ʱ���������������� �������·����������a��b������a�缫�Ϸ�����Ӧ�ĵ缫��ӦʽΪ ��
��2������ͼ2װ�õĵ�ԴΪ��1�����еĶ�����ȼ�ϵ�أ���ͨ��Դһ��ʱ��۲쵽װ���е������Һ��ɫ����ɫ��Ϊ��ɫ����������װ���е�Cu�缫Ӧ�������ȼ�ϵ���� �缫����a��b��������ͨ��ʱ������Ӧ���ܵ����ӷ�Ӧ����ʽΪ���������缫���϶���Ϊʯī���������Һ��ΪMnSO4��Һ�����Ʊ�MnO2����������ӦʽΪ�������������23�ˣ��������ϲ���MnO2������Ϊ �ˣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ��������ͽ�������Ӧ�Ʊ���ˮ�����������û�������غ�ɫ���׳��⣬100������ʱ������װ������:
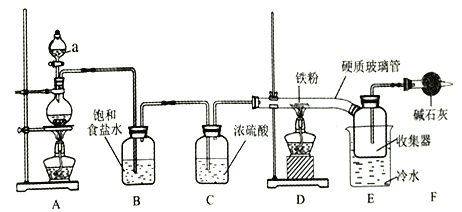
(1)����a��������________��
(2)A�з�Ӧ�Ļ�ѧ����ʽ��________��
(3)��ʯ�ҵ�������________��
(4)��Ӧ��ʼʱ���ȵ�ȼ_______���ľƾ���(�A����D��)��
(5)D�з�Ӧ��ʼ���ռ������д����غ�ɫ�����ɣ���Ӧ�������ռ�����Ӳ�ʲ������е����ʿ���ת������ƿ�У���ˮ�ܽ⣬��ַ�Ӧ����KSCN��Һδ���ɫ����ԭ����__________��(�����ӷ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H3BO3)ΪһԪ���ᣬ��֪H3BO3������NaOH��Һ��Ӧ�����ӷ���ʽΪH3BO3+OH-=B(OH)4-��H3BO3����ͨ�����ķ����Ʊ����乤��ԭ������ͼ��ʾ(��Ĥ����Ĥ�ֱ�ֻ���������ӡ�������ͨ��)������˵��������ǣ� ��
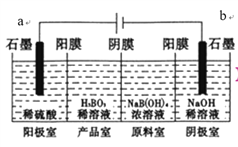
A. a���Դ������������
B. �����ĵ缫��ӦʽΪ��2H2O-4e-=O2��+4H+
C. ����·��ͨ��3mol����ʱ���ɵõ�1molH3BO3
D. B(OH)4-������Ĥ�����Ʒ�ң�Na+������Ĥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڡ�������ɫ����д���������������������ں����������¹��Ǹ������չ����ģ��ߴ������Ĺ�ľ�����²β�İ߲��ĺ�Ӱ�������¹�������γɵ�������������ԭ����
A.����һ�ֽ���B.�����е�Сˮ�ο����IJ����˶�
C.�������������D.�����е�Сˮ�ο���ֱ����СԼΪ1��100 nm
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com