
【题目】有机物X可作为合成青蒿素的一种基本原料,已知X的结构如下,下列有关X的说法正确的是
 ( )
( )
A. X为烃的含氧衍生物
B. X最多可以和3mol H2发生加成反应
C. X只能发生取代反应和加成反应
D. X可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同
科目:高中化学 来源: 题型:
【题目】常温下,向 20mL 0.2mol/L ![]() 溶液中滴加 0.2mol/L
溶液中滴加 0.2mol/L ![]() 溶液, 相关微粒的物质的量如下图 (其中Ⅰ代表
溶液, 相关微粒的物质的量如下图 (其中Ⅰ代表![]() ,Ⅱ代表
,Ⅱ代表![]() ,Ⅲ代表
,Ⅲ代表![]() ),根据图示判断,下列说法正确的是 ( )
),根据图示判断,下列说法正确的是 ( )

A. ![]() 在水中的电离方程式是:
在水中的电离方程式是: ![]()
![]()
B. 当![]() =20mL 时,溶液中各离子浓度的大小顺序为:
=20mL 时,溶液中各离子浓度的大小顺序为: ![]()
C. 等体积等浓度的![]() 溶液与
溶液与![]() 溶液混合后,其溶液中水的电离程度比纯水大
溶液混合后,其溶液中水的电离程度比纯水大
D. 当![]() =30 mL 时,溶液中存在以下关系:
=30 mL 时,溶液中存在以下关系: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为 ,下列说法不正确的是( )
,下列说法不正确的是( )
A. X的化学式为C8H8
B. 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C. X能使高锰酸钾酸性溶液褪色
D. X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应属于氧化还原反应且水既不作氧化剂又不作还原剂的是( )
A. CaO+H2O=Ca(OH)2
B. NaH+H2O=NaOH+H2↑
C. 3NO2+H2O=2HNO3+NO
D. 2H2O+2F2=4HF+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,回答下列问题:

(1)正极发生____反应(选填“氧化”或“还原”),负极电极反应式为:____。
(2)电子流动方向,从____电极(选填“Cu”或“Zn”),经外电路,流向另一电极。阳离子向____电极定向移动(选填“Cu”或“Zn”)。
(3)有0.1 mol电子流过导线,则产生H2在标准状况下的体积为____,若是断开Zn和Cu之间的导线,产生气泡的速度____(选填“加快”、“不变”或“减慢”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
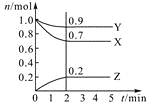
(1)该反应的化学方程式为 。
(2)反应开始至2 min,用Y表示的平均反应速率为 ,X的转化率为 。
(3)在一定温度下,下列情况可作为上述反应达到反应限度的标志的是 。
A.X、Y、Z的浓度相等 |
B.X、Y、Z的分子数比为3︰1︰2 |
C.Z的生成速率是Y的生成速率的二倍 |
D.单位时间内生成n mol Y,同时生成3n mol X |
(4)在密闭容器里,通入a mol A(g)和b mol B(g),
发生反应A(g)+ B(g)= 2C(g),当改变下列条件时,会加快反应速率的是 (填序号)。
①降低温度
②保持容器的体积不变,充入氦气
③加入催化剂
④保持容器的体积不变,增加A(g)的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是A、B、C三种烃的有关信息;
A | B | C |
①能使溴的四氯化碳溶液褪色; ②比例模型为:
| ①平面型结构 ②棍模型为: | ①能使溴的四氯化碳溶液褪色; ②1mol能与2molH2在一定条件下反应生成A ③比例模型为: |
|
图2 |
根据表中信息回答下列问题:
(1)写出烃A与水反应的化学反应方程式_____________________;
(2)烃B分子碳碳键具有的特点是_______________________
(3)如图1是烃B与液溴制取溴苯的装置,试回答:
(a)装置C中的现象___________________________________.
(b)装置B的作用__________________________________.
(4)如图2是制取烃C的装置,试回答:
(a)为了控制生成乙炔的速率,分液漏斗中盛放的液体是_______________。
(b)滴下液体后烧瓶中发生反应生成乙炔,写出此反应的化学方程式:_________。
(c)电石中含有硫化钙杂质,产生H2S,PH3等气体,为了不对乙炔性质造成干扰,应该除杂,一般选用___________洗气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应),请回答下列问题:

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。
例如,石油分馏产物之一的十六烧烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为______,乙的结构简式为________。
4乙,则甲的分子式为______,乙的结构简式为________。
(2)B装置中的实验现象可能是______,写出反应的化学方程式:______ , 其反应类型是_________。
(3)C装置中可观察到的现象是_______,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_______ (填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由:_________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是______(选填字母,下同);除去甲烷中乙烯的方法是_______。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com