��2010?�ij�һģ����Դ�����ǵ�ǰ������������ٵ��������⣬ͬʱȫ�������ů����̬������������ͻ�����������ܡ�����ȼ�ϵ�ء���չ��̼�����ǻ�ѧ�����ߵ��о�����
I������ͨ��������ˮú�������Ƶã�����CO��g��+H
2O��g��?CO
2��g��+H
2��g����H��0����850��ʱ��ƽ�ⳣ��K=1��
��1���������¶ȵ�750��ʱ���ﵽƽ��ʱK
����
����
1������ڡ�����С�ڡ����ڡ���
��2��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0mol CO��3mol H
2O��1.0mol CO
2��x mol H
2����
�ٵ�x=5.0ʱ��������Ӧ��
�淴Ӧ
�淴Ӧ
�������Ӧ�����淴Ӧ����������У�
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ�����������
x��3
x��3
��
����850��ʱ������x=5.0��x=6.0���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H
2����������ֱ�Ϊa%��b%����a
��
��
b������ڡ�����С�ڡ����ڡ���
II����֪4.6gҺ̬�Ҵ���ȫȼ�����ɶ�����̼��Һ̬ˮ�ų�����136kJ��1molҺ̬ˮת��Ϊ����ˮ����44kJ��������
��3����д���Ҵ�ȼ��������̬ˮ���Ȼ�ѧ����ʽ
C2H5OH��l��+3O2��g��=2CO2��g��+3H2O��g����H=-1228kJ/mol
C2H5OH��l��+3O2��g��=2CO2��g��+3H2O��g����H=-1228kJ/mol
��
��4����0.1mol�Ҵ�������������ȼ�գ��õ�������ȫ��ͨ�뵽100mL 3mol/L NaOH��Һ�У�����HCO
-3�ĵ��룬��������Һ��c��CO
2-3��
��
��
c��HCO
-3��������ڡ�����С�ڡ����ڡ�����ԭ����
���ɵ�̼������̼�����Ƶ����ʵ�����ȣ�CO32-ˮ��̶ȴ���HCO3-ˮ��̶�
���ɵ�̼������̼�����Ƶ����ʵ�����ȣ�CO32-ˮ��̶ȴ���HCO3-ˮ��̶�
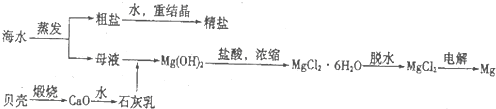
����������������



 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�






 ��
�� ��
�� ��
��
 ��
�� ��
�� ��
��