
����Ŀ����֪![]() ��
��![]() ��
��![]() ��
��![]() �Ƕ����ڽ�Ԫ���е����ַǽ���Ԫ��,���ǵ�ԭ��������������,
�Ƕ����ڽ�Ԫ���е����ַǽ���Ԫ��,���ǵ�ԭ��������������,![]() Ԫ�ص�ԭ���γɵ����Ӿ���һ������,
Ԫ�ص�ԭ���γɵ����Ӿ���һ������,![]() ��
��![]() ��Ԫ�����ڱ��д������ڵ�λ��, ���ǵĵ����ڳ����¾�Ϊ��ɫ����,
��Ԫ�����ڱ��д������ڵ�λ��, ���ǵĵ����ڳ����¾�Ϊ��ɫ����,![]() ԭ�ӵ��������������ڲ��������2����
ԭ�ӵ��������������ڲ��������2����
1.��д��![]() ��Ԫ�����ڱ��е�λ��Ϊ��________���ڡ���________�塣
��Ԫ�����ڱ��е�λ��Ϊ��________���ڡ���________�塣
2.�������![]() �ĵ���ʽΪ________________
�ĵ���ʽΪ________________
3.��![]() ��
��![]() ��
��![]() ��
��![]() ����Ԫ�ؿ������ʽ��,�û������ˮ��Һ������
����Ԫ�ؿ������ʽ��,�û������ˮ��Һ������![]() ��Һ�ڼ��������·�Ӧ�����ӷ���ʽΪ_________________��
��Һ�ڼ��������·�Ӧ�����ӷ���ʽΪ_________________��
4.��һ��������,��![]() �����뵥�ʿɻ�������
�����뵥�ʿɻ�������![]() ,��ҵ����
,��ҵ����![]() �������������Ĺܵ��Ƿ�©��,�ɹ۲쵽��������,ͬʱ�е���
�������������Ĺܵ��Ƿ�©��,�ɹ۲쵽��������,ͬʱ�е���![]() ����,д����ѧ����ʽ__________________________________���÷�Ӧ�б�������
����,д����ѧ����ʽ__________________________________���÷�Ӧ�б�������![]() ����뷴Ӧ��
����뷴Ӧ��![]() ������֮��____________��
������֮��____________��
���𰸡� �� ��A ![]()
![]()
![]()
![]()
![]()
![]()
![]() 1:4
1:4
��������XԪ�ص�ԭ���γɵ����Ӿ���һ�����ӣ���XΪH��Z��W��Ԫ�����ڱ��д������ڵ�λ�ã����ǵĵ����ڳ����¾�Ϊ��ɫ���壬��Ϊ�����ڷǽ���Ԫ�أ�ԭ��������������ZΪN��WΪO��Yԭ�ӵ��������������ڲ��������2������YΪC����
��1���������������֪��ZΪN�����ڵڶ����ڵ�VA�壻��2��YW2��CO2�����ڹ��ۻ��������ʽΪ![]() ����3����X��Y��Z��W����Ԫ�ؿ������ʽ����̼����泥��û������ˮ��Һ����������������Һ�ڼ��������·�Ӧ�����ӷ���ʽΪNH4++HCO3��+2OH��
����3����X��Y��Z��W����Ԫ�ؿ������ʽ����̼����泥��û������ˮ��Һ����������������Һ�ڼ��������·�Ӧ�����ӷ���ʽΪNH4++HCO3��+2OH��![]() NH3��+CO32��+2H2O����4����������ǿ�����ԣ��������������ɵ������Ȼ��⣬���ɵ��Ȼ���Ͱ�����Ӧ��ð���̣���Ӧ�Ļ�ѧ����ʽΪ8NH3+3Cl2��6NH4Cl+N2�����ݷ���ʽ��֪�÷�Ӧ�б������İ�������뷴Ӧ�İ���������֮��2��8��1��4��
NH3��+CO32��+2H2O����4����������ǿ�����ԣ��������������ɵ������Ȼ��⣬���ɵ��Ȼ���Ͱ�����Ӧ��ð���̣���Ӧ�Ļ�ѧ����ʽΪ8NH3+3Cl2��6NH4Cl+N2�����ݷ���ʽ��֪�÷�Ӧ�б������İ�������뷴Ӧ�İ���������֮��2��8��1��4��


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С���ͬѧ�ֱ����������ͼ�ס�����ʾ��ʵ�顣��ش�������⣺

��1�����Է���������ͼ�ɹ۲�___________________�����ԱȽϵó����ۡ���ͬѧ�����FeCl3��ΪFe2(SO4)3��Ϊ��������������___________________________��
��2����������������ͼ����ʾ��ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԡ�ͼ������A������Ϊ____________��ʵ������Ҫ������������____________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ���
A. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
B. NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
C. Cu2(OH)2CO3![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2
D. SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO4
(NH4)2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϵͳ�������������л���������д����Ӧ�Ľṹ��ʽ��
(1) _________��
_________��
(2) _________��
_________��
(3)3��2��ϡ__________________��
(4)1,3,5���ױ�__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ������һ��c(Na2CO3)+c(NaHCO3)=0.100 mol��L-1�Ļ����Һ����Һ��c(HCO3-)��c(CO32-)��pH�Ĺ�ϵ����ͼ��ʾ������ָ����Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����

A. pH=9����Һ�У�c(HCO3-)>c(H2CO3)+c(CO32-)
B. c(HCO3-)= c(CO32-)��E����Һ�У�c(OH-)+c(CO32-)>c(H+)+ c(H2CO3) +0.050 mol��L-1
C. pH=11����Һ�У�c(Na+)<2c(CO32-)+c(HCO3-)
D. 0.100 mol��L-1��Na2CO3��Һ�У�c(H+)+c(H2CO3) + c(HCO3-)=c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������½�0.1 mol N2��0.3 mol H2�����ܱ������з�����Ӧ��N2��3H2![]() 2NH3�����й��ڸ÷�Ӧ��˵����ȷ���� ( ��
2NH3�����й��ڸ÷�Ӧ��˵����ȷ���� ( ��
A. ���տ�����0.2 mol NH3
B. ѹ�����������ѹǿ��ʹ��Ӧ���ʼ�С
C. ���ͷ�Ӧ��ϵ���¶��ܼӿ췴Ӧ����
D. ����������䣬���������ټ���N2���ܼӿ췴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʪ����п������ͭ������Ҫ��п��ͭ�������ӣ�Cd�����ܣ�Co���ȵ��ʡ�һ����ͭ�������������ӵ��������£�

�±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ0.1mol/L���㣩��
�������� | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
��ʼ������pH | 1.5 | 6.5 | 7.2 |
������ȫ��pH | 3.3 | 9.9 | 9.5 |
��1�����������У�������ͨ������ķ������н��裬ԭ���Ƿ�ֹ��Cu���������������ӷ���ʽ��__________________��
��2�����ܹ����У�п�ۻ���As2O3�γ���ز���AsH3������ص�������ӦʽΪ_____��
��3������ʱ�ȼ�������KMnO4���ټ���ZnO����pH��
�� ���������У������ϲμӷ�Ӧ������n��KMnO4����n��Fe2+��=_________��
�� ����ʱ����ZnO���Ʒ�ӦҺpH�ķ�ΧΪ________________��
��4��������������Ͷ���KMnO4����������������Һ����FeԪ�ز��ࡣ�����ʵ�鷽��������֤��_____________________��
��5�����������Һ�ö��Ե缫���ɻ���ӵ��ʡ�����Һ�п�ѭ�����õ�������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯ����ʪ�����������ų��Ĺ�ҵ��������Ҫ�ɷ���CaSO4��2H2O��
��CaSO4��2H2O��ˮ��Ӧ��ص��Ȼ�ѧ����ʽΪ��
CaSO4��2H2O(s)=CaSO4��![]() H2O(s)+
H2O(s)+![]() H2O(g) ��H1��83.2 kJ��mol-1
H2O(g) ��H1��83.2 kJ��mol-1
CaSO4��2H2O(s)=CaSO4(s)+2H2O(l) ��H2��26 kJ��mol-1
H2O (g)=H2O(l) ��H3��-44 kJ��mol-1
��ӦCaSO4��![]() H2O(s)=CaSO4(s)+
H2O(s)=CaSO4(s)+ ![]() H2O(g)�Ħ�H4��_________kJ��mol-1��
H2O(g)�Ħ�H4��_________kJ��mol-1��
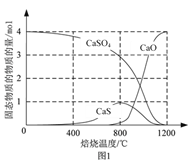
���ú��ʵĻ�ԭ�����Խ�CaSO4��ԭ������SO2�����ڹ�ҵ�������ᡣ
����CO����ԭ�����ı䷴Ӧ�¶ȿɵõ���ͬ�IJ����ͬ�¶��·�Ӧ�����ù���ɷֵ����ʵ�����ͼ1��ʾ���ڵ���800 ��ʱ��Ҫ��ԭ����Ϊ___________������800 ��ʱ��Ҫ�����ķ�Ӧ�Ļ�ѧ����ʽΪ___________��
���Ը���úΪ��ԭ������2.5 Сʱ����ͬ�����������ת���ʵ�Ӱ������ͼ2��ʾ��CaCl2��������___________�����¶ȸ���1200 ��ʱ����������CaCl2��CaSO4��ת����������ͬ����ԭ����___________��

����C����ԭ�������ܱ������м�����ͬ�����ļ��鲻ͬC/Sֵ��̿����CaSO4�����ʵ���֮�ȣ��Ļ������1100 ����ȣ��������ͼ3��ʾ����C/SֵΪ0.5ʱ����Ӧ����ΪCaO��SO2��CO2����C/Sֵ����0.7ʱ����Ӧ����������SO2�����������������������Ҫԭ�������___________��
�����÷�ӦCaSO4(s)+(NH4)2CO3(aq)![]() CaCO3(s)+(NH4)2SO4(aq)���Խ���ʯ��ת��Ϊ����李�����Ӧ�ﵽƽ�����Һ��c(SO42-)=2.0 mol��L-1����ʱ��Һ��c(CO32-)=___________������֪Ksp��CaCO3��=2.8��10-9��Ksp��CaSO4��=3.2��10-6��
CaCO3(s)+(NH4)2SO4(aq)���Խ���ʯ��ת��Ϊ����李�����Ӧ�ﵽƽ�����Һ��c(SO42-)=2.0 mol��L-1����ʱ��Һ��c(CO32-)=___________������֪Ksp��CaCO3��=2.8��10-9��Ksp��CaSO4��=3.2��10-6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A��һ�־��ô��ᵯ����Ҫ��Ч�ɷ֡�������A����Է�������Ϊ161���ҷ�����ֻ����һ������������A��F��ת����ϵ����ͼ��ʾ����������������Cu(OH)2����Һ��1molC��Ӧ������1molCu2O��lmolD, B1��B2��Ϊ���ȶ��Ļ������һ�Ϊͬ���칹�塣
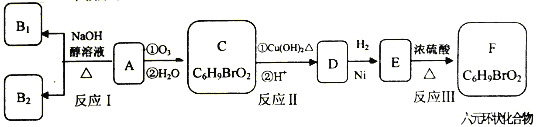
��֪����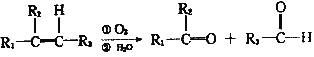
�� һ��̼ԭ������������̼̼˫���Ľṹ���ȶ���
������������⣺
��l��B1����Է���������_______��
��2��C�еĹ�������ȩ����_______��
��3��д��A ���ȵ��ռ�ˮ��Һ��Ӧ�Ļ�ѧ����ʽ��______________��
��4��д����Ӧ��Ļ�ѧ����ʽ��__________________��
��5��д����������������E������ͬ���칹��_______��
�� �������������� �����ܷ���������Ӧ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com