
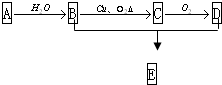
 ��ͼ��ʾ����֪A�IJ�����һ������ʯ�ͻ���ˮƽ�ı�־��D�������ԣ�E�Ǿ�����ζ�IJ�����ˮ��Һ�壮
��ͼ��ʾ����֪A�IJ�����һ������ʯ�ͻ���ˮƽ�ı�־��D�������ԣ�E�Ǿ�����ζ�IJ�����ˮ��Һ�壮| һ�������� |
| һ�������� |
| ŨH2SO4 |
| �� |
| ŨH2SO4 |
| �� |
| һ�������� |
| һ�������� |
| ŨH2SO4 |
| �� |
| ŨH2SO4 |
| �� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�








 ����д���֣�
����д���֣� ����д���֣�
����д���֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ����ʦ���С��ٴ�һ�и���12��������ѧ�Ծ����������� ���ͣ������
(8��)�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O(g)Ϊԭ�ϣ�ͨ����ӦI��II���Ʊ��״���
��ش��������⣺
(1)��1.0molCH4��2.0molH2O(g)ͨ�뷴Ӧ��(�ݻ�Ϊl00L)����һ�������·�����Ӧ��
cCH4(g)+H2O(g)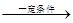 CO(g)+3H2(g) I��
CO(g)+3H2(g) I��
CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��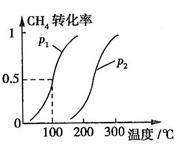
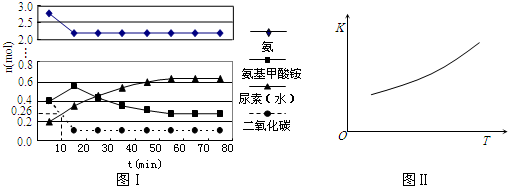
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ
��ͼ�е�P1 P2(�<������>����=��)��100��ʱƽ�ⳣ��Ϊ ��
�۸÷�Ӧ��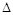 H 0��(�<������>����=��)
H 0��(�<������>����=��)
(2)��ѹǿΪ0.1MPa�����£�a molCO��3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״���CO(g)+2H2(g) CH30H(g)
CH30H(g) 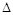 H<0 ��
H<0 ��
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� (�����)��
| A�������¶� | B����CH3OH(g)����ϵ�з��� |
| C������He��ʹ��ϵ��ѹǿ���� | D���ٳ���lmolCO��3 mol H2 |
| ʵ���� | T(��) | n(CO)��n(H2) | p(MPa) |
| l | 150 | 1��3 | 0.1 |
| 2 | n | 1��3 | 5 |
| 3 | 350 | m | 5 |
 = MPa��
= MPa��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ���ٴ�һ�и���12��������ѧ�Ծ��������棩 ���ͣ������
(8��)�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O(g)Ϊԭ�ϣ�ͨ����ӦI��II���Ʊ��״���
��ش��������⣺
(1)��1.0molCH4��2.0molH2O(g)ͨ�뷴Ӧ��(�ݻ�Ϊl00L)����һ�������·�����Ӧ��
cCH4(g)+H2O(g) 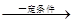 CO(g)+3H2(g)
I��
CO(g)+3H2(g)
I��
CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
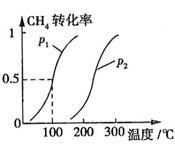
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ
��ͼ�е�P1 P2(�<������>����=��)��100��ʱƽ�ⳣ��Ϊ ��
�۸÷�Ӧ��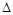 H
0��(�<������>����=��)
H
0��(�<������>����=��)
(2)��ѹǿΪ0.1MPa�����£�a molCO��3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״���CO(g)+2H2(g) CH30H(g)
CH30H(g) 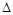 H<0 ��
H<0 ��
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� (�����)��
A�������¶� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���lmolCO��3 mol H2
��Ϊ��Ѱ�Һϳɼ״��������¶Ⱥ�ѹǿ��ijͬѧ���������ʵ�飬����ʵ�������Ѿ������������ʵ����Ʊ��С�
|
ʵ���� |
T(��) |
n(CO)��n(H2) |
p(MPa) |
|
l |
150 |
1��3 |
0.1 |
|
2 |
n |
1��3 |
5 |
|
3 |
350 |
m |
5 |
a���ϱ���ʣ���ʵ���������ݣ�n= ��m= ��
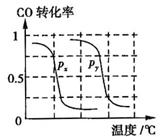
b�����ݷ�Ӧ����ص㣬��ͼ����ѹǿ�ֱ�Ϊ0.1MPa��5MPa��CO��ת�������¶ȱ仯������ͼ����ָ��ͼ�е�ѹǿ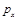 = MPa��
= MPa��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com