
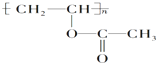
 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A、1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1mol |
| B、该有机物水解所得产物能发生取代反应 |
| C、该有机物可通过加聚反应生成 |
| D、该有机物的单体只有一种且能使溴水褪色 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口附近 |
| C、蒸发结晶时,要用玻璃棒不断搅拌,直至溶液蒸干,停止加热 |
| D、称量NaOH固体时,药品放在烧杯中置于托盘天平左盘,砝码放在右盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH溶液 |
| B、硫酸溶液 |
| C、NaCN溶液 |
| D、盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、主族金属元素的化合价均不会超过+4 |
| B、元素周期表中氧元素的位置列出的“16.00”是元素的相对原子质量 |
| C、Na2O2中阳离子与阴离子物质的量之比为1:1 |
| D、含有相同质子数和电子数的两种微粒可能是一种分子和一种离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铁溶液腐蚀铜制作印刷电路板:2Fe3++Cu=2Fe2++Cu2+ |
| B、漂白粉溶液中通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C、向碘化钾溶液中通入臭氧:O3+2I一+3H2O═6OH-+I2 |
| D、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
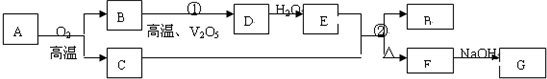
查看答案和解析>>
科目:高中化学 来源: 题型:
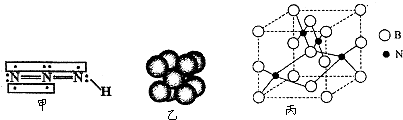
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com