
 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
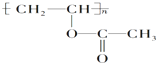 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A、1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1mol |
| B、该有机物水解所得产物能发生取代反应 |
| C、该有机物可通过加聚反应生成 |
| D、该有机物的单体只有一种且能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
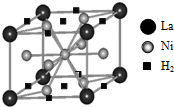 能源、材料和信息是现代社会的三大“支柱”.
能源、材料和信息是现代社会的三大“支柱”.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S(s)在氧气中燃烧的反应是放热反应 |
| B、S(s)+O2(g)═SO2(g)△H=b kJ?mol-1,则a<b |
| C、1mol SO2(g)所具有的能量低于1mol S(s)与1mol O2(g)所具有的能量之和 |
| D、16g固体硫在氧气中充分燃烧,可放出148.6kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z-+H2O?HZ+OH- |
| B、HZ+Y-═HY+Z- |
| C、HY+H2O?H3O++Y- |
| D、HX+Z-═HZ+X- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com