
| n |
| V |
| ||
| △t |
| 2.4mol |
| 2L |
| ||
| 2min |


科目:高中化学 来源: 题型:
| A、恒温密闭容器中NO2和N2O4形成的平衡体系,减小体积,体系颜色加深 |
| B、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| C、滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0×10-7 mol/L |
| B、1.0×10-6 mol/L |
| C、1.0×10-3 mol/L |
| D、1.0×10-12 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
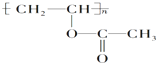 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A、1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1mol |
| B、该有机物水解所得产物能发生取代反应 |
| C、该有机物可通过加聚反应生成 |
| D、该有机物的单体只有一种且能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
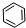 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com