
【题目】乙烯的产量是衡量一个国家石油化工水平的重要标志。聚乙烯是以乙烯为原料合成的一种人们常用的高分子材料。下列有关叙述正确的是( )
A.乙烯合成聚乙烯的反应属于化合反应
B.乙烯合成聚乙烯的化学方程式是:nCH2=CH2 ![]()
![]()
C.聚乙烯在自然界中很难降解,容易导致“白色污染”
D.聚乙烯是纯净物
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是

A. b为正极,电极反应式为:O2+4H++4e-=2H2O
B. 电解质溶液中的H+移向a电极
C. 若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
D. 呼出气体中酒精含量越高,微处理器中通过的电流越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】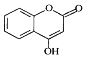 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成。
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成。
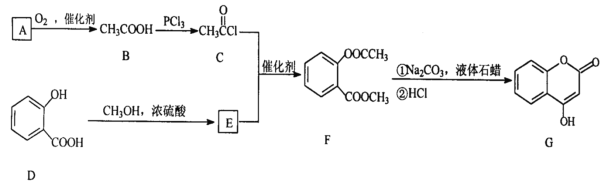
请回答下列问题:
(1)A与银氨溶液反应有银镜生成,则A的结构简式是__________________
(2)B→C的反应类型是______________
(3)写出F和过量NaOH溶液共热时反应的化学方程_______________________________
(4)下列关于G的说法正确的是______________
a.能与溴单质反应
b.能与金属钠反应
c.1molG最多能和3mol氢气反应
d.分子式是C9H7O3
(5)与D互为同分异构体且含有酚羟基、酯基的有_____________种
(6)根据已学知识和获取的信息,写出以CH3COOH,![]() 为原料合成重要的化工产品
为原料合成重要的化工产品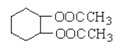 的路线流程图__________________________(无机试剂任选)合成路线流程图示例如下:CH3CH2OH
的路线流程图__________________________(无机试剂任选)合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2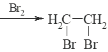
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B.1mol金刚石晶体中,平均含有2molC—C键
C.构成单质分子的微粒之间不一定存在共价键
D.某气态团簇分子结构如图所示,该分子的分子式为EF或FE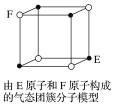
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是( )
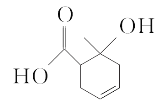
A.能和碳酸氢钠溶液反应的官能团有2种
B.1 mol该有机物最多能与2 mol H2发生加成反应
C.与![]() 互为同分异构体
互为同分异构体
D.既可以发生取代反应又可以发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的醋酸,某学生用0.100 mol/L NaOH标准溶液进行测定醋酸的浓度的实验,取20.00mL待测醋酸放入锥形瓶中,并滴加2~3滴指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。完成下列填空:
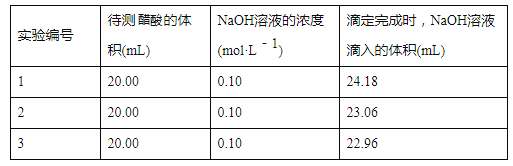
(1)量取醋酸用的仪器是__________,该实验中指示剂最好选用________,滴定时眼睛应注视________,滴定达到终点的标志是_________。
(2)排除碱式滴定管尖嘴中气泡的方法应采用以下_________操作(填甲/乙/丙),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(3)根据上述数据,可计算出该醋酸的浓度约为_________ (保留小数点后3位)。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________。
A.用滴定管取20.00mL待测醋酸,使用前,水洗后未用待测醋酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y两根金属棒插入Z溶液中构成如图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是( )
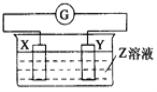
选项 | X | Y | Z |
A | Zn | Cu | 稀硫酸 |
B | Cu | Zn | 稀硫酸 |
C | Cu | Ag | 硫酸铜溶液 |
D | Ag | Zn | 硝酸银溶液 |
A.AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1)在基态Cu2+核外电子中,M层的电子运动状态有_________种。
(2)Cu2+与OH-反应能生成[Cu(OH)4]2-,[Cu(OH)4]2-中的配位原子为_____(填元素符号)。
(3)[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为________。
(4)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为________;推测抗坏血酸在水中的溶解性:________(填“难溶于水”或“易溶于水”)。
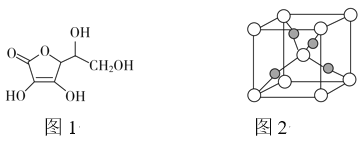
(5)一个Cu2O晶胞(如图2)中,Cu原子的数目为________。
(6)单质铜及镍都是由_______________键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于检测CO的某气敏传感器的工作原理如图所示。下列说法不正确的是

A.工作过程中化学能转化为电能
B.工作一段时间后溶液的pH几乎不变
C.电极I上发生反应:CO - 2e- + H2O = CO2 + 2H+
D.电极II上发生反应:O2 + 2H2O + 4e- = 4OH![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com